20. 为了减少CO对大气的污染,某研究性学习小组拟研究利用CO和H
2O反应转化为绿色能源H
2。已知:
2CO(g)+O
2(g)=2CO
2(g) △H=—566kJ•moL
-12H
2(g)+O
2(g)=2H
2O(g) △H=—483.6kJ•moL
-1H
2O(g)=H
2O(l) △H=—44.0kJ•moL
-1(1)写出CO和H
2O(g)作用生成CO
2和H
2的热化学方程式:___________________________。
(2)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
N
2(g)+3H
2(g)

2NH
3(g) △H=—92.4kJ/mol
当合成氨反应达到平衡后,改变某一外界条件(不改变N
2、H
2和NH
3的量),反应速率与时间的关系如图所示。

①图中t
3时引起平衡移动的条件可能是__________________________________________,其中表示平衡混合物中NH
3的含量最高的一段时间是_____________。
②温度为T℃时,将1 mol N
2和2 mol H
2放入容积为0.5 L的密闭容器中,充分反应后测得N
2的平衡转化率为50%。则反应在T℃时的平衡常数为____________mol
-2·L
2。
③目前工业合成氨的原理是:
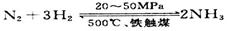
下图表示随条件改变,平衡体系中氨气体积分数的变化趋势。
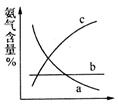
当横坐标为压强时,变化趋势正确的是(填序号,下同)__________,当横坐标为温度时,变化趋势正确的是___________。
(3)常温下氨气和HCl均极易溶于水,现将相同体积、相同物质的量浓度的氨水和盐酸混合,所得溶液中各离子的物质的量浓度按照由大到小的顺序排列依次为_______>_______>_______>________。