24. 氯化亚铜(CuCl)是一种重要的化工产品。它不溶于H
2SO
4、HNO
3 和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解氧化成绿色的碱式氯化铜[Cu
2(OH)
4-nCl
n],n随着环境酸度的改变而改变。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如图:
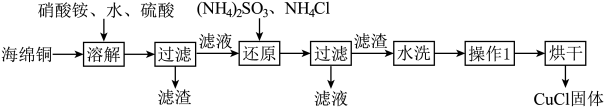
(1)还原过程中主要反应的离子方程式为
_______。
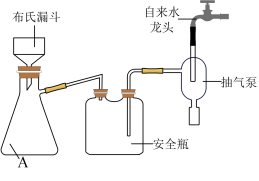
(2)实验室为了加快过滤速度,往往采用抽滤的操作(如图)。仪器A的名称
__________,有关抽滤,下列说法正确的是
__________
A.抽滤完毕,应先拆下连接抽气泵和吸滤瓶的橡胶管,再关闭水龙头,最后将滤液从吸滤瓶上口倒出
B.在布氏漏斗中放入滤纸后,直接用倾析法转移溶液和沉淀,再打开水龙头抽滤
C.在抽滤装置中洗涤晶体时,为减少晶体溶解损失,应使洗涤剂快速通过滤纸
D.减压过滤不宜用于过滤胶状或颗粒太小的沉淀
(3)操作1为马上再洗涤,然后在真空干燥机内于70℃干燥2h,冷却、密封包装。其中最合理的洗涤试剂
__________A. 浓盐酸
B. 浓氨水
C. 无水乙醇
D. 水+乙醇
真空干燥的原因是
___________。
(4)随着pH减小,Cu
2(OH)
4-nCl
n中铜的质量分数
__________A. 增大
B. 不变
C. 减小
D. 不能确定