四川大数据精准教学联盟2021届高三第二次统一监测理综化学试题
四川
高三
二模
2021-03-07
1416次
整体难度:
适中
考查范围:
常见无机物及其应用、认识化学科学、有机化学基础、化学反应原理、化学实验基础、物质结构与性质
四川大数据精准教学联盟2021届高三第二次统一监测理综化学试题
四川
高三
二模
2021-03-07
1416次
整体难度:
适中
考查范围:
常见无机物及其应用、认识化学科学、有机化学基础、化学反应原理、化学实验基础、物质结构与性质
一、单选题 添加题型下试题
单选题
|
容易(0.94)
名校
1. NSR技术可以通过交替吸附、脱附汽车尾气中的NOx将NOx、CO等进行无害化处理,其工作原理如图所示。下列说法错误的是
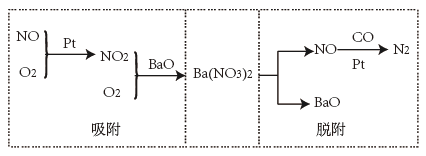

| A.CO能使血红蛋白丧失携氧功能 |
| B.空气不足时发生“吸附” |
| C.“脱附”时CO转化为CO2 |
| D.上述过程中Pt作催化剂 |
【知识点】 氮氧化物的危害及无害化处理方法解读
您最近一年使用:0次
2021-03-05更新
|
846次组卷
|
7卷引用:四川大数据精准教学联盟2021届高三第二次统一监测理综化学试题
四川大数据精准教学联盟2021届高三第二次统一监测理综化学试题(已下线)2021年高考化学押题预测卷(广东卷)(03)河北省石家庄市第二中学西校区2021-2022学年高三下学期4月月考化学试题(已下线)专题14物质的反应和转化-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题13物质的反应和转化-2022年高考真题+模拟题汇编(全国卷)(已下线)专题14物质的反应和转化-五年(2018~2022)高考真题汇编(全国卷)四川省泸县第一中学2023-2024学年高三上学期期末考试理综试题-高中化学
单选题
|
较易(0.85)
名校
2. 设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.1L0.1 mo/L NH4NO3溶液中氮原子数目为0.2NA |
| B.5.6gFe与水蒸气完全反应转移的电子数目为0.3NA |
| C.等质量的N2和CO所含原子数目均为2NA |
| D.标准状况下,5.6LCHCl3所含C—Cl键数目为0.75NA |
您最近一年使用:0次
2021-03-05更新
|
874次组卷
|
7卷引用:四川大数据精准教学联盟2021届高三第二次统一监测理综化学试题
四川大数据精准教学联盟2021届高三第二次统一监测理综化学试题(已下线)重点4 阿伏加德罗常数-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)考点02 物质的量 气体摩尔体积-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点02 物质的量 气体摩尔体积-备战2022年高考化学一轮复习考点帮(浙江专用)四川省泸州市泸县第一中学2022-2023学年高三上学期期末考试化学试题2024届四川省合江县马街中学校高三上学期一诊模拟考试理综试题(已下线)热点04 有关阿伏加德罗常数的正误判断
单选题
|
适中(0.65)
解题方法
3. 亚胺培南是一种抗生素,其结构如图所示。下列有关亚胺培南的叙述错误的是
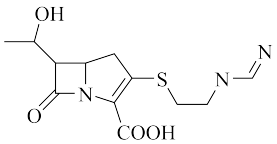

| A.分子中含有3个双键 |
| B.分子中含有1个甲基 |
| C.能发生酯化反应 |
| D.能使酸性高锰酸钾溶液褪色 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
4. 在下表中,根据实验操作和现象能得出相应结论的是
| 选项 | 实验操作和现象 | 结论 |
| A | 取少量某溶液于试管中,滴加少量氯水,振荡;再滴入几滴淀粉溶液,溶液变蓝色 | 原溶液含有I- |
| B | 向盛有Mg(OH)2悬浊液的试管中滴入适量CuSO4溶液,振荡,有蓝色絮状沉淀生成 | Ksp[Mg(OH)2]> Ksp[Cu(OH)2] |
| C | 取1 mL 20%的蔗糖溶液,加入3~5滴稀硫酸。水浴加热5 min,冷却。再向其中加入新制银氨溶液,振荡,水浴加热,无银镜产生 | 蔗糖没有水解 |
| D | 用酒精灯加热铝箔,铝箱熔化但不滴落 | Al的熔点高于Al2O3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
5. 短周期主族元素xX、yY、zZ、mM的原子序数依次增大,其中m=x+z,Y与X组成无色气体甲,Y与Z组成淡黄色粉末乙,甲与乙反应生成Y的单质。下列说法错误的是
| A.乙中阴、阳离子个数比为1:2 | B.M在周期表中位于第VIIA族 |
| C.简单氢化物的沸点: M>Y | D.X可形成多种同素异形体 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
6. Li/SOCl2 电池以锂、碳膜为电极,LiAlCl4(SOCl2)为电解质溶液,为防止锂电极上形成致密的LiCl薄膜产生电压滞后现象,可采用如图所示的双膜结构。该电池工作时的总反应为4Li+ 2SOCl2=S+ SO2+ 4LiCl。下列说法错误的是


| A.锂为电池的负极 |
| B.锂电极周围需使用阳离子交换膜 |
| C.碳膜上的电极反应为2SOCl2+4e- =S+ SO2 +4Cl- |
| D.电流由锂电极流经负载、碳膜、电解质溶液回到锂电极 |
您最近一年使用:0次
单选题
|
较难(0.4)
解题方法
7. 室温下,以酚酞为指示剂,用NaOH溶液滴定一元弱酸HX,测得HX的分布系数 与溶液pH的关系如图所示。下列说法正确的是
与溶液pH的关系如图所示。下列说法正确的是

 与溶液pH的关系如图所示。下列说法正确的是
与溶液pH的关系如图所示。下列说法正确的是
| A.终点溶液中: c(Na+)=c(X -) | B.b点溶液中: c(Na+)>c(X- ) |
| C.HX的电离平衡常数为104.75 | D.水的电离程度大小: a> b |
【知识点】 电离平衡常数及影响因素解读 盐溶液中离子浓度大小的比较解读
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
解题方法
8. 光敏剂草酸铁钾晶体(化学式为K3[Fe(C2O4)3]•H2O)是一种含铁(III)的配合物,某学习小组进行了草酸铁钾晶体的性质探究实验。回答下列问题:
实验1:探究草酸铁钾的光敏性
(1)取草酸铁钾溶液按如图甲所示装置进行实验。实验中观察到A中产生浅黄色沉淀,取少量浅黄色沉淀与K3[Fe(CN)6]溶液混合,产生蓝色沉淀,则浅黄色沉淀中铁元素的化合价为___________ 。 实验中还观察到B中澄清石灰水变浑浊,则光解产生了___________ (填化学式)。

查阅资料得知草酸铁钾晶体光解与其溶液光解原理相似,X射线研究表明其光解后的残留固体为两种草酸盐。草酸铁钾晶体光解反应的化学方程式为___________ 。
实验2:探究草酸铁钾晶体光解后残留固体的热稳定性
取草酸铁钾晶体充分光解后的残留固体按图乙所示装置进行实验:

(2)装置连接好后,首先需要进行的实验操作是___________ ,装置D的作用是___________ 。
(3) A中放置下表所列固体,打开K,通入一段时间N2.然后关闭K。先点燃F处酒精灯,再将A中温度控制在指定范围,加热到不再有气体生成为止。记录到B、D、F、G中的现象如下:
进一步探究发现,实验②结束后A中残留固体由黑色不溶性固体和K2CO3组成。
查阅资料得知: 230~ 380°C时浅黄色固体分解,560~800°C时草酸钾分解。上述黑色不溶性固体中的物质可能是___________ ,草酸钾分解反应的化学方程式为___________ 。
(4)写出一种尾气处理的方法___________ 。
实验1:探究草酸铁钾的光敏性
(1)取草酸铁钾溶液按如图甲所示装置进行实验。实验中观察到A中产生浅黄色沉淀,取少量浅黄色沉淀与K3[Fe(CN)6]溶液混合,产生蓝色沉淀,则浅黄色沉淀中铁元素的化合价为

查阅资料得知草酸铁钾晶体光解与其溶液光解原理相似,X射线研究表明其光解后的残留固体为两种草酸盐。草酸铁钾晶体光解反应的化学方程式为
实验2:探究草酸铁钾晶体光解后残留固体的热稳定性
取草酸铁钾晶体充分光解后的残留固体按图乙所示装置进行实验:

(2)装置连接好后,首先需要进行的实验操作是
(3) A中放置下表所列固体,打开K,通入一段时间N2.然后关闭K。先点燃F处酒精灯,再将A中温度控制在指定范围,加热到不再有气体生成为止。记录到B、D、F、G中的现象如下:
| 实验序号 | A中固体 | 控制温度 | B | D | F | G |
| ① | 草酸铁钾晶体充分光解后的残留固体 | 230~380℃ | 出现白色浑浊 | 无明显变化 | 固体变成红色 | 出现白色浑浊 |
| ② | 实验①结束后的残留固体 | 560~800℃ | 无明显变化 | 无明显变化 | 固体变成红色 | 出现白色浑浊 |
查阅资料得知: 230~ 380°C时浅黄色固体分解,560~800°C时草酸钾分解。上述黑色不溶性固体中的物质可能是
(4)写出一种尾气处理的方法
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
解题方法
9. 砷钴矿主要成分为CoAs3,还含有CoAs、Fe3As2、CuO、FeO、 SiO2等成分。利用砷钴矿制备醋酸钻钴[(CH3COO)2Co]的流程如下图所示。流程中的“焙砂”含CoO、Co2O3、CuO、Fe2O3、 CoSiO3,“酸浸液”含Fe2+、 Co2+、 Cu2+、 H+。

回答下列问题:
(1)砷钴矿“电炉熔炼"时CoAs3)首先分解为Co3As2和As(g),若该反应中只有As,的化合价发生改变,则被氧化与被还原的As的物质的量之比为_______ 。
(2)冰钴“自热焙烧”生成的As2O3俗称砒霜,它可转化为砷化氢,砷化氢的化学式为___________ 。
(3)焙砂“酸浸”时所得“浸渣"的化学式为__ ,生成O2的反应的离子方程式__ 。
(4)常温下,部分金属氢氧化物的溶度积常数如下表:
“第一次除铁”时调节pH至5,Cu2+部分沉淀,溶液中剩余Cu2+的浓度为___________ mol/L。
滤渣2的化学式为___________ “第二次除铁”时若改用同浓度的NaClO溶液,Co2+会被氧化为Co3+,由此可知ClO 、ClO-、Co3+氧化能力由强到弱的顺序为
、ClO-、Co3+氧化能力由强到弱的顺序为___________ 。
(5)“萃取铁铜”时,环烷酸对不同金属离子的萃取率与溶液pH的关系如图所示。据图分析萃取时溶液pH的适宜范围为___________ (填正确答案标号)。
A.1~3 B.3~5 C.4~6 D.5~7

萃取前需要加NaClO3溶液处理的原因是___________ 。

回答下列问题:
(1)砷钴矿“电炉熔炼"时CoAs3)首先分解为Co3As2和As(g),若该反应中只有As,的化合价发生改变,则被氧化与被还原的As的物质的量之比为
(2)冰钴“自热焙烧”生成的As2O3俗称砒霜,它可转化为砷化氢,砷化氢的化学式为
(3)焙砂“酸浸”时所得“浸渣"的化学式为
(4)常温下,部分金属氢氧化物的溶度积常数如下表:
| 氢氧化物 | Co(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶度积常数(Ksp) | 2×10-15 | 5×10-20 | 2×10-15 | 1×10-38 |
“第一次除铁”时调节pH至5,Cu2+部分沉淀,溶液中剩余Cu2+的浓度为
滤渣2的化学式为
 、ClO-、Co3+氧化能力由强到弱的顺序为
、ClO-、Co3+氧化能力由强到弱的顺序为(5)“萃取铁铜”时,环烷酸对不同金属离子的萃取率与溶液pH的关系如图所示。据图分析萃取时溶液pH的适宜范围为
A.1~3 B.3~5 C.4~6 D.5~7

萃取前需要加NaClO3溶液处理的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
解题方法
10. 氮的氧化物与空气中的氧气、温室气体(如甲烷)发生的反应,都会对空气质量产生一定的影响。
(1)科学家探索利用甲烷将氮的氧化物还原为氮气和水蒸气。已知有下列反应:
i. CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) △H = -801 kJ/mol
ii.N2(g) + O2(g) = 2NO(g) ∆H= +180 kJ/mol
ii.2NO(g) + O2(g) = 2NO2(g) △H= -114 kJ/mol
则甲烷直接将NO2还原为N2的热化学方程式为___________ 。
(2)下表是不同温度下NO (g)+ O2(g)
O2(g)  NO2(g)的平衡常数:
NO2(g)的平衡常数:
①为提高NO的转化率,可采取的措施有___________ (写两条);
②774K时,将4 mol NO和2mol O2充入1L恒容密闭容器中,不能判断反应已达到化学平衡状态的是___________ (填正确答案标号)。。
A.容器中压强不再变化 B. v正(O2)=2v逆(NO2)
C. c(NO):c(O2):c(NO2)=2:1:2 D.混合气体的密度保持不变
E.NO的转化率达50%
(3)我国科学家在研究CH4与NO2的反应机理时发现,该反应有3个途径(如图甲)R1、R2和R3,分别生成CH3+ HNO2、CH3+ tran-HONO(反式)和CH3+ cis-HIONO(顺式),对应的中间状态分别为TS1、TS2和TS3. R1、R2和R3的速率常数(一定温度时,反应物单位浓度时的反应速率)分别记为k1、k2和k3,总反应的速率常数为k, k=k1+ k2+k3,1380~1800K温度范围内的速率常数变化如图乙。
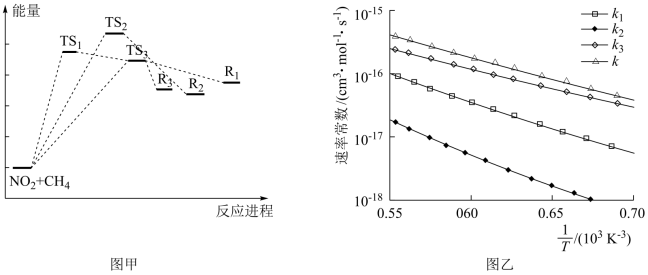
①从能量变化来看,反应速率最快的是________ (填“ R1”“R2”或“R3"),原因是_______ ;
②从速率常数来看,对总反应速率影响最大的是______ (填“R1”“R2”或“R3"),原因是______ 。
③下列有关说法正确的是________ (填正确答案标号)。
A.HNO2比tran-HONO和cisHONO都稳定
B.在高温时,R1和R3会相互竞争
C.温度升高,3个反应的速率常数都增大
D.CH4与NO2存在多种反应机理,R1是主要反应
(1)科学家探索利用甲烷将氮的氧化物还原为氮气和水蒸气。已知有下列反应:
i. CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) △H = -801 kJ/mol
ii.N2(g) + O2(g) = 2NO(g) ∆H= +180 kJ/mol
ii.2NO(g) + O2(g) = 2NO2(g) △H= -114 kJ/mol
则甲烷直接将NO2还原为N2的热化学方程式为
(2)下表是不同温度下NO (g)+
 O2(g)
O2(g)  NO2(g)的平衡常数:
NO2(g)的平衡常数:| T/K | 300 | 400 | 500 | 774 |
| K/(mol·L)-/2 | 1.1×106 | 3.7×103 | 1.2×102 | 1.0 |
①为提高NO的转化率,可采取的措施有
②774K时,将4 mol NO和2mol O2充入1L恒容密闭容器中,不能判断反应已达到化学平衡状态的是
A.容器中压强不再变化 B. v正(O2)=2v逆(NO2)
C. c(NO):c(O2):c(NO2)=2:1:2 D.混合气体的密度保持不变
E.NO的转化率达50%
(3)我国科学家在研究CH4与NO2的反应机理时发现,该反应有3个途径(如图甲)R1、R2和R3,分别生成CH3+ HNO2、CH3+ tran-HONO(反式)和CH3+ cis-HIONO(顺式),对应的中间状态分别为TS1、TS2和TS3. R1、R2和R3的速率常数(一定温度时,反应物单位浓度时的反应速率)分别记为k1、k2和k3,总反应的速率常数为k, k=k1+ k2+k3,1380~1800K温度范围内的速率常数变化如图乙。

①从能量变化来看,反应速率最快的是
②从速率常数来看,对总反应速率影响最大的是
③下列有关说法正确的是
A.HNO2比tran-HONO和cisHONO都稳定
B.在高温时,R1和R3会相互竞争
C.温度升高,3个反应的速率常数都增大
D.CH4与NO2存在多种反应机理,R1是主要反应
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
名校
解题方法
11. 2020年底,我国嫦娥五号月球探测器成功发射,进行无人采样后已顺利回收。
(1)月球表面的月海玄武岩中富含钛和铁,基态钛原子的核外电子排布式是____ ,基态铁原子核外电子占据的最高能级是____ 。
(2)将月海玄武岩用硝酸溶解,所得溶液用KSCN检验,溶液呈红色。KSCN中K、C、N的电负性从大到小的顺序是______ ,C 原子的杂化轨道类型是____ ,SCN-的空间构型是______ ,SCN- 中含有的 键数目是
键数目是______ 。
(3)嫦娥五号采样机中的钻杆是由中国科学院科学家研制的碳化硅增强铝基复合材料制成,具有轻质、高刚度、高强度和耐磨损等特点。
①铝基复合材料中有一种重要的物质氮化铝(AlN, 熔点为2249°C),氮化铝属类金刚石氮化物,则它属于______ (填晶体类型名称)。氮化铝可用氧化铝(增点为2054°C)为原料来制取,从晶体类型角度分析AlN的熔点比氧化铝高的原因是______ 。
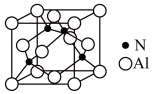
②氮化铝的晶体结构如图所示,其中铝原子的配位数是___________ ,Al与N原子最近的距离为acm,则该晶体的密度为_____ g/cm3 (写出表达式即可)。
(1)月球表面的月海玄武岩中富含钛和铁,基态钛原子的核外电子排布式是
(2)将月海玄武岩用硝酸溶解,所得溶液用KSCN检验,溶液呈红色。KSCN中K、C、N的电负性从大到小的顺序是
 键数目是
键数目是(3)嫦娥五号采样机中的钻杆是由中国科学院科学家研制的碳化硅增强铝基复合材料制成,具有轻质、高刚度、高强度和耐磨损等特点。
①铝基复合材料中有一种重要的物质氮化铝(AlN, 熔点为2249°C),氮化铝属类金刚石氮化物,则它属于
②氮化铝的晶体结构如图所示,其中铝原子的配位数是

您最近一年使用:0次
2021-03-05更新
|
571次组卷
|
3卷引用:四川大数据精准教学联盟2021届高三第二次统一监测理综化学试题
四川大数据精准教学联盟2021届高三第二次统一监测理综化学试题河北省石家庄市第二中学西校区2021-2022学年高三下学期4月月考化学试题(已下线)03 物质结构与性质综合题型集训(3) (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
解答题-有机推断题
|
适中(0.65)
12. 世界上第一种商业化合成的抗菌药物百浪多息( )对于治疗溶血性链球菌感染有很强的功效,其合成路线如下:
)对于治疗溶血性链球菌感染有很强的功效,其合成路线如下:
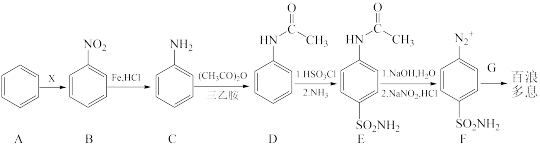
已知:
(1)A→B的反应需要添加的试剂X有___ , B的名称是___ , C 的官能团名称是__ 。
(2) C→D的化学反应方程式为____ , 该反应的类型是____ 。
(3)若F与G的反应无其它有机产物生成,则G的结构简式为_____ 。
(4) D有多种同分异构体,同时满足下列条件的同分异构体的结构简式为___ 。
①有两种官能团,苯环上有两个支链:
②能发生银镜反应;
③核磁共振氢谱中有五组峰,峰面积之比为2:2:2:2:1。
(5)写出由 制备
制备  的合成路线
的合成路线___________ (无机试剂任选)。
 )对于治疗溶血性链球菌感染有很强的功效,其合成路线如下:
)对于治疗溶血性链球菌感染有很强的功效,其合成路线如下:
已知:

(1)A→B的反应需要添加的试剂X有
(2) C→D的化学反应方程式为
(3)若F与G的反应无其它有机产物生成,则G的结构简式为
(4) D有多种同分异构体,同时满足下列条件的同分异构体的结构简式为
①有两种官能团,苯环上有两个支链:
②能发生银镜反应;
③核磁共振氢谱中有五组峰,峰面积之比为2:2:2:2:1。
(5)写出由
 制备
制备  的合成路线
的合成路线
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、认识化学科学、有机化学基础、化学反应原理、化学实验基础、物质结构与性质
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 氮氧化物的危害及无害化处理方法 | |
| 2 | 0.85 | 阿伏加德罗常数的应用 气体物质与NA相关的推算 氧化还原反应与NA相关推算 物质结构基础与NA相关推算 | |
| 3 | 0.65 | 烯烃与强氧化性物质的反应 羧酸酯化反应 多官能团有机物的结构与性质 | |
| 4 | 0.65 | 铝与氧气的反应 溶度积规则及其应用 蔗糖水解相关实验 常见阴离子的检验 | |
| 5 | 0.85 | 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 | |
| 6 | 0.65 | 原电池正负极判断 原电池电极反应式书写 新型电池 | |
| 7 | 0.4 | 电离平衡常数及影响因素 盐溶液中离子浓度大小的比较 | |
| 二、解答题 | |||
| 8 | 0.65 | 物质性质的探究 | 实验探究题 |
| 9 | 0.65 | 氧化性、还原性强弱的比较 氧化还原反应有关计算 溶度积常数相关计算 常见无机物的制备 | 工业流程题 |
| 10 | 0.65 | 盖斯定律与热化学方程式 化学平衡图像分析 化学平衡状态的判断方法 化学平衡常数的影响因素及应用 | 原理综合题 |
| 11 | 0.65 | 物质结构与性质综合考查 利用杂化轨道理论判断化学键杂化类型 晶胞的有关计算 | 结构与性质 |
| 12 | 0.65 | 根据要求书写同分异构体 根据题给物质选择合适合成路线 有机推断综合考查 | 有机推断题 |



