下列关于甲、乙、丙、丁四个图象的说法中,正确的是( )
A.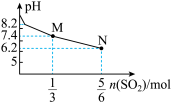 表示用1 L 1 mol·L-1 Na2SO3溶液吸收SO2时溶液pH随SO2的物质的量的变化,则M点时溶液中:c(SO32-)>c(HSO3‑) 表示用1 L 1 mol·L-1 Na2SO3溶液吸收SO2时溶液pH随SO2的物质的量的变化,则M点时溶液中:c(SO32-)>c(HSO3‑) |
B. a点Kw的数值比b点Kw的数值大 a点Kw的数值比b点Kw的数值大 |
C. 表示MOH和ROH两种一元碱的溶液分别加水稀释时的pH变化,由图可得碱性:ROH>MOH 表示MOH和ROH两种一元碱的溶液分别加水稀释时的pH变化,由图可得碱性:ROH>MOH |
D.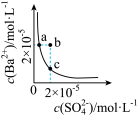 表示某温度时,BaSO4在水中的沉淀溶解平衡曲线,则加入Na2SO4可以使溶液由a点变到b点 表示某温度时,BaSO4在水中的沉淀溶解平衡曲线,则加入Na2SO4可以使溶液由a点变到b点 |
更新时间:2020-05-13 11:02:39
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下列说法正确的是( )
| A.常温下,向水中加入少量固体硫酸氢钠,c(H+)增大,Kw变大 |
| B.0.1 mol·L-1的醋酸加水稀释,c(CH3COOH)/c(CH3COO-)减小,但K不变。 |
| C.足量体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量)后者用时少 |
| D.25℃,在AgCl悬浊液中加入少量NaCl固体,c(Ag+)减小,Ksp(AgCl)减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】根据下列实验操作和现象,得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 常温下,用pH计分别测定等体积1  溶液和0.1 溶液和0.1  溶液的pH,测得的pH值相同 溶液的pH,测得的pH值相同 | 浓度对水的电离程度无影响 |
| B | 灼烧铜丝至其表面变黑、灼热,伸入盛有某有机物的试管中,铜丝恢复亮红色 | 该有机物中可能有醇羟基或羧基 |
| C | 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去,试管里出现凝胶 | 非金属性:Cl>Si |
| D | 加热麦芽糖和稀 混合溶液,冷却;加入NaOH溶液后加入银氨溶液,加热,出现银镜 混合溶液,冷却;加入NaOH溶液后加入银氨溶液,加热,出现银镜 | 麦芽糖发生了水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】常温下,分别取未知浓度的MOH和HA溶液,加水稀释至原体积的n倍。稀释过程中,两溶液pH的变化如图所示。下列叙述正确的是
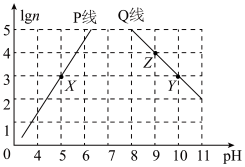
| A.P线代表HA的稀释图像且HA为强酸 |
| B.水的电离程度:Z>Y=X |
C.将X点溶液与Y点溶液混合至中性时, |
D.将X点溶液与Z点溶液等体积混合,所得溶液中一定有: |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】两种一元碱MOH和ROH的溶液分别加水稀释,溶液pH的变化如图所示,下列叙述正确的是


| A.MOH是一种弱碱 |
| B.在x点,c(M+)=c(R+) |
| C.稀释前,c(ROH)="10" c(MOH) |
| D.稀释前MOH溶液和ROH溶液中由水电离出的c(OH﹣)后者是前者的 10倍 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】常温时,1mol·L-1的CH3NH2和1mol·L-1的NH2OH(NH2OH+H2O NH3OH++OHˉ)两种碱溶液,起始时的体积均为10mL,分别向两溶液中加水进行稀释,所得曲线如图所示(V表示溶液的体积),pOH=-lgc(OH-)。下列说法正确的是
NH3OH++OHˉ)两种碱溶液,起始时的体积均为10mL,分别向两溶液中加水进行稀释,所得曲线如图所示(V表示溶液的体积),pOH=-lgc(OH-)。下列说法正确的是

 NH3OH++OHˉ)两种碱溶液,起始时的体积均为10mL,分别向两溶液中加水进行稀释,所得曲线如图所示(V表示溶液的体积),pOH=-lgc(OH-)。下列说法正确的是
NH3OH++OHˉ)两种碱溶液,起始时的体积均为10mL,分别向两溶液中加水进行稀释,所得曲线如图所示(V表示溶液的体积),pOH=-lgc(OH-)。下列说法正确的是
| A.NH2OH的电离常数K的数量级为10-8 |
B.CH3NH3Cl盐溶液中水解离子方程式为:CH3NH2+H2O CH3NH3++OH- CH3NH3++OH- |
C.当两溶液均稀释至lg =4时,溶液中水的电离程度:NH2OH >CH3NH2 =4时,溶液中水的电离程度:NH2OH >CH3NH2 |
| D.浓度相同的CH3NH3Cl和NH3OHCl的混合溶液中离子浓度大小关系:c(CH3NH3+)<c(NH3OH+) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】磷酸(H3PO4)是一种中强酸,常温下,H3PO4水溶液中含磷微粒的分布分数(平衡时某微粒的浓度占各含磷微粒总浓度的分数)与pH的关系如下图,下列说法正确的是
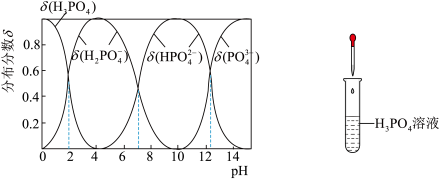

| A.滴加NaOH溶液至pH=7,溶液中c(Na+)>c(H2PO4-)+c(HPO42—)+c(PO43—) |
| B.该温度下,H3PO4的三级电离常数Ka3>10-12 |
| C.H3PO4的电离方程式为:H3PO4⇌ 3H+ + PO43— |
| D.滴加少量Na2CO3溶液,化学反应方程式为3 Na2CO3 + 2H3PO4=2Na2PO4+3H2O+3CO2↑ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知:pKa=-lgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19。用0.1 mol·L-1NaOH溶液滴定20mL 0.1mol·L-1H2SO3溶液的滴定曲线如下图所示(曲线上的数字为pH)。下列说法正确的是

A.a点所得溶液中:2c(HSO )+c(SO )+c(SO )=0.1mol/L )=0.1mol/L |
B.b点所得溶液中:c(H+)+c(SO )=c(OH-)+c(H2SO3) )=c(OH-)+c(H2SO3) |
C.c点所得溶液中:c(Na+)>3c(HSO ) ) |
D.e点所得溶液中:c(Na+)>c(SO )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】已知某温度时CH3COOH的电离平衡常数为K。该温度下向20mL0.1mol•L-1CH3COOH溶液中逐滴加入0.1mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法中错误的是


| A.a点表示的溶液中c(CH3COO-)=10-3mol•L-1 |
| B.b点表示的溶液中c(CH3COO-)>c(Na+) |
| C.c点表示CH3COOH和NaOH恰好反应完全 |
| D.d点表示的溶液中c(CH3COO-)<c(Na+) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】已知HA是一元弱酸,MA是难溶盐,且 不发生水解。常温下,向某
不发生水解。常温下,向某 的溶液中逐滴加入MOH溶液后,溶液中
的溶液中逐滴加入MOH溶液后,溶液中 和
和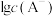 随
随 的变化关系如下图所示。下列说法错误的是
的变化关系如下图所示。下列说法错误的是
 不发生水解。常温下,向某
不发生水解。常温下,向某 的溶液中逐滴加入MOH溶液后,溶液中
的溶液中逐滴加入MOH溶液后,溶液中 和
和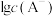 随
随 的变化关系如下图所示。下列说法错误的是
的变化关系如下图所示。下列说法错误的是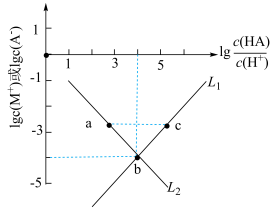
A.曲线 表示 表示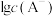 随 随 的变化 的变化 |
B.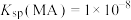 |
| C.pH:a>c |
D.b点时溶液中存在: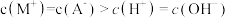 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】湿法提银工艺中,浸出的Ag+需加入Cl-进行沉淀。25℃时,平衡体系中含Ag微粒的分布系数δ[如δ(AgCl )=
)=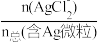 ]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是

 )=
)=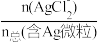 ]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
| A.25℃时,AgCl的溶解度随c(Cl-)增大而不断减小 |
| B.沉淀最彻底时,溶液中c(Ag+)=10-7.21mol·L-1 |
C.当c(Cl-)=10-2.54mol·L-1时,溶液中c(Ag+)>c(AgCl )>c(Cl )>c(Cl ) ) |
D.25℃时,AgCl +Cl- +Cl- AgCl AgCl 的平衡常数K=100.2 的平衡常数K=100.2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】稀土是“工业味精”,老一辈无产阶级革命家邓小平同志曾说过“中东有石油,我们有稀土”。稀土元素铈(Ce)主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是
| A.工业上可以电解Ce(SO4)2溶液制备铈单质 |
B.向Ce(SO4)2溶液中通入SO2,其离子方程式为2Ce4++SO2+2H2O=2Ce3++SO +4H+ +4H+ |
| C.常温下,已知Ksp[Ce(OH)3]=1.0×10-20,则Ce3+在pH为5.0时恰好完全沉淀 |
D.四种铈的核素'器 Ce、 Ce、 Ce、 Ce、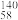 Ce、 Ce、 Ce,它们之间可以通过化学反应进行转化 Ce,它们之间可以通过化学反应进行转化 |
您最近一年使用:0次



