CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为______ (写离子符号);若所得溶液c( )∶c(
)∶c( )=2∶1,溶液pH=
)=2∶1,溶液pH=___________ 。(室温下,H2CO3的K1=4×10−7;K2=5×10−11)
(2)CO2与CH4经催化重整,制得合成气:CH4(g)+ CO2(g)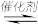 2CO (g)+ 2H2(g),已知上述反应中相关的化学键键能数据如下:
2CO (g)+ 2H2(g),已知上述反应中相关的化学键键能数据如下:
则该反应的ΔH=_________ 。分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是_______ (填“A” 或“B ”)。
(3)O2辅助的Al~CO2电池工作原理如图所示。
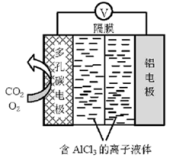
该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。电池的负极反应式:________ ,电池的正极反应式:6O2+6e−=6O ;6CO2+6O2−=3
;6CO2+6O2−=3 + 6O2,反应过程中O2的作用是
+ 6O2,反应过程中O2的作用是________ 。
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为
 )∶c(
)∶c( )=2∶1,溶液pH=
)=2∶1,溶液pH=(2)CO2与CH4经催化重整,制得合成气:CH4(g)+ CO2(g)
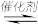 2CO (g)+ 2H2(g),已知上述反应中相关的化学键键能数据如下:
2CO (g)+ 2H2(g),已知上述反应中相关的化学键键能数据如下:| 化学键 | C—H | C=O | H—H | C O(CO) O(CO) |
| 键能/kJ·mol−1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=
(3)O2辅助的Al~CO2电池工作原理如图所示。

该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。电池的负极反应式:
 ;6CO2+6O2−=3
;6CO2+6O2−=3 + 6O2,反应过程中O2的作用是
+ 6O2,反应过程中O2的作用是
18-19高二上·江西九江·阶段练习 查看更多[1]
(已下线)【南昌新东方】江西省九江第一中学2018-2019学年高二上学期第二次月考化学试题
更新时间:2020-06-15 20:00:40
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)已知:①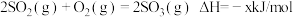
②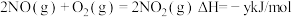
则反应 的ΔH=
的ΔH=___________ kJ·mol−1。反应②的ΔS___________ (填“>”或“<”)0,若y>0,则反应②在___________ (填“高温”“低温”或“任何温度”)下能自发进行。
(2)已知: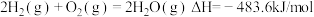 ,查阅文献资料,化学键的键能如下表:
,查阅文献资料,化学键的键能如下表:
①氨分解反应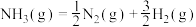 的活化能Ea1=300kJ·mol−1,则合成氨反应
的活化能Ea1=300kJ·mol−1,则合成氨反应 的活化能Ea2=
的活化能Ea2=___________ kJ·mol−1。
②氨气完全燃烧生成N2(g)和气态水的热化学方程式为___________ 。
(3)奥运会火炬常用的燃料为丙烷、丁烷等。已知:丙烷的燃烧热ΔH1=−2220kJ/mol;正丁烷的燃烧热ΔH2=−2878kJ/mol,异丁烷的燃烧热ΔH3=−2869.6kJ/mol。
①写出丙烷燃烧热的热化学方程式___________ 。
②下列有关说法不正确的是___________ 。
A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.异丁烷分子中的碳氢键比正丁烷的多
C.正丁烷比异丁烷稳定
(1)已知:①
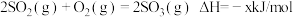
②
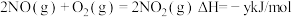
则反应
 的ΔH=
的ΔH=(2)已知:
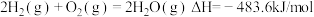 ,查阅文献资料,化学键的键能如下表:
,查阅文献资料,化学键的键能如下表:| 化学键 | H−H键 | N≡N键 | N−H键 |
| E/(kJ·mol−1) | 436 | 946 | 391 |
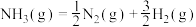 的活化能Ea1=300kJ·mol−1,则合成氨反应
的活化能Ea1=300kJ·mol−1,则合成氨反应 的活化能Ea2=
的活化能Ea2=②氨气完全燃烧生成N2(g)和气态水的热化学方程式为
(3)奥运会火炬常用的燃料为丙烷、丁烷等。已知:丙烷的燃烧热ΔH1=−2220kJ/mol;正丁烷的燃烧热ΔH2=−2878kJ/mol,异丁烷的燃烧热ΔH3=−2869.6kJ/mol。
①写出丙烷燃烧热的热化学方程式
②下列有关说法不正确的是
A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.异丁烷分子中的碳氢键比正丁烷的多
C.正丁烷比异丁烷稳定
您最近一年使用:0次
【推荐2】甲醇是一种很好的燃料,工业上可用多种原料通过不同的反应制得甲醇.
(1)已知在常温常压下:
CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=-442.8kJ∙mol﹣1
2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ∙mol﹣1
H2O(g)=H2O(l) △H=-44.0kJ∙mol﹣1
则2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H=
(2)已知C(s)+H2O(g)=CO(g)+H2(g) △H=akJ·mol-1
2C(s)+O2(g)=2CO(g) △H=-220kJ·mol-1
H-H、O=O和O-H键的键能分别为436、496和462kJ·mol-1,则a为____________________
(3)工业上正在研究利用来生产甲醇燃料的方法,该反应为:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0kJ∙mol﹣1
CH3OH(g)+H2O(g) △H=-49.0kJ∙mol﹣1
在某温度下,将6mol CO2和8mol H2充入容积为2L的密闭容器中,8分钟时达平衡状态,H2的转化率为75%.请回答:
①用CH3OH表示该反应在0~8min内的平均反应速率v(CH3OH)=_____ .
②此温度下该反应平衡常数K=_____ ;
(4)一氧化碳与氢气也可以合成甲醇:CO(g)+2H2(g) CH3OH(g) △H<0
CH3OH(g) △H<0
①若该反应在恒温恒容条件下进行,下列说法正确的是_____ ;
a.若混合气体的密度不再改变,说明反应已达化学平衡状态
b.反应达到平衡后,通入CH3OH(g)使压强增大,平衡向右移动
c.反应达到平衡后,通入氩气使压强增大,平衡向右移动
d.反应达到平衡后,升高温度,平衡逆向移动,平衡常数减小
e.若使用催化剂,会改变反应的途径,但反应热不变
②某温度下,在一个容积为2L的密闭容器中进行该反应,已知此温度下的平衡常数K=50L2∙mol﹣2,反应到某时刻测得各组分的物质的量如下:
请比较此时正、逆反应速率的大小:v正_____ v逆(填“>”、“<”或“=”).
(1)已知在常温常压下:
CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=-442.8kJ∙mol﹣1
2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ∙mol﹣1
H2O(g)=H2O(l) △H=-44.0kJ∙mol﹣1
则2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H=
(2)已知C(s)+H2O(g)=CO(g)+H2(g) △H=akJ·mol-1
2C(s)+O2(g)=2CO(g) △H=-220kJ·mol-1
H-H、O=O和O-H键的键能分别为436、496和462kJ·mol-1,则a为
(3)工业上正在研究利用来生产甲醇燃料的方法,该反应为:
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=-49.0kJ∙mol﹣1
CH3OH(g)+H2O(g) △H=-49.0kJ∙mol﹣1在某温度下,将6mol CO2和8mol H2充入容积为2L的密闭容器中,8分钟时达平衡状态,H2的转化率为75%.请回答:
①用CH3OH表示该反应在0~8min内的平均反应速率v(CH3OH)=
②此温度下该反应平衡常数K=
(4)一氧化碳与氢气也可以合成甲醇:CO(g)+2H2(g)
 CH3OH(g) △H<0
CH3OH(g) △H<0①若该反应在恒温恒容条件下进行,下列说法正确的是
a.若混合气体的密度不再改变,说明反应已达化学平衡状态
b.反应达到平衡后,通入CH3OH(g)使压强增大,平衡向右移动
c.反应达到平衡后,通入氩气使压强增大,平衡向右移动
d.反应达到平衡后,升高温度,平衡逆向移动,平衡常数减小
e.若使用催化剂,会改变反应的途径,但反应热不变
②某温度下,在一个容积为2L的密闭容器中进行该反应,已知此温度下的平衡常数K=50L2∙mol﹣2,反应到某时刻测得各组分的物质的量如下:
| 物质 | CO | H2 | CH3OH |
| 物质的量/(mol) | 0.4 | 0.4 | 0.8 |
请比较此时正、逆反应速率的大小:v正
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】I.碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。有机物M经过太阳光光照可转化成N,转化过程如下:
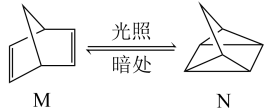 ΔH= + 88.6kJ/mol
ΔH= + 88.6kJ/mol
(1)则M、N相比,较稳定的是_______ 。
II.“金山银山不如绿水青山”,汽车尾气治理是我国一项重要的任务。经过化学工作者的努力,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。
已知:①CO的燃烧热为283kJ·mol-1
②N2(g)+O2(g) 2NO(g) ΔH= + 180.5kJ·mol-1
2NO(g) ΔH= + 180.5kJ·mol-1
③2NO(g)+O2(g) 2NO2(g) ΔH= - 116.5kJ·mol-1
2NO2(g) ΔH= - 116.5kJ·mol-1
回答下列问题:
(2)若1molN2(g)、1molO2(g)分子中化学键断裂时分别需要吸收946kJ、498kJ的能量,则1molNO(g)分子中化学键断裂时需吸收的能量为_______ kJ。
(3)为了模拟反应2NO(g)+2CO(g) N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒温恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如下表:
N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒温恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如下表:
①前3s内的平均反应速率v(N2)=_______ (保留两位小数)
②能说明上述反应达到平衡状态的是_______ 。(填正确答案标号)
A.n(CO2)=3n(N2)
B.混合气体的平均相对分子质量不变
C.气体质量不变
D.容器内混合气体的压强不变
E.2c(CO2)=3c(N2)
(4)对于气缸中NO的生成,主要由于发生了反应 N2(g)+ O2(g) 2NO(g)。化学家提出了如下反应历程:
2NO(g)。化学家提出了如下反应历程:
第一步 O2 2O 慢反应
2O 慢反应
第二步 O+N2 NO+N 较快平衡
NO+N 较快平衡
第三步 N+O2 NO+O 快速平衡
NO+O 快速平衡
下列说法错误的是_______(填标号)。
 ΔH= + 88.6kJ/mol
ΔH= + 88.6kJ/mol(1)则M、N相比,较稳定的是
II.“金山银山不如绿水青山”,汽车尾气治理是我国一项重要的任务。经过化学工作者的努力,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。
已知:①CO的燃烧热为283kJ·mol-1
②N2(g)+O2(g)
 2NO(g) ΔH= + 180.5kJ·mol-1
2NO(g) ΔH= + 180.5kJ·mol-1③2NO(g)+O2(g)
 2NO2(g) ΔH= - 116.5kJ·mol-1
2NO2(g) ΔH= - 116.5kJ·mol-1回答下列问题:
(2)若1molN2(g)、1molO2(g)分子中化学键断裂时分别需要吸收946kJ、498kJ的能量,则1molNO(g)分子中化学键断裂时需吸收的能量为
(3)为了模拟反应2NO(g)+2CO(g)
 N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒温恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如下表:
N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒温恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(10-4mol·L-1) | 10.00 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)/(10-3mol·L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
①前3s内的平均反应速率v(N2)=
②能说明上述反应达到平衡状态的是
A.n(CO2)=3n(N2)
B.混合气体的平均相对分子质量不变
C.气体质量不变
D.容器内混合气体的压强不变
E.2c(CO2)=3c(N2)
(4)对于气缸中NO的生成,主要由于发生了反应 N2(g)+ O2(g)
 2NO(g)。化学家提出了如下反应历程:
2NO(g)。化学家提出了如下反应历程:第一步 O2
 2O 慢反应
2O 慢反应第二步 O+N2
 NO+N 较快平衡
NO+N 较快平衡第三步 N+O2
 NO+O 快速平衡
NO+O 快速平衡下列说法错误的是_______(填标号)。
| A.第一步反应不从N2分解开始,因为N2比O2稳定 |
| B.N、O 原子均为该反应的催化剂 |
| C.三步反应中第一步反应活化能最大 |
| D.三步反应的速率都随温度升高而增大 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】合成氨是人工固氮比较成熟的技术,在工业上有重要的用途。
(1)已知化学键的键能如下表,则
___________ 。
(2)恒温条件下,在体积固定的容器中发生合成氨的反应,下列叙述表明反应已达平衡状态的是___________ 。
①体系压强保持不变
②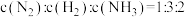
③每消耗 ,有
,有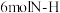 键发生断裂
键发生断裂
④混合气体的密度保持不变
⑤混合气体的平均摩尔质量保持不变
⑥
(3)合成氨反应的平衡常数与温度的对应关系如下表:
试解释平衡常数随温度的升高而减小的原因___________ 。工业上合成氨一般以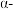 铁触媒为催化剂,
铁触媒为催化剂,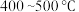 条件下反应,选取该反应温度而非室温或更高温度的原因是
条件下反应,选取该反应温度而非室温或更高温度的原因是___________ 。
(4)在恒温条件下实验室模拟合成氨反应,甲、乙两容器充入相同量的 与
与 后体积相同,甲容器保持体积不变,乙容器保持压强不变,则反应到达平衡状态时,转化率甲
后体积相同,甲容器保持体积不变,乙容器保持压强不变,则反应到达平衡状态时,转化率甲___________ 乙(填“>”、“<”或“=”)。反应达平衡后向甲容器中再充入一定量的 ,则甲容器中
,则甲容器中 的转化率
的转化率___________ (填“增大”、“减小”或“不变”)。
(5)肼 又称联氨可看成是氨气中的氢原子被氨基取代后的产物,常用作火箭的液体燃料。肼燃料电池的原理如图所示,则负极发生的电极反应式为
又称联氨可看成是氨气中的氢原子被氨基取代后的产物,常用作火箭的液体燃料。肼燃料电池的原理如图所示,则负极发生的电极反应式为___________ 。

(1)已知化学键的键能如下表,则

| 化学键 |  |  |  |  |
键能/ | 435.9 | 946.5 | 391.1 | 192.8 |
①体系压强保持不变
②
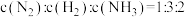
③每消耗
 ,有
,有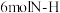 键发生断裂
键发生断裂④混合气体的密度保持不变
⑤混合气体的平均摩尔质量保持不变
⑥

(3)合成氨反应的平衡常数与温度的对应关系如下表:
温度( ) ) | 25 | 400 | 450 |
| 平衡常数 | 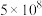 | 0.507 | 0.152 |
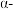 铁触媒为催化剂,
铁触媒为催化剂,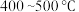 条件下反应,选取该反应温度而非室温或更高温度的原因是
条件下反应,选取该反应温度而非室温或更高温度的原因是(4)在恒温条件下实验室模拟合成氨反应,甲、乙两容器充入相同量的
 与
与 后体积相同,甲容器保持体积不变,乙容器保持压强不变,则反应到达平衡状态时,转化率甲
后体积相同,甲容器保持体积不变,乙容器保持压强不变,则反应到达平衡状态时,转化率甲 ,则甲容器中
,则甲容器中 的转化率
的转化率(5)肼
 又称联氨可看成是氨气中的氢原子被氨基取代后的产物,常用作火箭的液体燃料。肼燃料电池的原理如图所示,则负极发生的电极反应式为
又称联氨可看成是氨气中的氢原子被氨基取代后的产物,常用作火箭的液体燃料。肼燃料电池的原理如图所示,则负极发生的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】在恒容密闭容器中通入CH4与CO2,使其物质的量浓度均为1.0mol·L-1,在一定条件下发生反应:CO2(g)+CH4(g) 2CO(g)+2H2(g)。测得平衡时CH4的体积分数与温度及压强的关系如图1所示。回答下列问题:
2CO(g)+2H2(g)。测得平衡时CH4的体积分数与温度及压强的关系如图1所示。回答下列问题:

(1)该反应的ΔH__ 0。(填“<”“>”或“=”)
(2)压强p1、p2、p3由大到小的顺序为__ ;压强为p2时,b点处v正__ v逆;(填“<”“>”或“=”)
(3)a点时CH4的转化率为___ 。
(4)为探究速率与浓度的关系,根据相关实验数据,粗略地绘制出了两条速率—浓度关系曲线:v正~c(CH4)和v逆~c(CO),如图2。
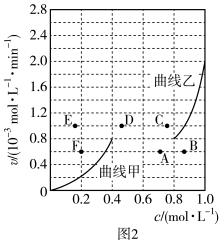
①与曲线v正~c(CH4)相对应的是图中曲线__ (填“甲”或“乙”)。
②降低温度,反应重新达到平衡时,v正、v逆相应的平衡点分别为__ (填字母)。
 2CO(g)+2H2(g)。测得平衡时CH4的体积分数与温度及压强的关系如图1所示。回答下列问题:
2CO(g)+2H2(g)。测得平衡时CH4的体积分数与温度及压强的关系如图1所示。回答下列问题:
(1)该反应的ΔH
(2)压强p1、p2、p3由大到小的顺序为
(3)a点时CH4的转化率为
(4)为探究速率与浓度的关系,根据相关实验数据,粗略地绘制出了两条速率—浓度关系曲线:v正~c(CH4)和v逆~c(CO),如图2。

①与曲线v正~c(CH4)相对应的是图中曲线
②降低温度,反应重新达到平衡时,v正、v逆相应的平衡点分别为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如图:

(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g)ΔH1=+551kJ·mol-1
反应Ⅲ:S(s)+O2(g)=SO2(g)ΔH3=-297kJ·mol-1
反应Ⅱ的化学方程式为___ ,标准状况下每有6.72L的SO2发生反应,释放的能量为___ kJ。
(2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。
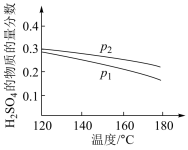
p2___ p1(填“>”或“<”),得出该结论的理由是___ 。
(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下:
i.SO2+4H++4I-=S↓+2I2+2H2O
ii.I2+2H2O+SO2=4H++4I-+SO
探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18mLSO2饱和溶液加入到2mL下列试剂中,密闭放置观察现象。
①C是A的对比实验,则a=___ 。
②设计实验B、C的目的:___ 。

(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g)ΔH1=+551kJ·mol-1
反应Ⅲ:S(s)+O2(g)=SO2(g)ΔH3=-297kJ·mol-1
反应Ⅱ的化学方程式为
(2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。

p2
(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下:
i.SO2+4H++4I-=S↓+2I2+2H2O
ii.I2+2H2O+SO2=4H++4I-+SO

探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18mLSO2饱和溶液加入到2mL下列试剂中,密闭放置观察现象。
| 序号 | A | B | C |
| 试剂组成 | 0.4mol·L-1KI | 0.2mol·L-1H2SO4 | amol·L-1KI,0.2mol·L-1 H2SO4 |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 无明显现象 | 溶液变黄,出现浑浊较A快 |
②设计实验B、C的目的:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
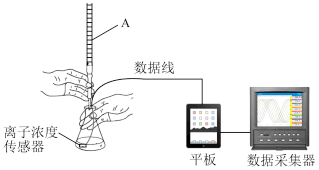
【推荐1】通过数字化手持技术,利用离子浓度传感器可直观地观察溶液中离子浓度的变化。某实验小组利用数字化手持技术探究 溶液
溶液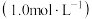 )滴定盐酸(10.00mL、
)滴定盐酸(10.00mL、 )的过程中离子浓度的变化,实验装置如图所示(夹持装置略)。
)的过程中离子浓度的变化,实验装置如图所示(夹持装置略)。
已知:常温下,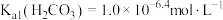 、
、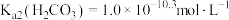 。
。
回答下列问题:
(1)仪器A的名称是_______ 。
(2)若采用常规滴定方法,用盐酸标准溶液滴定 溶液生成
溶液生成 时,采用的指示剂是
时,采用的指示剂是_______ (填“甲基橙”或“酚酞”)。
(3)滴定完成后, 标准溶液过量,数据采集器得到的
标准溶液过量,数据采集器得到的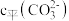 、
、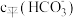 、
、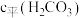 随加入
随加入 标准溶液体积的变化曲线如图所示(假设水溶液中
标准溶液体积的变化曲线如图所示(假设水溶液中 以
以 形式存在,忽略滴定过程中
形式存在,忽略滴定过程中 的逸出)。
的逸出)。
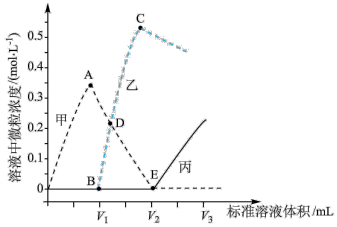
①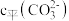 的变化曲线是
的变化曲线是_______ (填“甲”“乙”或“丙”)。
②写出BC段的离子方程式:_______ 。
③E点对应
_______ 。
④滴加的 标准液体积为
标准液体积为 时,混合液中含碳元素的主要微粒为
时,混合液中含碳元素的主要微粒为_______ 。
⑤D点对应溶液的
_______ 。
 溶液
溶液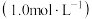 )滴定盐酸(10.00mL、
)滴定盐酸(10.00mL、 )的过程中离子浓度的变化,实验装置如图所示(夹持装置略)。
)的过程中离子浓度的变化,实验装置如图所示(夹持装置略)。
已知:常温下,
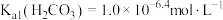 、
、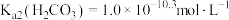 。
。回答下列问题:
(1)仪器A的名称是
(2)若采用常规滴定方法,用盐酸标准溶液滴定
 溶液生成
溶液生成 时,采用的指示剂是
时,采用的指示剂是(3)滴定完成后,
 标准溶液过量,数据采集器得到的
标准溶液过量,数据采集器得到的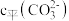 、
、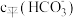 、
、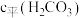 随加入
随加入 标准溶液体积的变化曲线如图所示(假设水溶液中
标准溶液体积的变化曲线如图所示(假设水溶液中 以
以 形式存在,忽略滴定过程中
形式存在,忽略滴定过程中 的逸出)。
的逸出)。
①
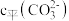 的变化曲线是
的变化曲线是②写出BC段的离子方程式:
③E点对应

④滴加的
 标准液体积为
标准液体积为 时,混合液中含碳元素的主要微粒为
时,混合液中含碳元素的主要微粒为⑤D点对应溶液的

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】I.电离平衡常数是衡量弱电解质电离程度的量,已知如表数据(25℃):
(1)25℃时,下列物质的量浓度相同的四种溶液的pH由大到小的顺序为_______ (填序号)
a.NaCN溶液 b.Na2CO3溶液 c.CH3COONa溶液 d.NaHCO3溶液
(2)25℃时,向NaClO溶液中通入少量CO2,所发生反应的化学方程式为___________ 。
(3)将相同物质的量浓度的NaClO溶液和Na2CO3溶液等体积混合,各离子浓度关系正确的是___________ (填标号)
a.c(ClO-)>c( )>c(H+) b.c(Na+)=3[c(HClO)+c(ClO-)]
)>c(H+) b.c(Na+)=3[c(HClO)+c(ClO-)]
c.c(H+)=2c( )+c(
)+c( )+c(HClO) d.c(HClO)+c(ClO-)=c(H2CO3)+c(
)+c(HClO) d.c(HClO)+c(ClO-)=c(H2CO3)+c( )
)
II.根据下列化合物:①NaOH②H2SO4③CH3COOH④NaCl⑤CH3COONa⑥(NH4)2SO4⑦CH3COONH4⑧NH4HSO4⑨NH3·H2O⑩NH4Cl,请回答下列问题:
(4)物质的量浓度相同的①NaOH②H2SO4③CH3COOH④NaCl⑤CH3COONa五种稀溶液中,水电离的OH-浓度由大到小的顺序为___________ (填序号)。
(5)物质的量浓度相同的⑥(NH4)2SO4⑦CH3COONH4⑧NH4HSO4⑨NH3·H2O⑩NH4Cl六种稀溶液中, 浓度由小到大的顺序为
浓度由小到大的顺序为___________ (填序号)。
(6)已知t℃时,Kw=1×10-13,在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b=___________ 。
III.乙二酸(H2C2O4)俗名草酸,是可溶于水的二元弱酸。
(7)利用滴定原理和装置。可以用0.0500mol·L-1酸性KMnO4溶液滴定某菠菜提取液中草酸的含量。原理为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。
①取待测菠菜提取液2mL于锥形瓶中,并将酸性KMnO4标准溶液装入___________ 中备用。
②滴定终点的判断依据是___________ 。
(8)草酸钙能对血液起抗凝作用。已知正常人体血液中Ca2+含量约为2.5×10-3mol·L-1,则理论上c( )最低为
)最低为___________ 时会生成CaC2O4沉淀。[已知Ksp(CaC2O4)=4.0×10-9]
(9)常温下,用0.200mol/LKOH溶液滴定20.00mL某未知浓度的H2C2O4溶液,滴定曲线如图所示,
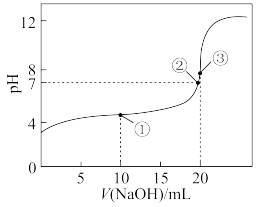
③点所示溶液中:2c( )+2c(
)+2c( )+2c(H2C2O4)=c(K+)。点①所示溶液中混合溶液中离子浓度大小关系为
)+2c(H2C2O4)=c(K+)。点①所示溶液中混合溶液中离子浓度大小关系为___________ 。
| 化学式 | CH3COOH | H2CO3 | HCN | HClO | NH3·H2O |
| 电离常数 | 1.8×10−5 | K1=4.4×10−7 K2=4.7×10−11 | 4.9×10−10 | 3.0×10−8 | 1.8×10−5 |
(1)25℃时,下列物质的量浓度相同的四种溶液的pH由大到小的顺序为
a.NaCN溶液 b.Na2CO3溶液 c.CH3COONa溶液 d.NaHCO3溶液
(2)25℃时,向NaClO溶液中通入少量CO2,所发生反应的化学方程式为
(3)将相同物质的量浓度的NaClO溶液和Na2CO3溶液等体积混合,各离子浓度关系正确的是
a.c(ClO-)>c(
 )>c(H+) b.c(Na+)=3[c(HClO)+c(ClO-)]
)>c(H+) b.c(Na+)=3[c(HClO)+c(ClO-)]c.c(H+)=2c(
 )+c(
)+c( )+c(HClO) d.c(HClO)+c(ClO-)=c(H2CO3)+c(
)+c(HClO) d.c(HClO)+c(ClO-)=c(H2CO3)+c( )
)II.根据下列化合物:①NaOH②H2SO4③CH3COOH④NaCl⑤CH3COONa⑥(NH4)2SO4⑦CH3COONH4⑧NH4HSO4⑨NH3·H2O⑩NH4Cl,请回答下列问题:
(4)物质的量浓度相同的①NaOH②H2SO4③CH3COOH④NaCl⑤CH3COONa五种稀溶液中,水电离的OH-浓度由大到小的顺序为
(5)物质的量浓度相同的⑥(NH4)2SO4⑦CH3COONH4⑧NH4HSO4⑨NH3·H2O⑩NH4Cl六种稀溶液中,
 浓度由小到大的顺序为
浓度由小到大的顺序为(6)已知t℃时,Kw=1×10-13,在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b=
III.乙二酸(H2C2O4)俗名草酸,是可溶于水的二元弱酸。
(7)利用滴定原理和装置。可以用0.0500mol·L-1酸性KMnO4溶液滴定某菠菜提取液中草酸的含量。原理为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。
①取待测菠菜提取液2mL于锥形瓶中,并将酸性KMnO4标准溶液装入
②滴定终点的判断依据是
(8)草酸钙能对血液起抗凝作用。已知正常人体血液中Ca2+含量约为2.5×10-3mol·L-1,则理论上c(
 )最低为
)最低为(9)常温下,用0.200mol/LKOH溶液滴定20.00mL某未知浓度的H2C2O4溶液,滴定曲线如图所示,

③点所示溶液中:2c(
 )+2c(
)+2c( )+2c(H2C2O4)=c(K+)。点①所示溶液中混合溶液中离子浓度大小关系为
)+2c(H2C2O4)=c(K+)。点①所示溶液中混合溶液中离子浓度大小关系为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】H2S和含硫废水(其中S元素的主要化合价是-2价)对设备、环境等会造成严重危害。已知:H2S有剧毒:常温下溶解度为1:2.6(体积)。
(1)碱法脱硫:用K2CO3溶液吸收H2S。
已知:氢硫酸和碳酸的电离常数如下表。
用过量的K2CO3溶液吸收H2S的离子方程式是_______ 。
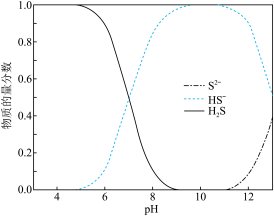
(2)H2S、HS-、S2-在水溶液中的物质的量分数随pH的分布曲线如图。当pH≈8时,含硫废水中最主要的含硫(-2价)微粒是_______ 。
(3)沉淀法处理含硫废水:向pH≈8的含硫废水中加入适量Cu2+的溶液,产生黑色沉淀且溶液的pH降低。用化学平衡移动的原理解释溶液的pH降低的原因是_______ 。
(4)氧化还原法处理含硫废水:向pH≈8的含硫废水中加入一定浓度的Na2SO3溶液,加酸将溶液调为pH=5,产生淡黄色沉淀。
①反应的离子方程式是_______ 。
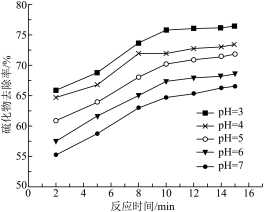
②不同pH时,硫化物去除率随时间的变化曲线如图。本工艺选择控制体系的pH=5,不选择pH<5,从环境保护的角度分析其主要原因是_______ 。
(1)碱法脱硫:用K2CO3溶液吸收H2S。
已知:氢硫酸和碳酸的电离常数如下表。
| Ka1 | Ka2 | |
| H2S | 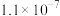 | 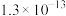 |
| H2CO3 | 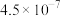 | 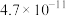 |
(2)H2S、HS-、S2-在水溶液中的物质的量分数随pH的分布曲线如图。当pH≈8时,含硫废水中最主要的含硫(-2价)微粒是

(3)沉淀法处理含硫废水:向pH≈8的含硫废水中加入适量Cu2+的溶液,产生黑色沉淀且溶液的pH降低。用化学平衡移动的原理解释溶液的pH降低的原因是
(4)氧化还原法处理含硫废水:向pH≈8的含硫废水中加入一定浓度的Na2SO3溶液,加酸将溶液调为pH=5,产生淡黄色沉淀。
①反应的离子方程式是
②不同pH时,硫化物去除率随时间的变化曲线如图。本工艺选择控制体系的pH=5,不选择pH<5,从环境保护的角度分析其主要原因是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】含氯物质在生产、生活中有重要作用。工业上常用次氯酸钠处理含有 NO 等氮氧化物的尾气,反应方程式如下:NaClO + NO + H2O — NaCl + HNO3 (未配平)。
(1)氯在元素周期表中的位置是_______ ,其所在主族的元素中,最高价氧化物对应的水化物酸性最强的是_______ (填化学式)。其所在周期的元素中,第一电离能最大的是______ (填化学式)。
(2)配平上述反应方程式_______ 。每有 0.3mol 电子发生转移,可消耗标准状况下 NO 气体的体积约为______ L。
(3)NaClO 溶液中存在如下关系:c(OH-)_____ c(HClO)(填“>”、“=”、或“<”)。
其他条件相同,随着 NaClO 溶液初始 pH(用稀硫酸调节)的不同,NO 转化率如图。
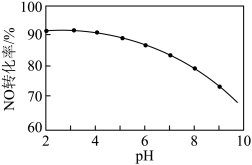
(4)NaClO 溶液的初始pH 越大,NO 的转化率越________ (填“高”或“低”),其原因是_________ 。
(5)取少量 NaClO 溶液和 KClO3 溶液,分别置于 A 试管和 B 试管,滴加试剂,观察现象,记录于下表。请将表格填写完整。
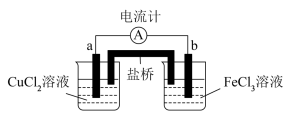
(6)某化学学习小组设计原电池装置如下图 (a 为铜电极 b 为石墨电极) :,请写出负极的电极反应式________ ;盐桥在原电池中所起的作用(任意写出一条)__________ 。
(1)氯在元素周期表中的位置是
(2)配平上述反应方程式
(3)NaClO 溶液中存在如下关系:c(OH-)
其他条件相同,随着 NaClO 溶液初始 pH(用稀硫酸调节)的不同,NO 转化率如图。

(4)NaClO 溶液的初始pH 越大,NO 的转化率越
(5)取少量 NaClO 溶液和 KClO3 溶液,分别置于 A 试管和 B 试管,滴加试剂,观察现象,记录于下表。请将表格填写完整。
| 滴加 KI 溶液 | 再滴加 CCl4,振荡、静置 | 结论 | |
| A 试管 | 溶液变为棕黄色 | 溶液分层,下层显 | 氧化性强弱:(填“>”或“<”) KClO3 |
| B 试管 | 无现象 | 溶液分层,均无色 |
(6)某化学学习小组设计原电池装置如下图 (a 为铜电极 b 为石墨电极) :,请写出负极的电极反应式

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】习近平总书记在浙江湖州市安吉县考察时提出了一个科学论断“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。请回答下列问题:
(1)硫酸工业排出的尾气(主要含 )可用软锰矿浆(
)可用软锰矿浆( )吸收,写出如图所示“反应”的化学方程式为
)吸收,写出如图所示“反应”的化学方程式为________ 。 和CO的方法之一是在汽车的排气管上装一个催化转化装置,使
和CO的方法之一是在汽车的排气管上装一个催化转化装置,使 和CO在催化剂作用下转化为无毒物质,发生反应
和CO在催化剂作用下转化为无毒物质,发生反应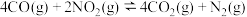 .一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和
.一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和 ,
, 的物质的量随时间的变化曲线如图所示。
的物质的量随时间的变化曲线如图所示。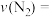
________ 。
②从11min起其他条件不变,压缩容器的容积变为1L,则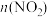 的变化曲线可能为图中的
的变化曲线可能为图中的________ (填字母)。
③恒温恒容条件下,不能说明该反应已经达到平衡状态的是________ (填标号)。
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.容器内混合气体密度保持不变
D.容器内混合气体平均相对分子质量保持不变
(3)利用反应 构成原电池的装置如图所示。此方法既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能,回答下列问题:
构成原电池的装置如图所示。此方法既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能,回答下列问题:________ (填“正极”或“负极”),发生________ (填“氧化反应”或“还原反应”),电极B上发生的电极反应为________ 。
(1)硫酸工业排出的尾气(主要含
 )可用软锰矿浆(
)可用软锰矿浆( )吸收,写出如图所示“反应”的化学方程式为
)吸收,写出如图所示“反应”的化学方程式为
 和CO的方法之一是在汽车的排气管上装一个催化转化装置,使
和CO的方法之一是在汽车的排气管上装一个催化转化装置,使 和CO在催化剂作用下转化为无毒物质,发生反应
和CO在催化剂作用下转化为无毒物质,发生反应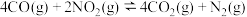 .一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和
.一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和 ,
, 的物质的量随时间的变化曲线如图所示。
的物质的量随时间的变化曲线如图所示。
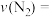
②从11min起其他条件不变,压缩容器的容积变为1L,则
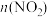 的变化曲线可能为图中的
的变化曲线可能为图中的③恒温恒容条件下,不能说明该反应已经达到平衡状态的是
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.容器内混合气体密度保持不变
D.容器内混合气体平均相对分子质量保持不变
(3)利用反应
 构成原电池的装置如图所示。此方法既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能,回答下列问题:
构成原电池的装置如图所示。此方法既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能,回答下列问题: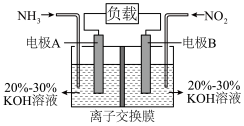
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】二甲醚(CH3OCH3)气体是一种可再生绿色新能源,被誉为“21 世纪的清洁燃料”。
(1)写出二甲醚一种同分异构体的结构简式:_______ 。
(2)已知:4.6g二甲醚气体完全燃烧生成液态水放出 145.5kJ 热量,写出其燃烧的热化学反应方程式_______ 。
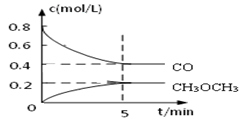
(3)工业上可用水煤气合成二甲醚:2CO(g) + 4H2(g)⇌CH3OCH3(g) + H2O(g)
①测得 CO 和 CH3OCH3(g)的浓度随时间变化如图所示,则反应开始至平衡时的 H2平均反应速率v(H2)=_______ mol/(L·min )。_______ 。
A.单位时间内生成 CO 和 H2的物质的量之比为 1﹕2
B.CH3OCH3的浓度不再变化
C.容器内压强不再变化
D.CH3OCH3 与 H2O 的物质的量相等
(4)二甲醚燃料电池工作原理如图所示_______ (填“a 电极”或“b 电极”)
②H+通过质子交换膜时的移动方向是_______ 。(填选项字母)
A.从左向右 B.从右向左
③通入 O2的电极反应式是_______ 。
(1)写出二甲醚一种同分异构体的结构简式:
(2)已知:4.6g二甲醚气体完全燃烧生成液态水放出 145.5kJ 热量,写出其燃烧的热化学反应方程式
(3)工业上可用水煤气合成二甲醚:2CO(g) + 4H2(g)⇌CH3OCH3(g) + H2O(g)
①测得 CO 和 CH3OCH3(g)的浓度随时间变化如图所示,则反应开始至平衡时的 H2平均反应速率v(H2)=
A.单位时间内生成 CO 和 H2的物质的量之比为 1﹕2
B.CH3OCH3的浓度不再变化
C.容器内压强不再变化
D.CH3OCH3 与 H2O 的物质的量相等
(4)二甲醚燃料电池工作原理如图所示
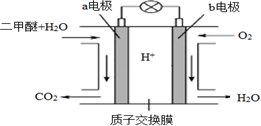
②H+通过质子交换膜时的移动方向是
A.从左向右 B.从右向左
③通入 O2的电极反应式是
您最近一年使用:0次



