一定温度下,将1molA(g)和1molB(g)充入2L密闭容器中发生反应:A(g)+B(g) xC(g)+D(s)△H<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。
xC(g)+D(s)△H<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。
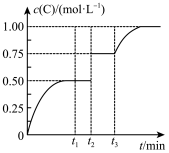
下列有关说法正确的是( )
 xC(g)+D(s)△H<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。
xC(g)+D(s)△H<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。
下列有关说法正确的是( )
| A.x=1 |
| B.t2时刻改变的条件是使用催化剂 |
| C.t3时刻改变的条件是增大反应物的浓度或压缩容器体积 |
| D.t1~t2、t2~t3平衡常数相等,且K=4 |
19-20高二上·湖南长沙·期中 查看更多[9]
湖南省长沙市湖南师范大学附属中学2019-2020学年高二上学期期中考试化学试题(已下线)第02章 化学反应的方向、限度与速率(B卷能力提升卷)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)山东省滕州市第一中2020-2021学年高二上学期10月月考化学试题辽宁省渤海大学附属高级中学2020-2021学年高二上学期期中考试化学试题河北省保定市曲阳县第一高级中学2020-2021学年高二上学期第二次月考化学试题(已下线)专题2.2.4 化学平衡图像(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)辽宁省大连市第一中学2021-2022学年高二上学期阶段性学情反馈(二)化学试题新疆生产建设兵团第十师北屯高级中学2021-2022学年高二上学期期中考试化学试题北京理工大学附属中学2023-2024学年高二上学期期中考试化学试题
更新时间:2020-08-22 10:50:54
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在一密闭容器中发生反应:2A(g)+2B(g)  2C(g)+D(g) ΔH<0,达到平衡时采取下列措施,可以使正反应速率v正增大、D的物质的量浓度c(D)增大的是
2C(g)+D(g) ΔH<0,达到平衡时采取下列措施,可以使正反应速率v正增大、D的物质的量浓度c(D)增大的是
 2C(g)+D(g) ΔH<0,达到平衡时采取下列措施,可以使正反应速率v正增大、D的物质的量浓度c(D)增大的是
2C(g)+D(g) ΔH<0,达到平衡时采取下列措施,可以使正反应速率v正增大、D的物质的量浓度c(D)增大的是| A.移走少量C | B.升高温度 |
| C.缩小容积,增大压强 | D.体积不变,充入惰性气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】利用如下实验研究Fe3+与I—的反应。
步骤1:向烧杯中加入10mL0.1mol·L-1的KI溶液,再滴加2mL0.1mol·L-1的Fe2(SO4)3溶液,振荡,把溶液分为四等份于编号为①②③④的四支试管中。
步骤2:向试管①中加入淀粉溶液,观察到溶液变蓝。
步骤3:向试管②中滴加15%KSCN溶液5~6滴,观察到溶液变红。
步骤4:向试管③、试管④中分别加入1mL2.0mol·L-1的FeSO4溶液和1mL的蒸馏水,振荡,观察到试管③中溶液颜色比试管④中溶液颜色浅。
下列说法不正确的是
步骤1:向烧杯中加入10mL0.1mol·L-1的KI溶液,再滴加2mL0.1mol·L-1的Fe2(SO4)3溶液,振荡,把溶液分为四等份于编号为①②③④的四支试管中。
步骤2:向试管①中加入淀粉溶液,观察到溶液变蓝。
步骤3:向试管②中滴加15%KSCN溶液5~6滴,观察到溶液变红。
步骤4:向试管③、试管④中分别加入1mL2.0mol·L-1的FeSO4溶液和1mL的蒸馏水,振荡,观察到试管③中溶液颜色比试管④中溶液颜色浅。
下列说法不正确的是
| A.试管①中的现象说明此条件下Fe3+的氧化性大于I2 |
| B.试管②中的现象说明Fe3+与I—的反应为可逆反应 |
| C.步骤4的现象能说明此条件下I2能将Fe2+氧化成Fe3+ |
| D.试管②中红色物质的组成为[Fe(SCN)n(H2O)6—n]3—n,此微粒中心离子的配位数为n |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列关于工业合成氨的叙述中错误的是
| A.在动力、设备、材料允许的条件下尽可能在高压下进行 |
| B.温度越高越有利于工业合成氨 |
| C.在工业合成氨中N2、H2的循环利用可提高其利用率,降低成本 |
| D.将混合气体中的氨液化有利于合成氨反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定条件下,分别向体积为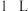 的密闭容器中充入气体,发生反应
的密闭容器中充入气体,发生反应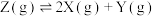 ,测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
,测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
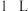 的密闭容器中充入气体,发生反应
的密闭容器中充入气体,发生反应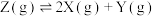 ,测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
,测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是| 实验 | 充入气体量 | 反应过程条件 |
| ① | 2molX+1molY | 恒温 |
| ② |  | 恒温 |
| ③ | 1molZ | 绝热(1) |
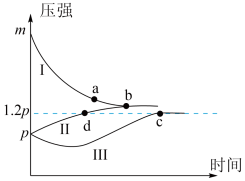
| A.曲线I对应实验①,且3m=p | B.Z的转化率:b<c |
| C.气体的总物质的量:nc<nd | D.b点平衡常数大于c点平衡常数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】密闭容器中发生反应:2X(g)+Y(s) 2Z(g) ΔH<0,达到平衡时,下列说法正确的( )
2Z(g) ΔH<0,达到平衡时,下列说法正确的( )
 2Z(g) ΔH<0,达到平衡时,下列说法正确的( )
2Z(g) ΔH<0,达到平衡时,下列说法正确的( )| A.减小容器体积,平衡正向移动 | B.再加入Z,达平衡时Z的体积分数增大 |
| C.再加入X,X的转化率减小 | D.降低温度,Y的转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列事实不能用勒夏特列原理解释的是
A.溴水中有下列平衡Br2+H2O HBr+HBrO,当加入少量硝酸银固体后,溶液颜色变浅 HBr+HBrO,当加入少量硝酸银固体后,溶液颜色变浅 |
| B.加催化剂,使N2和H2在一定条件下转化为NH3 |
| C.开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| D.实验室常用排饱和食盐水法收集Cl2 |
您最近一年使用:0次
【推荐1】—定温度下,在三个等体积的恒容密闭容器中,反应2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g)达平衡,下列说法不正确的是( )
C2H5OH(g)+3H2O(g)达平衡,下列说法不正确的是( )
 C2H5OH(g)+3H2O(g)达平衡,下列说法不正确的是( )
C2H5OH(g)+3H2O(g)达平衡,下列说法不正确的是( )| 容器 | 温度/K | 物质的起始浓度(mol·L-1) | 物质的平衡浓度(mol·L-1) | |||
CO2(g) | H2(g) | C2H5OH(g) | H2O(g) | C2H5OH(g) | ||
| 甲 | 500 | 0.20 | 0.60 | 0 | 0 | 0.08 |
| 乙 | 500 | 0.20 | 0.40 | 0 | 0 | |
| 丙 | 600 | 0 | 0 | 0.10 | 0.30 | 0.04 |
| A.该反应正反应为放热反应 |
| B.达平衡时,甲、乙容器内C2H5OH的浓度:甲>乙 |
| C.达平衡,甲、乙容器中反应所需的时间:甲<乙 |
D.达平衡时,甲、丙容器中转化率: (CO2,甲)= (CO2,甲)= (C2H5OH,丙) (C2H5OH,丙) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
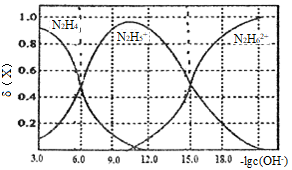
【推荐2】常温下将盐酸溶液滴加到联氨 的水溶液中,混合溶液中的微粒的物质的量分数
的水溶液中,混合溶液中的微粒的物质的量分数 随
随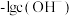 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是
 的水溶液中,混合溶液中的微粒的物质的量分数
的水溶液中,混合溶液中的微粒的物质的量分数 随
随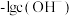 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是
A.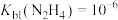 |
B.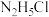 溶液中 溶液中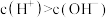 |
C.反应 的 的 |
D.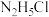 溶液中存在 溶液中存在 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】一定条件下存在反应C(s)+H2O(g) ⇌CO(g)+H2(g) ∆H>0,向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法错误的是
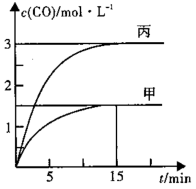
| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5 L | 0.5 L | V |
| 温度 | T1℃ | T2℃ | T1℃ |
| 起始量 | 2 molC 1mol H2O | 1 molCO 1 molH2 | 4 molC 2mol H2O |

| A.甲容器中,反应在前15min的平均速率v(H2)=0.1 mol·L-1·min-1 |
| B.丙容器的体积V<0.5L |
| C.当温度为T1℃时,反应的平衡常数K=4.5 |
| D.乙容器中,若平衡时n(H2O)=0.4mol,则T2>T1 |
您最近一年使用:0次

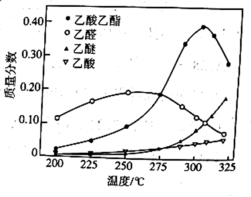
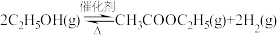 。在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是
。在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是