常温下,浓度均为 0.1 mol·L-1 的下列溶液中,粒子的物质的量浓度关系正确的是
A.氨水中,c(NH )=c(OH-)=0.1 mol·L-1 )=c(OH-)=0.1 mol·L-1 |
B.NH4Cl 溶液中,c(NH )>c(Cl-) )>c(Cl-) |
C.Na2SO4 溶液中,c(Na+)>c(SO )>c(OH-)=c(H+) )>c(OH-)=c(H+) |
D.Na2SO3 溶液中,c(Na+)=2c(SO )+c(HSO )+c(HSO )+c(H2SO3) )+c(H2SO3) |
14-15高三·广东广州·阶段练习 查看更多[22]
陕西省西安市蓝田县乡镇高中联考2023-2024学年高二上学期11月期中化学试题2023年广东省广州市高三化学冲刺训练题(二)2023年广东省广州市高三化学冲刺训练题(三)宁夏固原市第二中学2023-2024学年高二上学期期中考试化学试题第3课时 溶液中粒子浓度的大小比较(已下线)题型138 溶液中粒子浓度大小的比较(已下线)第八章 水溶液中的离子反应与平衡 第50讲 溶液中“粒子”浓度关系(已下线)【2022】【高二上】【期中考】【高中化学】59福建省福州市福建师范大学附属中学2022-2023学年高二上学期期末考试化学试题山东省枣庄市第三中学2022-2023学年高二上学期12月月考化学试题青海省西宁市湟源县第一中学2020-2021学年高二上学期期中考试化学试题四川省峨眉第二中学校2021-2022学年高二下学期5月月考化学试题天津市河北区2021-2022学年高三年级下学期总复习质量检测(一)化学试题山西省太原市第五中学2021-2022学年高二上学期12月月考化学试题(已下线)考向26 盐类的水解-备战2022年高考化学一轮复习考点微专题广东省广州市2022届高三10月调研考化学试题广东省潮州市2020-2021学年高二上学期期末考试化学试题黑龙江省肇东市第四中学校2020-2021学年高二上学期期中考试化学试题广东省广州市2021届高三年级阶段训练化学试题(已下线)2019年11月6日 《每日一题》选修4——单一溶液中粒子浓度关系判断(已下线)2018年11月7日——《每日一题》 人教 必修4-单一溶液中粒子浓度关系判断2015届广东省广州市高三综合测试(二)理综化学试卷
更新时间:2020-10-24 08:18:01
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】室温时,下列溶液中有关物质的量浓度关系不正确 的是
| A.0.1mol·L-1Na2CO3溶液中水电离出来的c(OH-)大于0.1mol·L-1NaOH溶液中水电离出来的c(OH-) |
| B.CH3COONa溶液的pH=8,则c(Na+)-c(CH3COO-)=9.9×10-7mol·L-1 |
| C.0.1mol·L-1NaHA溶液的pH=4,则有c(HA-)>c(H+)>c(H2A)>c(A2-) |
| D.纯水加热到100℃时,水的离子积变大、pH变小、呈中性 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】氯气与水的反应是一个典型的可逆反应,若该反应达到平衡后,只改变某一条件,则下列叙述正确的是( )
A.通入少量 时, 时, 减小 减小 |
B.通入少量 时,溶液的漂白性明显增强 时,溶液的漂白性明显增强 |
C.加入少量固体NaOH时,溶液中一定有c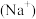 =c =c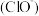 +c +c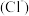 |
| D.加入少量水时溶液中水的电离平衡正向移动 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】 溶液中存在平衡:
溶液中存在平衡: (橙色)
(橙色) (黄色)
(黄色) 。在
。在 时,
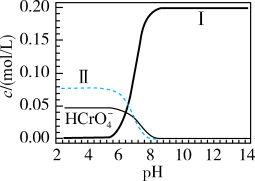
时, 溶液中含铬微粒的浓度与溶液pH的关系如图所示。下列说法
溶液中含铬微粒的浓度与溶液pH的关系如图所示。下列说法不正确 的是
 溶液中存在平衡:
溶液中存在平衡: (橙色)
(橙色) (黄色)
(黄色) 。在
。在 时,
时, 溶液中含铬微粒的浓度与溶液pH的关系如图所示。下列说法
溶液中含铬微粒的浓度与溶液pH的关系如图所示。下列说法
A.曲线Ⅱ代表 浓度 浓度 |
| B.将溶液的pH从5调至9,溶液颜色可由橙色变为黄色 |
C.溶液中存在 |
D.在 的 的 和 和 混合溶液中存在 混合溶液中存在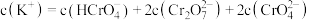 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】测定0.1
 溶液升温过程中的pH(不考虑水的蒸发),数据如下。
溶液升温过程中的pH(不考虑水的蒸发),数据如下。
下列说法正确的是

 溶液升温过程中的pH(不考虑水的蒸发),数据如下。
溶液升温过程中的pH(不考虑水的蒸发),数据如下。| 温度/℃ | 20 | 40 | 60 | 80 |
| pH | 11.80 | 11.68 | 11.54 | 11.42 |
A.温度升高, 溶液中 溶液中 降低 降低 |
B.温度升高时溶液pH降低,原因是 水解生成少量 水解生成少量 |
C. 溶液pH的变化是 溶液pH的变化是 改变与水解平衡移动共同作用的结果 改变与水解平衡移动共同作用的结果 |
D.溶液中 始终等于0.1 始终等于0.1 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
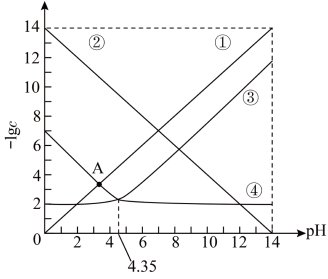
【推荐2】常温下,向一定浓度的 溶液中加适量强酸或强碱(忽略溶液体积变化),溶液中
溶液中加适量强酸或强碱(忽略溶液体积变化),溶液中 、
、 、
、 、
、 的负对数
的负对数 随溶液
随溶液 的变化关系如下图所示。下列叙述正确的是
的变化关系如下图所示。下列叙述正确的是
 溶液中加适量强酸或强碱(忽略溶液体积变化),溶液中
溶液中加适量强酸或强碱(忽略溶液体积变化),溶液中 、
、 、
、 、
、 的负对数
的负对数 随溶液
随溶液 的变化关系如下图所示。下列叙述正确的是
的变化关系如下图所示。下列叙述正确的是
A.曲线②表示 随溶液 随溶液 的变化情况 的变化情况 |
B.曲线①和曲线②的交点对应的溶液中存在 |
C.常温下,将 点对应溶液加水稀释, 点对应溶液加水稀释, 增大 增大 |
D. 电离常数 电离常数 的数量级为 的数量级为 |
您最近半年使用:0次



