 溶液中存在平衡:
溶液中存在平衡: (橙色)
(橙色) (黄色)
(黄色) 。在
。在 时,
时, 溶液中含铬微粒的浓度与溶液pH的关系如图所示。下列说法
溶液中含铬微粒的浓度与溶液pH的关系如图所示。下列说法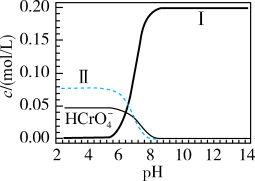
A.曲线Ⅱ代表 浓度 浓度 |
| B.将溶液的pH从5调至9,溶液颜色可由橙色变为黄色 |
C.溶液中存在 |
D.在 的 的 和 和 混合溶液中存在 混合溶液中存在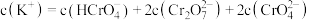 |
更新时间:2023-11-04 17:04:49
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列事实不能用勒夏特列原理解释的是
| A.加热浓氨水制取氨气 |
B.对2HI(g)  H2(g)+I2(g)平衡体系增大压强使颜色变深 H2(g)+I2(g)平衡体系增大压强使颜色变深 |
C.工业制金属钾:Na(l)+KCl(l)  NaCl(l)+K(g),选取适宜的温度,使K从反应混合物中分离出来,有利于K的生成 NaCl(l)+K(g),选取适宜的温度,使K从反应混合物中分离出来,有利于K的生成 |
| D.光照新制氯水时,溶液的颜色逐渐变浅 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法正确的是
| A.升高温度,会使单位体积内分子数增多,从而加快化学反应速率 |
B. (蓝色) (蓝色)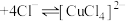 (黄色) (黄色)  , , 稀溶液受热颜色变黄 稀溶液受热颜色变黄 |
C.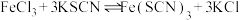 达平衡后,加入少量KCl固体,溶液红色变浅 达平衡后,加入少量KCl固体,溶液红色变浅 |
D. (橙色) (橙色) (黄色) (黄色) ,向 ,向 溶液中滴加几滴浓硫酸,溶液变为黄色 溶液中滴加几滴浓硫酸,溶液变为黄色 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】4 g Na2O2和Na2CO3的混合物溶于水,与100 mL物质的量浓度为1 mol/L 的盐酸恰好完全反应,蒸干溶液,最终得到固体的质量为
| A.5.85 g | B.8 g | C.15.5 g | D.无法计算 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】溴甲基蓝(用HBb表示)指示剂是一元弱酸,HBb为黄色,Bb-为蓝色。下列叙述正确的是
| A.0.01mol·L-1HBb溶液的pH=2 |
| B.HBb溶液的pH随温度升高而减小 |
| C.向NaOH溶液中滴加HBb指示剂,溶液显黄色 |
| D.0.01mol·L-1NaBb溶液中,c(H+)+c(Na+)=c(Bb-)+c(HBb) |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐1】25℃时,pH = 9的NaHA溶液中各微粒的物质的量浓度关系正确的是
| A.c(A2-)>c(H2A) | B.c(Na+)+c(H+) =c(OH-)+c(HA-)+2c(A2-) |
| C.c(Na+) ="c(" HA-) +c(H2A) | D.c(H+) =c(A2-) +c(OH-) |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】一定温度下,向饱和碳酸钠溶液中通入足量的CO2气体,忽略溶液体积的变化,所得溶液中有关量一定变大的是
| A.c(H+) | B.c(Na+) | C.n(H2O) | D.n( ) ) |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐3】某温度下,改变
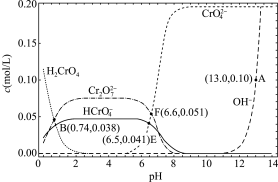
 溶液的
溶液的 时,各种含铬元素粒子及
时,各种含铬元素粒子及 浓度变化如图所示(已知
浓度变化如图所示(已知 是二元酸)。下列有关说法错误的是
是二元酸)。下列有关说法错误的是

 溶液的
溶液的 时,各种含铬元素粒子及
时,各种含铬元素粒子及 浓度变化如图所示(已知
浓度变化如图所示(已知 是二元酸)。下列有关说法错误的是
是二元酸)。下列有关说法错误的是
| A.该温度为25℃ |
B.溶液中存在平衡 ,该温度下此反应的 ,该温度下此反应的 |
C.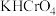 溶液中: 溶液中: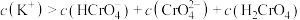 |
D.  溶液中: 溶液中: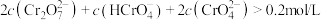 |
您最近半年使用:0次

 。若保持其他条件不变,升高温度,H2平衡浓度变小,下列说法正确的是
。若保持其他条件不变,升高温度,H2平衡浓度变小,下列说法正确的是


 溶液中滴加0.1
溶液中滴加0.1 


 和
和 浓度之和始终为0.1
浓度之和始终为0.1 

