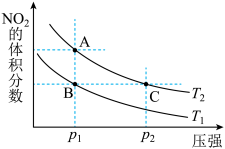
反应N2O4(g) 2NO2(g);ΔH=+57 kJ/mol在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2NO2(g);ΔH=+57 kJ/mol在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
 2NO2(g);ΔH=+57 kJ/mol在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2NO2(g);ΔH=+57 kJ/mol在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( ) 
| A.A、C两点的反应速率:A>C | B.B、C两点的反应速率:B=C |
| C.由状态B到状态A,可以用加热的方法 | D.A、C两点气体的颜色:A深,C浅 |
更新时间:2020-10-30 11:17:15
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】一定条件下,酸性KMnO4溶液与H2C2O4发生反应,Mn(Ⅱ)起催化作用,过程中不同价态含Mn粒子的浓度随时间变化如下图所示。下列说法正确的是


| A.Mn(Ⅲ)不能氧化H2C2O4 |
| B.整个滴定过程中,反应速率逐渐减小 |
| C.该条件下,Mn(Ⅱ)和Mn(Ⅶ)不能大量共存 |
D.总反应为:2MnO +5C2O +5C2O +16H+=2Mn2++10CO2↑+8H2O +16H+=2Mn2++10CO2↑+8H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某探究性学习小组认为 与KI溶液反应时,能发生以下反应:①
与KI溶液反应时,能发生以下反应:①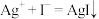
 ,②
,②
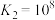 。设计如下装置进行验证,一段时间后,石墨Ⅱ电极上有光亮的物质生成。
。设计如下装置进行验证,一段时间后,石墨Ⅱ电极上有光亮的物质生成。
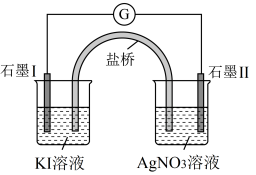
已知AgI的溶度积常数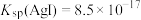 ,氧化性
,氧化性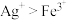 ,下列有关叙述正确的是
,下列有关叙述正确的是
 与KI溶液反应时,能发生以下反应:①
与KI溶液反应时,能发生以下反应:①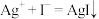
 ,②
,②
 。设计如下装置进行验证,一段时间后,石墨Ⅱ电极上有光亮的物质生成。
。设计如下装置进行验证,一段时间后,石墨Ⅱ电极上有光亮的物质生成。
已知AgI的溶度积常数
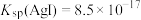 ,氧化性
,氧化性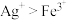 ,下列有关叙述正确的是
,下列有关叙述正确的是| A.石墨Ⅰ为正极,盐桥内溶质为KCl |
B.石墨Ⅱ的电极反应式为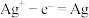 |
| C.往KI溶液中加入淀粉可检验生成的产物 |
D.平衡常数 : : ;反应活化能:①>② ;反应活化能:①>② |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列事实中,能用勒夏特列原理解释的是
| A.夏天,打开啤酒瓶时会从瓶口逸出气体 |
| B.高温及加入催化剂都能使合成氨的反应速率加快 |
| C.压缩氢气与碘蒸气的平衡混合体系,气体颜色变深 |
| D.N2(g)+3H2(g)=2NH3(g) ΔH<0,500℃左右比室温更有利于合成NH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
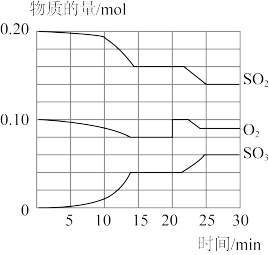
【推荐2】氨的催化氧化是硝酸工业中的重要反应: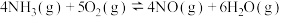
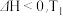 时,将
时,将 和
和 的混合气体充入
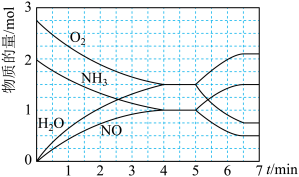
的混合气体充入 恒容密闭容器中发生上述反应,各物质的物质的量随时间变化关系如图所示:
恒容密闭容器中发生上述反应,各物质的物质的量随时间变化关系如图所示:
下列说法正确的是
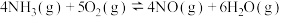
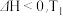 时,将
时,将 和
和 的混合气体充入
的混合气体充入 恒容密闭容器中发生上述反应,各物质的物质的量随时间变化关系如图所示:
恒容密闭容器中发生上述反应,各物质的物质的量随时间变化关系如图所示:下列说法正确的是

A. , ,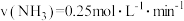 |
| B.加催化剂或缩小容积均可降低反应的活化能,提高反应速率 |
C. 时, 时,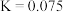 |
D. 时,改变的条件可能为降低温度 时,改变的条件可能为降低温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列对化学平衡移动的分析中,不正确的是
①已达平衡的反应C(s)+H2O(g) CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
②已达平衡的反应N2(g)+3H2(g) 2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
③2.0molPCl3和1.0molCl2充入恒容的密闭容器中,发生反应:PCl3(g)+ Cl2(g) PCl5(g)达平衡时,PCl5为0.4mol,如果此时移走1.0 molPCl3 和0.50 molCl2,在相同温度下再达平衡时PCl5的物质的量应大于0.20mol而小于0.40mol
PCl5(g)达平衡时,PCl5为0.4mol,如果此时移走1.0 molPCl3 和0.50 molCl2,在相同温度下再达平衡时PCl5的物质的量应大于0.20mol而小于0.40mol
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡不会发生移动
①已达平衡的反应C(s)+H2O(g)
 CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动②已达平衡的反应N2(g)+3H2(g)
 2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高③2.0molPCl3和1.0molCl2充入恒容的密闭容器中,发生反应:PCl3(g)+ Cl2(g)
 PCl5(g)达平衡时,PCl5为0.4mol,如果此时移走1.0 molPCl3 和0.50 molCl2,在相同温度下再达平衡时PCl5的物质的量应大于0.20mol而小于0.40mol
PCl5(g)达平衡时,PCl5为0.4mol,如果此时移走1.0 molPCl3 和0.50 molCl2,在相同温度下再达平衡时PCl5的物质的量应大于0.20mol而小于0.40mol④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡不会发生移动
| A.①④ | B.①②③ | C.②③④ | D.①②③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
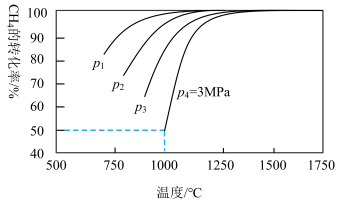
【推荐2】工业合成氨的原料气来源于化石燃料,如采用甲烷与二氧化碳反应:CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH=akJ·mol-1.在某容器中,充入等物质的量的CH4和CO2,下列说法正确的是
2CO(g)+2H2(g) ΔH=akJ·mol-1.在某容器中,充入等物质的量的CH4和CO2,下列说法正确的是
 2CO(g)+2H2(g) ΔH=akJ·mol-1.在某容器中,充入等物质的量的CH4和CO2,下列说法正确的是
2CO(g)+2H2(g) ΔH=akJ·mol-1.在某容器中,充入等物质的量的CH4和CO2,下列说法正确的是
| A.该原料气的制备反应为放热反应,a<0 |
| B.压强关系:p1>p2>p3>p4 |
| C.恒温恒压条件下,充入He,平衡逆向移动 |
| D.1000℃时的压强平衡常数Kp=4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】氮是生命的基础,氮及其化合物在生产生活中具有广泛应用。工业上用氨的催化氧化生产硝酸,其热化学方程式为4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=-904kJ•mol-1。生产硝酸的尾气中主要含有NO、NO2等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO3)2、Ca(NO2)2等化工产品。对于反应4NH3(g)+5O2(g)
4NO(g)+6H2O(g) △H=-904kJ•mol-1。生产硝酸的尾气中主要含有NO、NO2等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO3)2、Ca(NO2)2等化工产品。对于反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列有关说法正确的是
4NO(g)+6H2O(g),下列有关说法正确的是
 4NO(g)+6H2O(g) △H=-904kJ•mol-1。生产硝酸的尾气中主要含有NO、NO2等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO3)2、Ca(NO2)2等化工产品。对于反应4NH3(g)+5O2(g)
4NO(g)+6H2O(g) △H=-904kJ•mol-1。生产硝酸的尾气中主要含有NO、NO2等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO3)2、Ca(NO2)2等化工产品。对于反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列有关说法正确的是
4NO(g)+6H2O(g),下列有关说法正确的是| A.该反应只有在高温条件下能自发进行 |
| B.该反应的正反应的活化能小于逆反应的活化能 |
| C.达到平衡时,升高温度,v(正)减小、v(逆)增加 |
| D.c(NH3):c(O2):c(NO):c(H2O)=4:5:4:6时,说明反应达到平衡 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】乙酸甲酯催化醇解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式为: CH3COOCH3(l) +C6H13OH (l) 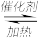 CH3COOC6H13(l) +CH3OH(l)
CH3COOC6H13(l) +CH3OH(l)
反应开始时,己醇和乙酸甲酯按物质的量之比 1:1 投料,测得 348 K、343 K 两个温度 下乙酸甲酯转化率(α)随时间(t)的变化关系如下图所示:
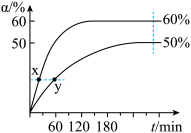
下列说法不正确的是
 CH3COOC6H13(l) +CH3OH(l)
CH3COOC6H13(l) +CH3OH(l)反应开始时,己醇和乙酸甲酯按物质的量之比 1:1 投料,测得 348 K、343 K 两个温度 下乙酸甲酯转化率(α)随时间(t)的变化关系如下图所示:

下列说法不正确的是
| A.该醇解反应的ΔH > 0 |
| B.反应速率:v(x)> v(y) |
| C.343K时,以物质的量分数表示的化学平衡常数 Kx=2.25 |
D.348K时,初始投料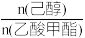 分别按 1:1和2:1进行,Kx 相同 分别按 1:1和2:1进行,Kx 相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】NO和O2混合后可发生反应:①2NO(g)+O2(g)=2NO2(g),②2NO2(g)⇌N2O4(g)反应体系中含氮物质的物质的量浓度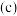 随着时间
随着时间 的变化曲线如图。下列说法正确的是
的变化曲线如图。下列说法正确的是
 随着时间
随着时间 的变化曲线如图。下列说法正确的是
的变化曲线如图。下列说法正确的是
A.c为c(NO2)随 的变化曲线 的变化曲线 |
B. 时,反应①达到化学平衡状态 时,反应①达到化学平衡状态 |
C. 时,c(NO)+c(NO2)+c(N2O4)=c0 时,c(NO)+c(NO2)+c(N2O4)=c0 |
D. 后,NO2的消耗速率等于生成速率 后,NO2的消耗速率等于生成速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】合成氨反应N2+3H2=2NH3,初始时氮气、氢气的体积比为1:3,在相同催化剂条件下平衡混合物中氨的体积分数φ(NH3)与温度、压强的关系如图所示;下列说法正确的是
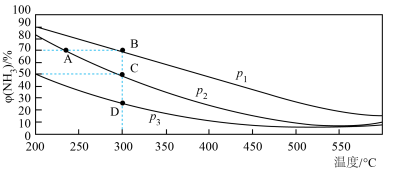

| A.图像中P1<P2<P3 |
| B.A、B、C、D的平衡常数大小关系A=B>C>D |
C.反应速率 逆(状态A)> 逆(状态A)> 逆(状态B) 逆(状态B) |
| D.在C点时,N2的转化率约为67% |
您最近一年使用:0次

 和
和 (
( )。反应过程中
)。反应过程中 物质的量变化如图所示。下列说法不正确的是
物质的量变化如图所示。下列说法不正确的是