氮是生命的基础,氮及其化合物在生产生活中具有广泛应用。工业上用氨的催化氧化生产硝酸,其热化学方程式为4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=-904kJ•mol-1。生产硝酸的尾气中主要含有NO、NO2等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO3)2、Ca(NO2)2等化工产品。对于反应4NH3(g)+5O2(g)
4NO(g)+6H2O(g) △H=-904kJ•mol-1。生产硝酸的尾气中主要含有NO、NO2等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO3)2、Ca(NO2)2等化工产品。对于反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列有关说法正确的是
4NO(g)+6H2O(g),下列有关说法正确的是
 4NO(g)+6H2O(g) △H=-904kJ•mol-1。生产硝酸的尾气中主要含有NO、NO2等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO3)2、Ca(NO2)2等化工产品。对于反应4NH3(g)+5O2(g)
4NO(g)+6H2O(g) △H=-904kJ•mol-1。生产硝酸的尾气中主要含有NO、NO2等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO3)2、Ca(NO2)2等化工产品。对于反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列有关说法正确的是
4NO(g)+6H2O(g),下列有关说法正确的是| A.该反应只有在高温条件下能自发进行 |
| B.该反应的正反应的活化能小于逆反应的活化能 |
| C.达到平衡时,升高温度,v(正)减小、v(逆)增加 |
| D.c(NH3):c(O2):c(NO):c(H2O)=4:5:4:6时,说明反应达到平衡 |
更新时间:2022-12-08 20:15:08
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】一定温度下,有可逆反应:3Fe(s)+4H2O(g)Fe3O4(s)+4H2O;△H>O。下列说法中正确的是


| A.降低反应温度,H2O(g)的转化率增大 |
| B.反应达到平衡后,增加Fe的量,平衡向正反应方向移动 |
| C.反应达到平衡后,t0时增大压强,V(正)、V(逆)的变化如右图所示 |
| D.在绝热密闭容器中,若体系温度不再发生变化,则说明该反应达到化学平衡 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】可逆反应3H2+N2 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是
 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是| A.v正(N2)=v正(H2) |
| B.v正(N2)=v逆(NH3) |
| C.2v正(H2)=3v逆(NH3) |
| D.v正(N2)=3v逆(H2) |
您最近一年使用:0次
【推荐3】一定条件下,向容积为1.00L的密闭容器中通入一定量的N2O4和NO2的混合气体,发生反应:N2O4(g)⇌2NO2(g) ∆H>0,体系中各物质浓度随时间变化如图所示。下列有关说法正确的是
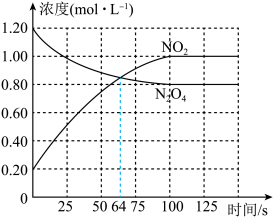
| A.64s时,反应达到化学平衡状态 |
| B.该条件下,此反应的化学平衡常数K=0.8 |
| C.当容器内气体的颜色不再发生变化时,该反应达到化学平衡状态 |
| D.若该容器与外界无热传递,则反应达到平衡前容器内气体的温度逐升高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】在一定温度下的可逆反应
 ,
,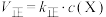 ,
, ,若该温度下的平衡常数
,若该温度下的平衡常数 ,下列说法错误的是
,下列说法错误的是

 ,
,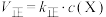 ,
, ,若该温度下的平衡常数
,若该温度下的平衡常数 ,下列说法错误的是
,下列说法错误的是A.该温度下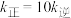 |
B.升高温度, 增大的倍数大于 增大的倍数大于 增大的倍数 增大的倍数 |
| C.有利于测定X的相对分子质量的条件为高温低压 |
D.恒压条件下,向平衡体系中充入惰性气体 ,X的转化率增大 ,X的转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实中,不能用勒夏特列原理解释的是
| A.压缩氢气与碘蒸气反应的平衡混合气体,颜色变深 |
| B.浓氨水中加入氢氧化钠固体时产生较多的刺激性气味的气体 |
| C.往FeCl3溶液中滴加少量KSCN溶液,溶液呈红色,再加入铁粉,溶液红色变浅 |
| D.将盛有二氧化氮和四氧化二氮混合气体的密闭容器置于冷水中,混合气体的颜色变浅 |
您最近一年使用:0次
【推荐1】下列根据实验操作和现象得出的结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向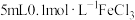 溶液中加入 溶液中加入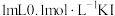 溶液,充分反应后,滴入 溶液,充分反应后,滴入 溶液,溶液变红 溶液,溶液变红 |  与 与 发生的反应为可逆反应 发生的反应为可逆反应 |
| B | 将铁钉置于盛有稀醋酸的试管中,长时间放置,暴露在空气中的铁钉表面出现大量锈迹 | 铁钉只发生析氢腐蚀 |
| C | 将浓硫酸与灼热的木炭反应产生的气体依次通过品红溶液、饱和 溶液、澄清石灰水,观察到品红溶液褪色,石灰水变浑浊 溶液、澄清石灰水,观察到品红溶液褪色,石灰水变浑浊 | 浓硫酸与木炭反应生成了 和 和 |
| D | 用注射器吸入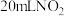 和 和 的混合气体,将细管端用橡胶塞封闭。迅速向外拉活塞,观察到气体颜色先变浅后变深(最终颜色比拉动活塞前要浅) 的混合气体,将细管端用橡胶塞封闭。迅速向外拉活塞,观察到气体颜色先变浅后变深(最终颜色比拉动活塞前要浅) | 减小压强时该平衡向着生成 的方向移动 的方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某密闭带活塞的容器中,反应达到平衡A(g)+2B(g) 3C(?),测得C(A)=0.6mol/L,将容积体积缩小为原来的一半并重新达到平衡,测得C(A)=1.0mol/L,下列说法正确的是
3C(?),测得C(A)=0.6mol/L,将容积体积缩小为原来的一半并重新达到平衡,测得C(A)=1.0mol/L,下列说法正确的是
 3C(?),测得C(A)=0.6mol/L,将容积体积缩小为原来的一半并重新达到平衡,测得C(A)=1.0mol/L,下列说法正确的是
3C(?),测得C(A)=0.6mol/L,将容积体积缩小为原来的一半并重新达到平衡,测得C(A)=1.0mol/L,下列说法正确的是| A.建立新平衡时,原平衡不移动 | B.建立新平衡时,原平衡向左移动 |
| C.C为非气体物质,加压时平衡向右移动 | D.C为气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】合成氨工业中原料气进入合成塔前需经过铜氨溶液“净化”,除去其中的CO,原理为
 。下列说法正确的是
。下列说法正确的是

 。下列说法正确的是
。下列说法正确的是| A.该反应在任何温度下均能自发进行 | B.降低温度有利于吸收CO |
| C.增大压强有利于铜氨溶液再生 | D.为节约成本,原料气可以不进行净化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】蓝天保卫战——持续三年的大气治理之战,其中低成本、高效率处理SO2、NO2等大气污染物一直是化学研究的重点课题,研究它们的性质、制备在工业生产和环境保护中有着重要意义。一种处理SO2、NO2的研究成果,其反应原理为SO2(g)+NO2(g)⇌SO3(g)+NO(g) ΔH=-41.8kJ·mol-1。标准状况下,SO2(g)+NO2(g)=SO3(s)+NO(g) ΔH,下列有关说法不正确的是
| A.该反应ΔH<0,ΔS<0 |
| B.升高温度,能增加SO2的反应速率和转化率 |
| C.SO2的生成速率和NO2的消耗速率相等说明该反应达到平衡状态 |
| D.标准状况下,该反应中每生成22.4LNO转移电子的数目约等于2×6.02×1023 |
您最近一年使用:0次

 ,
, 时,反应自发进行,如金属钠和水的反应
时,反应自发进行,如金属钠和水的反应

