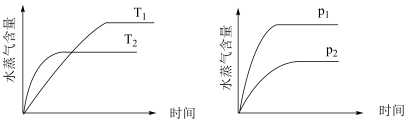
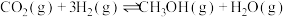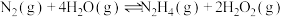在容积固定的密闭容器中,发生反应N2(g)+3H2(g)⇌2NH3(g)+Q(Q>0),改变条件,其平衡移动方向正确的是
| A.增大压强,往正反应方向移动 | B.加入催化剂,往正反应方向移动 |
| C.升高温度,往正反应方向移动 | D.移走氮气,往正方向方向移动 |
18-19高二上·上海奉贤·期中 查看更多[4]
(已下线)第二章 化学反应速率与化学平衡(A卷·知识通关练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)(已下线)2.2.3 影响化学平衡的因素(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)吉林省长春市清蒲中学2020-2021学年度高二上学期期末化学试题上海市奉城高级中学2018-20219学年高二上学期期中考试化学试题
更新时间:2020-12-22 17:00:41
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】可逆反应CO(g)+H2O(g) CO2(g)+H2(g),达到限度后,欲提高一氧化碳的转化率,可以采取的措施为( )
CO2(g)+H2(g),达到限度后,欲提高一氧化碳的转化率,可以采取的措施为( )
 CO2(g)+H2(g),达到限度后,欲提高一氧化碳的转化率,可以采取的措施为( )
CO2(g)+H2(g),达到限度后,欲提高一氧化碳的转化率,可以采取的措施为( )| A.使用催化剂 | B.增大压强 |
| C.增大一氧化碳的浓度 | D.增大水蒸气的浓度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】对于反应2SO2(g)+O2(g) 2SO3(g)△H<0已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图象不相符的是
2SO3(g)△H<0已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图象不相符的是
(t1时刻v正=v逆;t1时改变条件,t2时重新建立平衡)
 2SO3(g)△H<0已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图象不相符的是
2SO3(g)△H<0已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图象不相符的是(t1时刻v正=v逆;t1时改变条件,t2时重新建立平衡)
A.加入催化剂 |
B.增加SO3浓度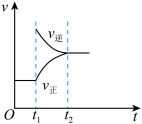 |
C.升高温度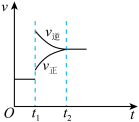 |
D.增大压强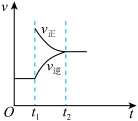 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g) +H2O(g) CO2(g)+H2(g) K=1,反应前CO的物质的量为4mol,平衡后CO的物质的量为2mol。下列说法正确的是
CO2(g)+H2(g) K=1,反应前CO的物质的量为4mol,平衡后CO的物质的量为2mol。下列说法正确的是
 CO2(g)+H2(g) K=1,反应前CO的物质的量为4mol,平衡后CO的物质的量为2mol。下列说法正确的是
CO2(g)+H2(g) K=1,反应前CO的物质的量为4mol,平衡后CO的物质的量为2mol。下列说法正确的是| A.升高温度,H2O浓度增大,表明正反应是吸热反应 |
| B.通入CO后,正反应速率逐渐大 |
| C.反应前H2O物质的量为2mol |
| D.CO的平衡转化率为50% |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】由N2O和NO反应生成N2和NO2的能量变化如图所示。下列说法不正确的是


| A.反应生成1molN2时转移2mole- |
| B.其他条件不变,降温可以提高NO的平衡转化率 |
| C.N2O(g)+NO(g)═N2(g)+NO2(g)△H=+139kJ•mol-1 |
| D.反应物断键吸收能量总和小于生成物成键释放能量总和 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】向体积为10 L的恒容密闭容器中通入1.1 mol CH4(g)和1.1 mol H2O(g)制备H2,反应原理为CH4(g) + H2O(g) CO(g) + 3H2(g) ΔH = + 206.2 kJ·mol-1。在不同温度(Ta、Tb)下测得容器中n(CO) 随时间的变化曲线如图所示:
CO(g) + 3H2(g) ΔH = + 206.2 kJ·mol-1。在不同温度(Ta、Tb)下测得容器中n(CO) 随时间的变化曲线如图所示:

下列说法正确的是
 CO(g) + 3H2(g) ΔH = + 206.2 kJ·mol-1。在不同温度(Ta、Tb)下测得容器中n(CO) 随时间的变化曲线如图所示:
CO(g) + 3H2(g) ΔH = + 206.2 kJ·mol-1。在不同温度(Ta、Tb)下测得容器中n(CO) 随时间的变化曲线如图所示: 
下列说法正确的是
| A.温度Ta<Tb |
| B.Ta时,0 ~ 4 min内υ(CH4) = 0.25mol·L-1·min-1 |
| C.Tb时,若改为恒温恒压容器,平衡时n(CO) > 0.6 mol |
| D.Tb时,平衡时再充入1.1 mol CH4,平衡常数增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列事实不能用勒夏特列原理解释的是
| A.开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| B.久置的氯水漂白能力降低 |
| C.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
D.2HI H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】对于反应:  (g)+ I2(g)
(g)+ I2(g) 
 (g)+2HI(g) △H>0.达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有
(g)+2HI(g) △H>0.达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有
 (g)+ I2(g)
(g)+ I2(g) 
 (g)+2HI(g) △H>0.达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有
(g)+2HI(g) △H>0.达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有| A.恒压条件下通入惰性气体 | B.降低温度 |
| C.增大环戊烯浓度 | D.将容器体积减小到原来的一半 |
您最近一年使用:0次