关于小苏打水溶液的表述正确的是( )
A.溶液中HCO 存在电离平衡:HCO 存在电离平衡:HCO +H2O⇌H2CO3+OH- +H2O⇌H2CO3+OH- |
B.c(Na+)+c(H+)=c(HCO )+c(CO )+c(CO )+c(OH- ) )+c(OH- ) |
| C.由于溶液显碱性,说明HCO3-的水解程度大于HCO3-的电离程度 |
D.c(Na+)=c(HCO )+c(CO )+c(CO )+c(H2CO3) )+c(H2CO3) |
更新时间:2021-01-04 21:27:18
|
相似题推荐
多选题
|
较易
(0.85)
【推荐1】84消毒液(主要成分是次氯酸钠)是家庭常用的消毒剂。以下有关说法正确的是
| A.次氯酸钠水解的溶液呈酸性,说明次氯酸是弱酸 |
| B.次氯酸钠水溶液具有很强的漂白性,说明其水溶液中存在次氯酸 |
| C.84消毒液杀菌消毒的原理是放出原子态氧杀死细菌 |
| D.二氧化硫具有漂白性,若将二氧化硫通入84消毒液中,其漂白能力增强 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐2】下列说法正确的是
| A.一定温度下,反应MgCl2(1)=Mg(1)+ Cl2(g)的 △H>0 △S>0 |
| B.灼烧海带样品时,坩埚应该垫在石棉网上加热 |
| C.纸层析实验中,须将滤纸上的试样点浸入展开剂中 |
| D.常温下pH= 6的酸性溶液中,可能存在NH3·H2O分子 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐1】常温下,某 的一元酸
的一元酸 溶液中,
溶液中, 的电离百分数为
的电离百分数为 ,某0.1
,某0.1 的一元碱
的一元碱 溶液中
溶液中 与
与 之比为
之比为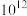 。将上述两种溶液等体积混合后,溶液显酸性,若混合时体积变化忽略不计,下列推论错误的是
。将上述两种溶液等体积混合后,溶液显酸性,若混合时体积变化忽略不计,下列推论错误的是
 的一元酸
的一元酸 溶液中,
溶液中, 的电离百分数为
的电离百分数为 ,某0.1
,某0.1 的一元碱
的一元碱 溶液中
溶液中 与
与 之比为
之比为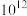 。将上述两种溶液等体积混合后,溶液显酸性,若混合时体积变化忽略不计,下列推论错误的是
。将上述两种溶液等体积混合后,溶液显酸性,若混合时体积变化忽略不计,下列推论错误的是A. 是一元强碱 是一元强碱 |
B.混合后, 的电离百分数大于a% 的电离百分数大于a% |
C.混合溶液中 小于 小于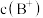 |
D. 与 与 之比值,原 之比值,原 溶液小于混合溶液 溶液小于混合溶液 |
您最近一年使用:0次
多选题
|
较易
(0.85)
解题方法
【推荐2】常温下,将等浓度的NaOH溶液分别滴加到等pH、等体积的HA、HB两种弱酸溶液中,溶液的pH与粒子浓度比值的对数关系如图所示。下列叙述错误的是
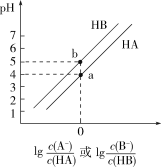

| A.酸性:HA<HB |
| B.a点时,溶液中由水电离出的c(OH-)约为1×10−10 mol∙L−1 |
| C.向HB溶液中滴加NaOH溶液至pH=7时:c(B-)>c(HB) |
| D.b点时,c(Na+)>c(B-)=c(HB)>c(H+)>c(OH-) |
您最近一年使用:0次
多选题
|
较易
(0.85)
解题方法
【推荐1】苹果酸(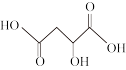 )是应用广泛的植物酸味剂,某同学利用电位滴定法滴加0.18 mol∙L−1的NaOH溶液以测定5.60mL苹果酸溶液中的苹果酸浓度。电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位(ERC)也产生了突跃,进而确定滴定终点的位置。滴定时电位滴定曲线如图所示。下列说法正确的是
)是应用广泛的植物酸味剂,某同学利用电位滴定法滴加0.18 mol∙L−1的NaOH溶液以测定5.60mL苹果酸溶液中的苹果酸浓度。电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位(ERC)也产生了突跃,进而确定滴定终点的位置。滴定时电位滴定曲线如图所示。下列说法正确的是
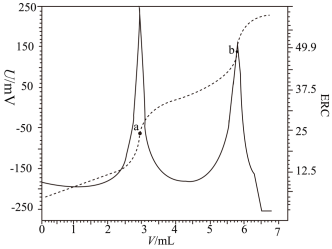
(注:——表示电极电位曲线图;……表示电极电压曲线图)
 )是应用广泛的植物酸味剂,某同学利用电位滴定法滴加0.18 mol∙L−1的NaOH溶液以测定5.60mL苹果酸溶液中的苹果酸浓度。电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位(ERC)也产生了突跃,进而确定滴定终点的位置。滴定时电位滴定曲线如图所示。下列说法正确的是
)是应用广泛的植物酸味剂,某同学利用电位滴定法滴加0.18 mol∙L−1的NaOH溶液以测定5.60mL苹果酸溶液中的苹果酸浓度。电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位(ERC)也产生了突跃,进而确定滴定终点的位置。滴定时电位滴定曲线如图所示。下列说法正确的是
(注:——表示电极电位曲线图;……表示电极电压曲线图)
| A.该滴定过程中需加入甲基橙作指示剂 |
| B.b点溶液中c(H+)<c(OH-) |
| C.原苹果酸溶液中c(C4H6O5)≈0.36 mol∙L−1 |
D.a点溶液中存在:c(OH-)+c(C4H6O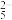 )=c(C4H6O5)+c(H+) )=c(C4H6O5)+c(H+) |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
【推荐2】用物质的量都是0.1 mol的CH3COOH和CH3COONa配成1L混合溶液,已知其中c(CH3COO-)大于c(Na+),对该混合溶液的下列判断正确的是 ( )
| A.c(H+)>c(OH-) |
| B.c(CH3COO-)+c(CH3COOH)=0.2 mol·L-1 |
| C.c(CH3COOH)>c(CH3COO-) |
| D.c(CH3COO-)+c(OH-)=0.1 mol·L-1 |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
解题方法
【推荐3】室温下,将0.1 mol·L-1 AgNO3溶液和0.1 mol·L-1 NaCl溶液等体积充分混合,一段时间后过滤,得滤液a和沉淀b。取等量的滤液a于两支试管中,分别滴加相同体积、浓度均为0.1 mol·L-1的Na2S溶液和Na2SO4溶液,前者出现浑浊,后者溶液仍澄清;再取少量的沉淀b,滴加几滴氨水,沉淀逐渐溶解。下列说法正确的是
| A.从实验现象可以得出该温度下:Ksp(Ag2S)<Ksp( Ag2SO4) |
| B.0.1 mol·L-1 Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S) |
| C.沉淀b中滴加氨水发生反应的离子方程式:AgCl+2NH3·H2O=[Ag(NH3)2]++Cl-+2H2O |
D.过滤后所得清液中一定存在:c(Ag+)= 且c(Ag+)> 且c(Ag+)> |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列叙述中一定正确的是
| A.0.1 mol/L的CH3COOH溶液中,由水电离出的c(H+)为10-13 mol/L |
| B.pH=2与pH=1的CH3COOH溶液中c(H+)之比为1︰10 |
| C.仅含有Na+、H+、OH-、CH3COO-四种离子的某溶液中可能存在: c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.1.0 mol/LNa2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
【推荐2】下列说法不正确的是
A. 的 的 溶液中,水电离产生的 溶液中,水电离产生的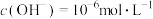 |
B. 的 的 和 和 混合溶液中, 混合溶液中, |
C. 的 的 溶液中, 溶液中,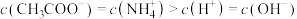 |
D. 的 的 溶液中,水电离产生的 溶液中,水电离产生的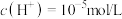 |
您最近一年使用:0次
多选题
|
较易
(0.85)
解题方法
【推荐3】下列说法正确的是
| A.0.1mol·L−1 NH3·H2O中:c(OH-)>c(NH4+)>c(NH3·H2O)>c(H+) |
| B.0.1mol·L−1 NaHSO3溶液(室温下pH<7)中:c(SO32-)<c(H2SO3) |
| C.浓度均为0.1mol·L−1 的Na2CO3和NaHCO3混合溶液中:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
| D.0.1mol·L−1 (NH4)2CO3溶液中:c(NH4+)+c(NH3·H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) |
您最近一年使用:0次

 水解平衡的影响,实验方案如下:配制
水解平衡的影响,实验方案如下:配制 溶液、50mL对照组溶液x,向两种溶液中分别滴加1滴
溶液、50mL对照组溶液x,向两种溶液中分别滴加1滴 HCl溶液、1滴
HCl溶液、1滴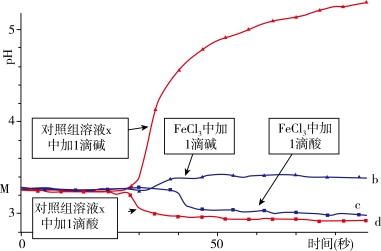
 发生了水解反应
发生了水解反应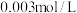 KCl
KCl 水解平衡发生了移动
水解平衡发生了移动

