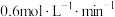下列说法正确的是
| A.合成氨反应选择在400~500℃进行的重要原因是该温度下反应物的转化率最大 |
| B.△H<0,△S>0的反应都是自发反应,△H>0,△S>0的反应任何条件都是非自发反应 |
| C.已知:P4(g)+6Cl2(g)=4PCl3(g) △H= akJ·mol-1 P4(g)+10Cl2(g)=4PCl5(g) △H=bkJ·mol-1 P4具有正四面体结构,PCl5中P-Cl键的键能为 ckJ·mol-1,PCl3中P-Cl键的键能为1.2c kJ·mol-1,由此计算Cl-Cl键的键能为(b -a+5.6c)/4kJ·mol-1 |
| D.在一定温度下,固定体积为2L密闭容器中,发生反应:2SO2(g)+O2(g)⇌ 2SO3(g) △H<0,当2v (O2)= v (SO3)时,说明该反应已达到平衡状态 |
更新时间:2021-02-04 19:56:49
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】反应N2(气)+O2(气)=2NO(气)的能量变化如图所示。已知:断开1molN2(气)中化学键需吸收946kJ能量,断开1molO2(气)中化学键需吸收498kJ能量。下列正确的是
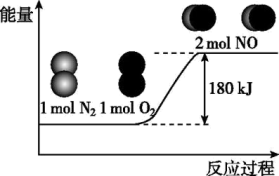

| A.氮气跟氧气反应生成NO(气)释放能量 |
| B.2molN原子结合成N2时吸946kJ能量 |
| C.断开1molNO(气)中的化学键可释放90kJ能量 |
| D.反应N2(气)+O2(气)=2NO(液)吸收的热量小于180kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】科学家已获得了气态 分子,其空间结构为正四面体形(如图所示)。已知断裂
分子,其空间结构为正四面体形(如图所示)。已知断裂 键吸收
键吸收 能量,断裂
能量,断裂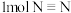 键吸收
键吸收 能量。下列说法错误的是
能量。下列说法错误的是
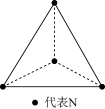
 分子,其空间结构为正四面体形(如图所示)。已知断裂
分子,其空间结构为正四面体形(如图所示)。已知断裂 键吸收
键吸收 能量,断裂
能量,断裂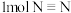 键吸收
键吸收 能量。下列说法错误的是
能量。下列说法错误的是
A. 中只含有非极性共价键 中只含有非极性共价键 |
B. 分子与 分子与 分子相比,后者更稳定 分子相比,后者更稳定 |
C. 的过程中吸收 的过程中吸收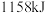 能量 能量 |
D.以 为原料替代 为原料替代 合成等量 合成等量 时,放出的热量减少 时,放出的热量减少 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】实验室配制碘水时,通常将 溶于KI溶液:
溶于KI溶液: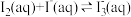 。关于该溶液,下列说法正确的是
。关于该溶液,下列说法正确的是
 溶于KI溶液:
溶于KI溶液: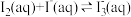 。关于该溶液,下列说法正确的是
。关于该溶液,下列说法正确的是A.KI的电子式: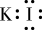 | B.滴入淀粉溶液,不变蓝 |
| C.加水稀释,平衡逆向移动 | D.加少量 固体平衡正向移动 固体平衡正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】
 。下列分析
。下列分析不正确 的是

 。下列分析
。下列分析A.氮分子的 键能大,断开该键需要较多能量 键能大,断开该键需要较多能量 |
| B.增大合成氨的反应速率与提高平衡混合物中氨的含量所采取的措施均一致 |
C.平衡混合物中 的沸点最高,液化、分离出 的沸点最高,液化、分离出 能提高其产率 能提高其产率 |
D.断裂1  和3 和3  的共价键所需能量小于断裂2 的共价键所需能量小于断裂2  的共价键所需能量 的共价键所需能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在恒温、体积为2L的密闭容器中加入1mol 和3mol
和3mol ,发生反应:
,发生反应: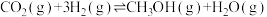
 。下列可认定该可逆反应已达到化学平衡状态的是
。下列可认定该可逆反应已达到化学平衡状态的是
 和3mol
和3mol ,发生反应:
,发生反应: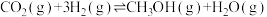
 。下列可认定该可逆反应已达到化学平衡状态的是
。下列可认定该可逆反应已达到化学平衡状态的是A. |
| B.容器内混合气体平均相对分子质量保持不变 |
C.容器中 、 、 、 、 、 、 的物质的量之比为1∶3∶1∶1 的物质的量之比为1∶3∶1∶1 |
| D.反应中每形成2mol H-O键,同时断裂3mol H-H键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】T0时,向容积为5L的恒容密闭容器中充入一定量的A(g)和B(g),发生反应: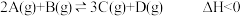 。测得反应过程中的部分数据如表所示,下列说法错误的是
。测得反应过程中的部分数据如表所示,下列说法错误的是
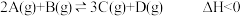 。测得反应过程中的部分数据如表所示,下列说法错误的是
。测得反应过程中的部分数据如表所示,下列说法错误的是| t/min | n(A)/mol | n(B)/mol |
| 0 | 4.0 | 2.0 |
| 5 | 2.0 | 1.0 |
| 10 | 2.0 | 1.0 |
| A.其他条件不变,温度变为T1时,平衡时测得C的浓度为0.8mol/L,则T1>T0 |
| B.8min时,该反应的v(正)=v(逆) |
| C.5min时,该反应达到平衡状态,且A、B的转化率相等 |
| D.平衡时,C的体积分数约为42.9% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是( )
| A.自发反应在任何条件下都能实现 |
| B.所有的自发反应都是放热的 |
| C.升高温度,活化分子百分数增大,化学反应速率一定增大 |
| D.一般使用催化剂可以降低反应的活化能,增大活化分子百分数,从而提高反应物的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列推论正确的是( )
| A.S(g)+O2(g)=SO2(g) △H1,S(s)+O2(g)=SO2(g) △H2;则:△H1>△H2 |
B.石墨燃烧热为393.5kJ·mol-1,则有C(s)+ O2(g)=CO(g) △H=-393.5kJ·mol-1 O2(g)=CO(g) △H=-393.5kJ·mol-1 |
| C.中和热为57.4kJ/mol,则有Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l) △H<-114.8kJ/mol |
| D.CaCO3(s)=CaO(s)+CO2(g) △H>0,则:该反应任何温度下都能自发进行 |
您最近一年使用:0次



 2 SO3为放热反应
2 SO3为放热反应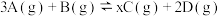 ,2 min末该反应达到平衡,生成0.8 mol D,并测定C的浓度为0.2mol·L
,2 min末该反应达到平衡,生成0.8 mol D,并测定C的浓度为0.2mol·L ,下列判断正确的是
,下列判断正确的是