下列说法正确的是
| A.ΔS>0的反应一定是自发的 |
| B.平衡产率是化学反应的最大限度,是无法改变的 |
| C.电离与电解是相同的化学过程 |
| D.若MA为强碱弱酸盐,Ka(HA)越小,则Kh(A—)越大 |
更新时间:2023-01-14 17:39:11
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】对于反应:2A(g)+B(g)⇌2C(g) ΔH<0,下列图象正确的是
A.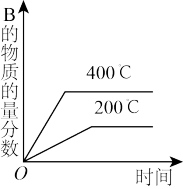 | B. |
C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据下列实验所得结论正确的是
| 选项 | A | B |
| 装置 | 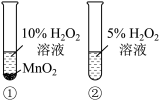 | 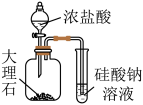 |
| 现象 | ①中产生大量气泡,②中无明显现象 | 试管中溶液出现浑浊 |
| 结论 | MnO2是H2O2分解的催化剂 | 酸性:碳酸>硅酸 |
| 选项 | C | D |
| 装置 | 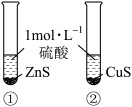 | 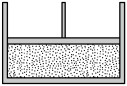 H2(g)+I2(g)⇌2HI(g)达到平衡状态 |
| 现象 | ①中固体溶解,②中固体不溶解 | 压缩体积,气体颜色加深 |
| 结论 | ZnS的溶解度大于CuS | 增大压强,上述平衡逆向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】一定温度下,将2molSO2和ImolO2充入1L恒容密闭容器中,发生反应:2SO2(g) +O2(g) 2SO3(g) △H=-196kJ·mol-1,5min时达到平衡,测得反应放热166.6kJ。下列说法错误的是
2SO3(g) △H=-196kJ·mol-1,5min时达到平衡,测得反应放热166.6kJ。下列说法错误的是
 2SO3(g) △H=-196kJ·mol-1,5min时达到平衡,测得反应放热166.6kJ。下列说法错误的是
2SO3(g) △H=-196kJ·mol-1,5min时达到平衡,测得反应放热166.6kJ。下列说法错误的是| A.0~5 min 内,用O2表示的平均反应速率V(O2)=0.17mol·L-1·min-1 |
| B.n(O2)/n(SO3)的值不变时,该反应达到平衡状态 |
| C.若增大O2的浓度,SO2的转化率增大 |
| D.条件不变,若起始时充入4molSO2和2molO2,平衡时放出的热量小于333.2kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】重晶石矿(含有较多的 )。重晶石矿常见三种处理方法如下:
)。重晶石矿常见三种处理方法如下:
热分解法: ;
;
碳热还原法: ;
;
沉淀转化法: ,
,
已知焓变与熵变是同一温度下的数值,下列说法不正确的是
 )。重晶石矿常见三种处理方法如下:
)。重晶石矿常见三种处理方法如下:热分解法:
 ;
;碳热还原法:
 ;
;沉淀转化法:
 ,
,已知焓变与熵变是同一温度下的数值,下列说法不正确的是
| A.高温有利于碳热还原法自发进行 |
| B.沉淀转化法的优点是节能、环保 |
C.热分解法获得 的同时,还生成 的同时,还生成 ,可联合生产硫酸,因此比碳热还原法更优 ,可联合生产硫酸,因此比碳热还原法更优 |
D.碳热还原法所得 可能含 可能含 等杂质,需进一步提纯 等杂质,需进一步提纯 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】对于化学反应方向的确定,下列说法不正确的是
| A.在温度、压强一定的条件下,焓因素和熵因素共同决定一个化学反应的方向 |
| B.温度、压强一定时,放热的熵增反应一定能自发进行 |
| C.能够自发进行的反应一定是熵增的过程 |
| D.固体的溶解过程与熵变有关 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,将0.01mol∙L-1盐酸逐滴加入10mL0.01mol∙L-1NaA溶液中。滴加过程中,A-、HA的物质的量分数(δ)随pH变化的关系如图1所示,pH随加入盐酸体积的变化如图2所示。下列说法正确的是
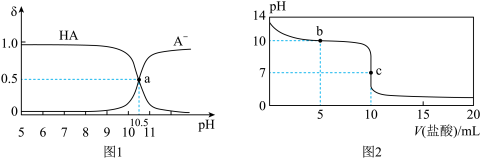

| A.当pH=7时,溶液中c(Cl-)=c(HA) |
| B.水解平衡常数Kh(NaA)=10-10.5 |
| C.b点对应溶液中:c(A-)>c(Cl-)>c(OH-) |
| D.c点对应溶液中:c(A-)+c(HA)= 0.01mol∙L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,用0.010mol·L-1NaOH溶液滴定0.010mol·L-1的二元酸H2A溶液,H2A、HA-、A2-的物质的量分数δ(X)随pH变化如图所示:下列说法错误的是


| A.滴加过程中离子浓度始终满足:c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-) |
| B.H2A的第一步电离平衡常数Ka1=1×10-6 |
| C.HA-的水解常数Kh=1×10-10 |
| D.将0.020mol·L-1Na2A溶液和0.010mol·L-1HCl溶液等体积混合,所得溶液的pH约为10 |
您最近一年使用:0次

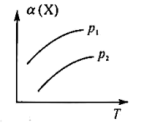
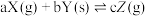 达到平衡后,X的转化率
达到平衡后,X的转化率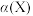 与温度
与温度 、压强
、压强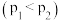 的关系如图所示。根据图像,下列判断正确的是
的关系如图所示。根据图像,下列判断正确的是