过硼酸钠(NaBO3•4H2O)是一种用途广泛的无机过氧化物,可用作织物的漂白、染色,医药上可作为消毒剂和杀菌剂。一种由硼镁矿(Mg2B2O5•H2O)制取过硼酸钠的工艺流程图如下:
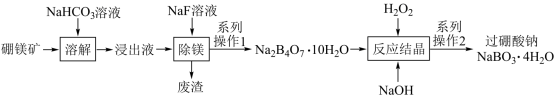
已知:过硼酸钠为白色晶状颗粒,熔点63℃,能溶于酸、碱,微溶于水,难溶于乙醇。在上述转化过程中硼元素的化合价始终未发生变化。回答下列问题:
(1)为加快“溶解”步骤的的速率可采取的措施___ (写一种即可)。
(2)“浸出液”中c(Mg2+)=2×10-3 mol/L,当Mg2+开始沉淀时,溶液中c(F-)=___ mol/L。[忽略溶液体积变化,已知Ksp(MgF2)= 2×10-11]
(3)过硼酸钠(NaBO3•4H2O)中硼元素的化合价为_____ 。
(4)写出“反应结晶”步骤中发生的化学反应方程式_____ 。
(5)“反应结晶”步骤在冰水浴中进行的原因___ 。
(6)过硼酸钠的水溶液不稳定,极易生成偏硼酸钠(NaBO2)并放出氧气,写出该反应的化学反应方程式____ 。
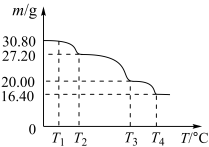
(7)过硼酸钠晶体(NaBO3•4H2O)可用作洗衣业的无氯漂白剂、清洗材料和牙齿增白剂,在70℃以上加热会逐步失去结晶水。实验测得过硼酸钠晶体的质量随温度变化的情况如下图所示,则T2℃时所得晶体的化学式为___ 。
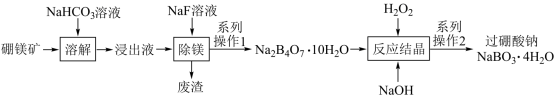
已知:过硼酸钠为白色晶状颗粒,熔点63℃,能溶于酸、碱,微溶于水,难溶于乙醇。在上述转化过程中硼元素的化合价始终未发生变化。回答下列问题:
(1)为加快“溶解”步骤的的速率可采取的措施
(2)“浸出液”中c(Mg2+)=2×10-3 mol/L,当Mg2+开始沉淀时,溶液中c(F-)=
(3)过硼酸钠(NaBO3•4H2O)中硼元素的化合价为
(4)写出“反应结晶”步骤中发生的化学反应方程式
(5)“反应结晶”步骤在冰水浴中进行的原因
(6)过硼酸钠的水溶液不稳定,极易生成偏硼酸钠(NaBO2)并放出氧气,写出该反应的化学反应方程式
(7)过硼酸钠晶体(NaBO3•4H2O)可用作洗衣业的无氯漂白剂、清洗材料和牙齿增白剂,在70℃以上加热会逐步失去结晶水。实验测得过硼酸钠晶体的质量随温度变化的情况如下图所示,则T2℃时所得晶体的化学式为

2021·广东·模拟预测 查看更多[2]
更新时间:2021-03-20 11:59:33
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
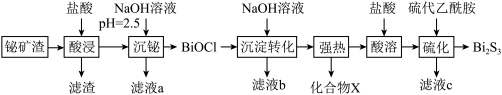
【推荐1】硫化铋(Bi2S3)广泛应用于太阳能电池、光电二极管及红外光谱学等。以铋矿渣(含Bi2O3、Fe2O3、CuO、Ag2O、Al2O3等)为原料制备Bi2S3的一种工艺流程如下。
②该工艺条件下,部分金属离子形成氢氧化物沉淀的pH如下表:
③常温下,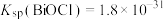 、
、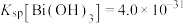 。
。
请回答下列问题:
(1)提高“酸浸”反应速率的措施是___________ (任答1条);“酸浸”中,形成“滤渣”的主要反应的离子方程式是___________ 。
(2)“滤液a”中主要的金属阳离有Fe3+、Cu2+___________ 。
(3)“沉铋”后所得BiOCl固体中含 杂质,设计实验去除BiOCl固体中含有的
杂质,设计实验去除BiOCl固体中含有的 杂质:
杂质:___________ 。
(4)“酸溶”时需加入过量的盐酸,盐酸过量的目的是___________ 、___________ 。
(5)已知常温时,BiOCl在水溶液中存在平衡: ,该反应的平衡常数为K,达到平衡时测得溶液pH=13,
,该反应的平衡常数为K,达到平衡时测得溶液pH=13,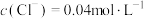 ,则K=
,则K=___________ 。
(6)化合物X的VSEPR模型是___________ 。
(7)已知 (硫代乙酰胺)
(硫代乙酰胺)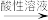
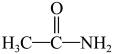 (乙酰胺)+H2S,则“硫化”的离子方程式为
(乙酰胺)+H2S,则“硫化”的离子方程式为___________ 。
②该工艺条件下,部分金属离子形成氢氧化物沉淀的pH如下表:
| 离子 | Fe3+ | Al3+ | Cu2+ |
| 开始沉淀时的pH | 1.5 | 3.6 | 4.5 |
| 沉淀完全时的pH | 3.2 | 4.7 | 6.7 |
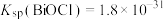 、
、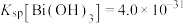 。
。请回答下列问题:
(1)提高“酸浸”反应速率的措施是
(2)“滤液a”中主要的金属阳离有Fe3+、Cu2+
(3)“沉铋”后所得BiOCl固体中含
 杂质,设计实验去除BiOCl固体中含有的
杂质,设计实验去除BiOCl固体中含有的 杂质:
杂质:(4)“酸溶”时需加入过量的盐酸,盐酸过量的目的是
(5)已知常温时,BiOCl在水溶液中存在平衡:
 ,该反应的平衡常数为K,达到平衡时测得溶液pH=13,
,该反应的平衡常数为K,达到平衡时测得溶液pH=13,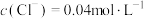 ,则K=
,则K=(6)化合物X的VSEPR模型是
(7)已知
 (硫代乙酰胺)
(硫代乙酰胺)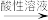
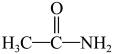 (乙酰胺)+H2S,则“硫化”的离子方程式为
(乙酰胺)+H2S,则“硫化”的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】 是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有少量
,还含有少量 、FeO、CoO、
、FeO、CoO、 )为原料制备
)为原料制备 的工艺流程如图。
的工艺流程如图。
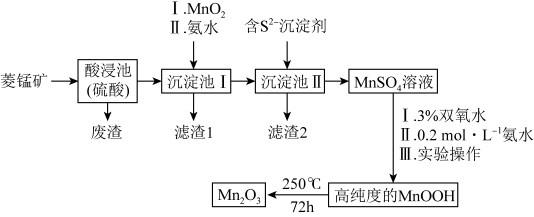
已知:25℃时,相关物质的 见表。
见表。
已知:氢氧化氧锰(MnOOH)难溶于水和碱性溶液。
(1)MnOOH中Mn的化合价为___________ 价。加快酸浸速率的措施___________ 。
(2)向“沉淀池Ⅰ”中加入 ,
, 的作用是
的作用是___________ (用离子方程式回答);“滤渣2”的主要成分是___________ (填化学式)。
(3) 转化为MnOOH的离子方程式为
转化为MnOOH的离子方程式为___________ 。
(4) 转化为MnOOH中“Ⅲ。实验操作”包含过滤、洗涤、干燥。检验MnOOH是否洗涤干净,具体操作为
转化为MnOOH中“Ⅲ。实验操作”包含过滤、洗涤、干燥。检验MnOOH是否洗涤干净,具体操作为___________ 。
(5)高纯度的MnOOH转化为 的化学方程式为
的化学方程式为___________ 。
(6)在“沉淀池Ⅰ”中,滴加氨水调节溶液的pH,使溶液中铝、铁元素完全沉淀,则理论上pH的最小值为___________ (当溶液中某离子浓度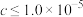 mol⋅L
mol⋅L 时。可认为该离子沉淀完全)。
时。可认为该离子沉淀完全)。
 是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有少量
,还含有少量 、FeO、CoO、
、FeO、CoO、 )为原料制备
)为原料制备 的工艺流程如图。
的工艺流程如图。
已知:25℃时,相关物质的
 见表。
见表。| 物质 |  |  |  |  |  |
 | 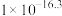 | 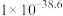 | 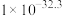 |  | 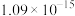 |
(1)MnOOH中Mn的化合价为
(2)向“沉淀池Ⅰ”中加入
 ,
, 的作用是
的作用是(3)
 转化为MnOOH的离子方程式为
转化为MnOOH的离子方程式为(4)
 转化为MnOOH中“Ⅲ。实验操作”包含过滤、洗涤、干燥。检验MnOOH是否洗涤干净,具体操作为
转化为MnOOH中“Ⅲ。实验操作”包含过滤、洗涤、干燥。检验MnOOH是否洗涤干净,具体操作为(5)高纯度的MnOOH转化为
 的化学方程式为
的化学方程式为(6)在“沉淀池Ⅰ”中,滴加氨水调节溶液的pH,使溶液中铝、铁元素完全沉淀,则理论上pH的最小值为
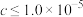 mol⋅L
mol⋅L 时。可认为该离子沉淀完全)。
时。可认为该离子沉淀完全)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】请回答下列问题:
(1)下列有关实验操作或结果的说法中正确的是___________ (填字母)。
A.滴定时,眼睛应始终注视滴定管内液面的变化
B.滴定实验都需要指示剂
C.酸碱中和滴定之前,锥形瓶用蒸馏水洗净即可,不能用待测液润洗
D.用pH试纸测量某溶液的pH时要先将试纸润湿
E.滴定管经蒸馏水洗净后,直接注入标准液,将使测得的待测液浓度偏高
F.用广泛pH试纸测量H2SO4溶液的pH时,测得pH=3.2
(2)有pH均为2的CH3COOH、HCl、H2SO4 三种物质的溶液,物质的量浓度由大到小的顺序为___________ ,若分别用这三种酸中和含等物质的量NaOH的溶液,所需酸溶液的体积分别为a、b、c,则a、b、c的大小关系是___________ 。
(3)NaHSO3溶液显酸性的原因是___________ (用化学用语和必要的文字说明)。
(4)常温时,BaSO4的Ksp=1.08×10-10,现将等体积的BaCl2溶液与3.5×10-3mol/L的Na2SO4溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小浓度为___________ 。
(1)下列有关实验操作或结果的说法中正确的是
A.滴定时,眼睛应始终注视滴定管内液面的变化
B.滴定实验都需要指示剂
C.酸碱中和滴定之前,锥形瓶用蒸馏水洗净即可,不能用待测液润洗
D.用pH试纸测量某溶液的pH时要先将试纸润湿
E.滴定管经蒸馏水洗净后,直接注入标准液,将使测得的待测液浓度偏高
F.用广泛pH试纸测量H2SO4溶液的pH时,测得pH=3.2
(2)有pH均为2的CH3COOH、HCl、H2SO4 三种物质的溶液,物质的量浓度由大到小的顺序为
(3)NaHSO3溶液显酸性的原因是
(4)常温时,BaSO4的Ksp=1.08×10-10,现将等体积的BaCl2溶液与3.5×10-3mol/L的Na2SO4溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小浓度为
您最近一年使用:0次
【推荐1】工业上常采用堆浸-反萃取-电积法从锌矿(主要成分为ZnS,含有FeS2、CuS、NiS、SiO2等杂质)中获得锌,其流程如图所示。
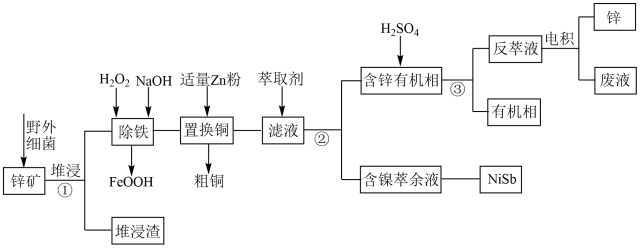
已知:①“堆浸”时金属硫化物均转化为硫酸盐;②pH较高时,氢氧化氧铁为胶状沉淀;③在我国,富矿少、贫矿多,品位低于5%的矿山属于贫矿。回答下列问题:
(1)“堆浸渣”的主要成分为_______ ,“堆浸”时为了提高反应速率,可以采取的措施为_______ (填标号)。
A.将锌矿粉碎 B.大幅度升温 C.延长堆浸时间 D.将锌矿充分暴露
(2)“除铁”时Zn2+、Cu2+、Ni2+在pH≤6时难以沉淀而除去,但是有Fe3+存在时,pH升高,Zn2+、Cu2+、Ni2+的去除率均升高,原因可能为_______ 。
(3)“置换铜”时用锌粉直接置换镍的速率极小,目前采用“锑盐净化法”,即在酸性含Ni2+溶液中同时加入锌粉和Sb2O3,可得到合金NiSb,该反应的离子方程式为_______ 。
(4)“萃取”时需要进行多次萃取且合并萃取液,其目的是_______ ,操作③的名称为_______ ,此流程中可循环利用的物质有锌、萃取剂和_______ 。
(5)反萃液的主要成分为ZnSO4,可通过一系列反应制备对可见光敏感的半导体催化剂ZnFe2O4。其中在无氧条件下灼烧ZnFe2(C2O4)3·6H2O获得产品ZnFe2O4时发生反应的化学方程式为_______ ,灼烧时需要借助马弗炉(Mufflefurnace,一种通用的加热设备,通常叫电炉等)和下列哪些仪器_______ (填标号)共同完成。
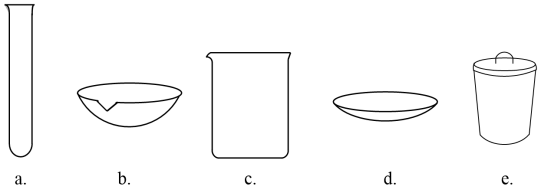
(6)“电积”时在_______ 极获得锌,得到的锌的质量分数为96.0% 。某企业利用上述流程从1600吨锌矿中可获得此种锌的质量为80吨,已知上述流程的总损耗率约为2%,则该锌矿为_______ (填“富矿”或“贫矿”)。

已知:①“堆浸”时金属硫化物均转化为硫酸盐;②pH较高时,氢氧化氧铁为胶状沉淀;③在我国,富矿少、贫矿多,品位低于5%的矿山属于贫矿。回答下列问题:
(1)“堆浸渣”的主要成分为
A.将锌矿粉碎 B.大幅度升温 C.延长堆浸时间 D.将锌矿充分暴露
(2)“除铁”时Zn2+、Cu2+、Ni2+在pH≤6时难以沉淀而除去,但是有Fe3+存在时,pH升高,Zn2+、Cu2+、Ni2+的去除率均升高,原因可能为
(3)“置换铜”时用锌粉直接置换镍的速率极小,目前采用“锑盐净化法”,即在酸性含Ni2+溶液中同时加入锌粉和Sb2O3,可得到合金NiSb,该反应的离子方程式为
(4)“萃取”时需要进行多次萃取且合并萃取液,其目的是
(5)反萃液的主要成分为ZnSO4,可通过一系列反应制备对可见光敏感的半导体催化剂ZnFe2O4。其中在无氧条件下灼烧ZnFe2(C2O4)3·6H2O获得产品ZnFe2O4时发生反应的化学方程式为

(6)“电积”时在
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】金、银是生活中常见的贵金属,用途非常广泛。工业上常利用氰化法从一种含金矿石(成分为Au、Ag、Fe2O3和其它不溶性杂质)中提取金。工艺流程如下:
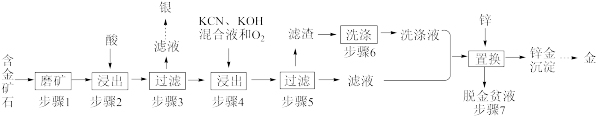
已知:① Zn + O2 + H2O = Zn(OH)2
O2 + H2O = Zn(OH)2
②Zn2+(aq)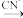 Zn(CN)2(s)
Zn(CN)2(s) 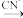 Zn(CN)
Zn(CN) (aq)
(aq)
(1)步骤1中“磨矿”的目的是___________ 。
(2)步骤2中浸出应选用___________ (填盐酸、硫酸或硝酸)。
(3)步骤4浸出的目的是将单质Au转化为Au(CN) 进入溶液,该反应的离子方程式为
进入溶液,该反应的离子方程式为___________ 。
(4)步骤4中为提高金的浸出速率可适当升高温度,但温度过高浸出速率反而会降低,原因是___________ 。
(5)步骤6的目的是___________ 。
(6)步骤7置换的总反应为:2Au(CN) +3Zn+4CN-+2H2O=2Au +2Zn(CN)
+3Zn+4CN-+2H2O=2Au +2Zn(CN) +ZnO
+ZnO +2H2↑,该过程中,为防止生成Zn(CN)2沉淀影响置换速率,可采取的措施是
+2H2↑,该过程中,为防止生成Zn(CN)2沉淀影响置换速率,可采取的措施是___________ 。
(7)脱金贫液(主要含有CN-)会破坏环境,可通过化学方法转化为无毒废水净化排放。碱性条件下,用NaClO将贫液中的CN- 氧化成无毒的CO 和N2,该反应的离子方程式为
和N2,该反应的离子方程式为___________ 。

已知:① Zn +
 O2 + H2O = Zn(OH)2
O2 + H2O = Zn(OH)2②Zn2+(aq)
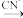 Zn(CN)2(s)
Zn(CN)2(s) 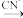 Zn(CN)
Zn(CN) (aq)
(aq)(1)步骤1中“磨矿”的目的是
(2)步骤2中浸出应选用
(3)步骤4浸出的目的是将单质Au转化为Au(CN)
 进入溶液,该反应的离子方程式为
进入溶液,该反应的离子方程式为(4)步骤4中为提高金的浸出速率可适当升高温度,但温度过高浸出速率反而会降低,原因是
(5)步骤6的目的是
(6)步骤7置换的总反应为:2Au(CN)
 +3Zn+4CN-+2H2O=2Au +2Zn(CN)
+3Zn+4CN-+2H2O=2Au +2Zn(CN) +ZnO
+ZnO +2H2↑,该过程中,为防止生成Zn(CN)2沉淀影响置换速率,可采取的措施是
+2H2↑,该过程中,为防止生成Zn(CN)2沉淀影响置换速率,可采取的措施是(7)脱金贫液(主要含有CN-)会破坏环境,可通过化学方法转化为无毒废水净化排放。碱性条件下,用NaClO将贫液中的CN- 氧化成无毒的CO
 和N2,该反应的离子方程式为
和N2,该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上由含铜废料(含有Cu、CuS、CuSO4等)制备硝酸铜晶体的流程如图:
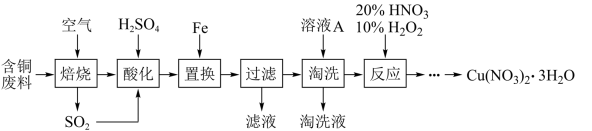
(1)写出CuS“焙烧”生成CuO和SO2的化学反应方程式:___________ 。
(2)图中SO2经转化生成的硫酸可用于“酸化”,转化反应中SO2与O2的物质的量之比为:_____ 。
(3)滤液的主要成分是___________ 。
(4)写出步骤中加10%H2O2的离子方程式:___________ 。
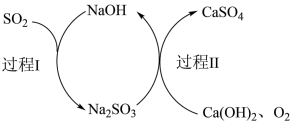
(5)大量排放SO2容易造成酸雨等环境问题,工业上可用双碱脱硫法处理废气。过程如图所示,其中可循环使用的试剂是___________ ,写出双碱脱硫法的总反应的化学方程式:___________ 。

(1)写出CuS“焙烧”生成CuO和SO2的化学反应方程式:
(2)图中SO2经转化生成的硫酸可用于“酸化”,转化反应中SO2与O2的物质的量之比为:
(3)滤液的主要成分是
(4)写出步骤中加10%H2O2的离子方程式:
(5)大量排放SO2容易造成酸雨等环境问题,工业上可用双碱脱硫法处理废气。过程如图所示,其中可循环使用的试剂是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】为探究某无结晶水的正盐X(仅含有两种短周期元素)的组成和性质,设计并完成下列实验。(气体体积已转化为标准状况下的体积)
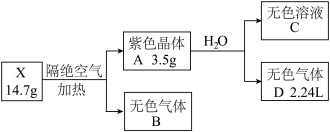
已知:B是空气的主要成分之一;C是一种强碱,且微溶于水,载人宇宙飞船内常用含C的过滤网吸收宇航员呼出的CO2,以净化空气;D遇湿润的红色石蕊试纸变蓝。
(1)B的组成元素在元素周期表中的位置是___ 。
(2)D分子的空间构型为___ 。
(3)X受热分解转变成A和B的化学反应方程式为___ 。

已知:B是空气的主要成分之一;C是一种强碱,且微溶于水,载人宇宙飞船内常用含C的过滤网吸收宇航员呼出的CO2,以净化空气;D遇湿润的红色石蕊试纸变蓝。
(1)B的组成元素在元素周期表中的位置是
(2)D分子的空间构型为
(3)X受热分解转变成A和B的化学反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】室内甲醛污染已被列入对公众健康影响最大的环境因素之一。市面上有一种光催化涂料,能够起到降低室内甲醛含量的作用。某化学兴趣小组想要通过此涂料来进行甲醛的光催化氧化反应,并测定被氧化的甲醛的量。设计实验装置如下:
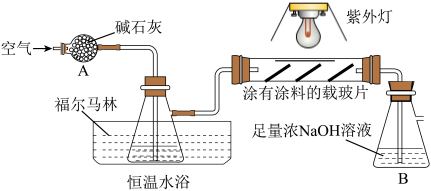
实验时先开启紫外灯,缓缓鼓入空气;一段时间后停止反应,关闭紫外灯,再继续通入一会儿空气,向B中加入足量BaCl2溶液,得到白色沉淀5.91 g。
(1)甲醛是一种重要的有机原料,用它制取酚醛树脂的化学方程式为_____________________ ,福尔马林是甲醛含量37%的水溶液,它的一个用途是____________ 。
(2)上图装置A中,碱石灰的作用是______________ ,恒温水浴的目的是_______________ 。
(3)硬质玻璃管中,甲醛在光催化氧化条件下的反应方程式:__________________________ 。
(4)计算被氧化的甲醛的物质的量为_________ mol。
(5)反应结束后,继续通入一会儿空气的目的是_____________________________________ 。
(6)甲同学认为,反应过程中部分甲醛可能被氧化为甲酸。为验证其存在,甲同学取B中溶液,分别选用下表试剂进行检验。但乙同学认为试剂选择均不合理,他的理由是:

实验时先开启紫外灯,缓缓鼓入空气;一段时间后停止反应,关闭紫外灯,再继续通入一会儿空气,向B中加入足量BaCl2溶液,得到白色沉淀5.91 g。
(1)甲醛是一种重要的有机原料,用它制取酚醛树脂的化学方程式为
(2)上图装置A中,碱石灰的作用是
(3)硬质玻璃管中,甲醛在光催化氧化条件下的反应方程式:
(4)计算被氧化的甲醛的物质的量为
(5)反应结束后,继续通入一会儿空气的目的是
(6)甲同学认为,反应过程中部分甲醛可能被氧化为甲酸。为验证其存在,甲同学取B中溶液,分别选用下表试剂进行检验。但乙同学认为试剂选择均不合理,他的理由是:
| 甲同学选择的试剂 | 乙同学认为不合理的理由 |
| 紫色石蕊试液 | |
| 新制氢氧化铜 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】五氧化二氮(N2O5)是一种绿色硝化剂,在军用炸药、火箭推进剂、医药等工业中得到广泛应用。常温下N2O5为白色固体,可溶于二氯甲烷等氯代烃溶剂,微溶于水且与水反应生成硝酸,高于室温时不稳定。回答下列问题:
(1)1840年,Devill将干燥的氯气通入无水硝酸银中,首次制得了固体N2O5。该反应的氧化产物为空气中的主要成分之一,写出反应的化学方程式:_______ 。
(2)某化学兴趣小组设计用臭氧(O3)氧化法制备N2O5,反应原理为 N2O4+O3→N2O5+O2。实验装置如下图:
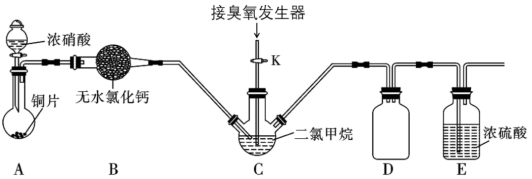
装置B的仪器名称是_______ ;装置E的作用是_______ 。实验时,先将三口烧瓶C浸入_______ (填字母编号)中,打开装置A中分液漏斗的活塞,随即关闭。一段时间后C中液体变为红棕色。然后打开活塞K,通过臭氧发生器向三口烧瓶中通入含有臭氧的氧气。
a.热水 b.冰水 c.自来水 d.饱和食盐水
(3)C中二氯甲烷(CH2Cl2)的作用是_______ (填字母编号)。判断C中反应已结束的简单方法是_______ 。
a.溶解反应物NO2 b.充分混合反应物使其反应更加充分 c.控制O3的通入速度 d.溶解生成物N2O5
(4)该装置存在一处明显缺陷,请指出_______ 。
(5)N2O5粗产品中常含有N2O4。该兴趣小组用滴定法测定N2O5粗产品的纯度。取2.0g粗产品,加入20.00mL 0.1250mol·L-1酸性高锰酸钾溶液。充分反应后,用0.1000mol·L-1 H2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液17.50mL。已知:N2O4与KMnO4发生反应的离子方程式为5N2O4+2MnO +2H2O→Mn2++10NO
+2H2O→Mn2++10NO +4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO
+4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO +6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是
+6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是_______ 。粗产品的纯度为_______ (结果保留三位有效数字)。
(1)1840年,Devill将干燥的氯气通入无水硝酸银中,首次制得了固体N2O5。该反应的氧化产物为空气中的主要成分之一,写出反应的化学方程式:
(2)某化学兴趣小组设计用臭氧(O3)氧化法制备N2O5,反应原理为 N2O4+O3→N2O5+O2。实验装置如下图:

装置B的仪器名称是
a.热水 b.冰水 c.自来水 d.饱和食盐水
(3)C中二氯甲烷(CH2Cl2)的作用是
a.溶解反应物NO2 b.充分混合反应物使其反应更加充分 c.控制O3的通入速度 d.溶解生成物N2O5
(4)该装置存在一处明显缺陷,请指出
(5)N2O5粗产品中常含有N2O4。该兴趣小组用滴定法测定N2O5粗产品的纯度。取2.0g粗产品,加入20.00mL 0.1250mol·L-1酸性高锰酸钾溶液。充分反应后,用0.1000mol·L-1 H2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液17.50mL。已知:N2O4与KMnO4发生反应的离子方程式为5N2O4+2MnO
 +2H2O→Mn2++10NO
+2H2O→Mn2++10NO +4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO
+4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO +6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是
+6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是
您最近一年使用:0次



