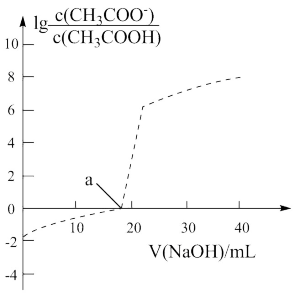
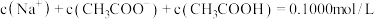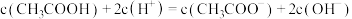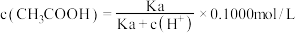下列各溶液中,微粒的物质的量浓度关系正确的是
A.1.0mol/LNa2CO3溶液:c(OH-)=c(HCO )+c(H+)+2c(H2CO3) )+c(H+)+2c(H2CO3) |
B.1.0mol/LNH4Cl溶液:c(NH )=c(Cl-) )=c(Cl-) |
| C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
D.1.0mol/LNaHCO3溶液中:c(OH-)+c(HCO )=c(H+)+c(Na+) )=c(H+)+c(Na+) |
更新时间:2021-04-22 17:18:19
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列关于 溶液的说法正确的是
溶液的说法正确的是
 溶液的说法正确的是
溶液的说法正确的是A.溶质的电离方程式为 |
B.溶液中微粒浓度关系满足: 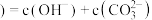 |
C.离子浓度关系: |
D.温度升高, 增大 增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】醋酸钙[(CH3COO)2Ca•H2O]常用作食品稳定剂和抑霉剂。设NA为阿伏加德罗常数值。关于常温下0.1 mol•L-1的(CH3COO)2Ca溶液,下列说法正确的是
| A.每升溶液中CH3COO-的数目为0.2NA |
| B.稀释溶液,则溶液的pH增大 |
| C.c(OH-)=c(H+)+c(CH3COOH) |
| D.c(H+)+c(Ca2+)=c(CH3COO-)+c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列溶液中粒子的物质的量浓度关系正确的是( )
| A.0.1mol/L NaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) |
| B.20ml 0.1mol/LCH3COONa溶液与10ml 0.1mol/LHCl溶液混合后呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(OH-) |
| C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| D.0.1mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+ c(CH3COOH) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知H2RO3为二元弱酸。常温下,用0. 10mol·L Na2RO3溶液吸收RO2气体,吸收液的pH与 的关系如图所示(忽略溶液体积变化)。下列说法不正确的是
的关系如图所示(忽略溶液体积变化)。下列说法不正确的是

 的关系如图所示(忽略溶液体积变化)。下列说法不正确的是
的关系如图所示(忽略溶液体积变化)。下列说法不正确的是
| A.常温下,K2(H2RO3)的数量级为10-8 |
B.常温下,中性溶液中c(HRO )>c(RO )>c(RO ) ) |
C.E点时,c(Na+)>c(RO )>c(OH-)>c(HRO )>c(OH-)>c(HRO )>c(H+) )>c(H+) |
D.G点时,2c(RO )+c(HRO )+c(HRO )-c(Na+)=(1.0×10-6.2-1.0×10-7.8)mol·L )-c(Na+)=(1.0×10-6.2-1.0×10-7.8)mol·L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】常温下,向 溶液中滴加
溶液中滴加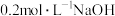 溶液。有关微粒的物质的量变化如图(其中Ⅰ代表
溶液。有关微粒的物质的量变化如图(其中Ⅰ代表 ,Ⅱ代表
,Ⅱ代表 ,Ⅲ代表A2-)。根据图示判断,下列说法不正确的是
,Ⅲ代表A2-)。根据图示判断,下列说法不正确的是
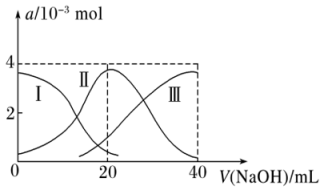
 溶液中滴加
溶液中滴加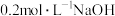 溶液。有关微粒的物质的量变化如图(其中Ⅰ代表
溶液。有关微粒的物质的量变化如图(其中Ⅰ代表 ,Ⅱ代表
,Ⅱ代表 ,Ⅲ代表A2-)。根据图示判断,下列说法不正确的是
,Ⅲ代表A2-)。根据图示判断,下列说法不正确的是
A.当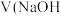 溶液 溶液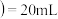 时,溶液中离子浓度大小关系: 时,溶液中离子浓度大小关系: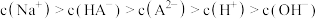 |
B.NaHA溶液中: |
C.当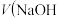 溶液 溶液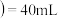 时,其溶液中水的电离程度比纯水大 时,其溶液中水的电离程度比纯水大 |
D.向 溶液加入水的过程中,pH减小 溶液加入水的过程中,pH减小 |
您最近一年使用:0次

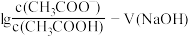 图象如图,下列说法
图象如图,下列说法