将0.01 mol CH3COONa溶于水,形成1 L溶液。
(1)该溶液中存在两个平衡体系,用电离方程式或离子方程式表示:
①_______ ;
②_______ 。
(2)该溶液中存在的粒子有:_______ (填粒子符号,下同),浓度为0.01 mol·L-1的粒子是_______ 。
(3)该溶液中存在三个守恒关系式:
①物料守恒:_______ ;
②电荷守恒:_______ ;
③质子守恒:_______ 。
(4)该溶液中离子浓度大小顺序为:_______ 。
(1)该溶液中存在两个平衡体系,用电离方程式或离子方程式表示:
①
②
(2)该溶液中存在的粒子有:
(3)该溶液中存在三个守恒关系式:
①物料守恒:
②电荷守恒:
③质子守恒:
(4)该溶液中离子浓度大小顺序为:
更新时间:2021-04-28 09:14:32
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】常温下,将某一元酸 和
和 溶液等体积混合,两种溶液的浓度和混合后所得溶液的
溶液等体积混合,两种溶液的浓度和混合后所得溶液的 如下表:
如下表:
(1)从①组情况分析, 是强酸还是弱酸?
是强酸还是弱酸?___________ 。
(2)②组情况表明,
___________ (填“>”、“<”或“=”,下同)0.2.混合溶液中离子浓度
___________  。
。
(3)从③组实验结果分析, 的电离程度
的电离程度___________ (填“>”、“<”或“=”) 的水解程度,该混合溶液中离子浓度由大到小的顺序是
的水解程度,该混合溶液中离子浓度由大到小的顺序是___________ 。
(4)从以上实验分析,将 的
的 溶液与
溶液与 的
的 溶液等体积混合,所得混合溶液中
溶液等体积混合,所得混合溶液中
___________ (填“>”、“<”或“=”) 。
。
 和
和 溶液等体积混合,两种溶液的浓度和混合后所得溶液的
溶液等体积混合,两种溶液的浓度和混合后所得溶液的 如下表:
如下表:| 实验编号 |  溶液的物质的量浓度 溶液的物质的量浓度 |  溶液的物质的量浓度 溶液的物质的量浓度 | 混合溶液的 |
| ① | 0.1 | 0.1 |  |
| ② |  | 0.2 |  |
| ③ | 0.2 | 0.1 |  |
 是强酸还是弱酸?
是强酸还是弱酸?(2)②组情况表明,


 。
。(3)从③组实验结果分析,
 的电离程度
的电离程度 的水解程度,该混合溶液中离子浓度由大到小的顺序是
的水解程度,该混合溶液中离子浓度由大到小的顺序是(4)从以上实验分析,将
 的
的 溶液与
溶液与 的
的 溶液等体积混合,所得混合溶液中
溶液等体积混合,所得混合溶液中
 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】常温下,向100mL 的HA溶液中逐滴加入
的HA溶液中逐滴加入 的MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
的MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:

(1)由图中信息可知HA为______ 酸(填“强”或“弱”),理由是______ 。
(2)常温下一定浓度的MA稀溶液的 ,则a
,则a______ (填“>”“<”或“=”)7,用离子方程式表示其原因:______ ,此时,溶液中由水电离出的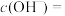
______ 。
(3)请写出K点所对应的溶液中离子浓度的大小关系:______ 。
(4)K点对应的溶液中,
______ (填“>”“<”或“=”) 。
。
 的HA溶液中逐滴加入
的HA溶液中逐滴加入 的MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
的MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
(1)由图中信息可知HA为
(2)常温下一定浓度的MA稀溶液的
 ,则a
,则a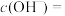
(3)请写出K点所对应的溶液中离子浓度的大小关系:
(4)K点对应的溶液中,

 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】请按要求填空。
(1)AgNO3的水溶液呈________ (填“酸”、“中”、“碱”)性,实验室在配制AgNO3的溶液时,常将AgNO3固体先____________________ ,然后再_________________________ ,以抑制其水解。
(2)硫化钠溶于水时发生水解,其水解的离子方程式为_____________________________ ,在配制硫化钠溶液时可以加入少量的________________ 以抑制其水解。
(1)AgNO3的水溶液呈
(2)硫化钠溶于水时发生水解,其水解的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
①HCOONa、NaCN、NaHCO3、Na2CO3这4种溶液中阴离子结合质子能力最强的是__________ 。
②体积相同、c(H+)相同的三种酸溶液a.HCOOH;b.HCN;c.H2SO4分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母)___________ 。
③向NaCN溶液通入少量CO2反应的化学方程式是_____________________________ 。
(2)①一定浓度的NaCN溶液pH=9,用离子方程式表示呈碱性的原因是____________ ;此时c(HCN)/c(CN-)=____________ 。
②常温下,NaCN与过氧化氢溶液反应,生成NaHCO3和能使湿润的红色石蕊试纸变蓝色的气体,大大降低其毒性。该反应的化学方程式是___________________________ 。
(3)已知CaCO3的Ksp=2.8×10-9,现将浓度为2×10-4 mol·L-1 Na2CO3溶液与CaCl2溶液等体积混合,则生成CaCO3沉淀所需CaCl2溶液的最小浓度为_____________ mol·L-1。
(1)已知部分弱酸的电离常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离常数(25 ℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
②体积相同、c(H+)相同的三种酸溶液a.HCOOH;b.HCN;c.H2SO4分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母)
③向NaCN溶液通入少量CO2反应的化学方程式是
(2)①一定浓度的NaCN溶液pH=9,用离子方程式表示呈碱性的原因是
②常温下,NaCN与过氧化氢溶液反应,生成NaHCO3和能使湿润的红色石蕊试纸变蓝色的气体,大大降低其毒性。该反应的化学方程式是
(3)已知CaCO3的Ksp=2.8×10-9,现将浓度为2×10-4 mol·L-1 Na2CO3溶液与CaCl2溶液等体积混合,则生成CaCO3沉淀所需CaCl2溶液的最小浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】有均为1mol/L的Na2CO3、FeCl3溶液,在Na2CO3溶液中滴入酚酞,则溶液呈现________ (填“浅红”或“红色”,原因:__________________________ (用离子方程表达),加热,则颜色变_________ (浅或深),在FeCl3溶液中滴入石蕊,,则溶液呈现________ (填颜色),若将其蒸干并灼烧,则得到的固体物质为:__________________________ ,若将饱和的FeCl3滴入沸水,则发生的反应: _________________________ (用离子方程表达)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)水的离子积常数Kw与温度t(℃)的关系如图所示:
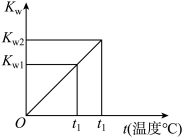
若t1=25℃,则Kw1=_______ ;若t2=100℃时,Kw2=10-12,则此时0.05mol·L-1的Ba(OH)2溶液的pH=_______ 。
(2)常温下用NaOH、氨水、CH3COOH、HCl、NH4HSO4五种溶液进行下列实验:
①浓度均为0.1mol/L的HCl和CH3COOH的pH:HCl_______ CH3COOH(填“<”“>”或“=”)。
②将xL0.01mol/L氨水与yL0.01mol/LHCl溶液充分反应至溶液呈中性,x、y大小关系为:x_______ y(填“<”“>”或“=”)。
③浓度均为0.1mol/L的NH4HSO4与NaOH等体积混合,反应的离子方程式为_______ ;此时溶液呈_______ 性(填“酸性”碱性”或“中性”)。
④用水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是_______ (填写序号)。
① ②
② ③c
③c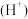 和c
和c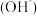 的乘积 ④
的乘积 ④ 的物质的量
的物质的量
(1)水的离子积常数Kw与温度t(℃)的关系如图所示:

若t1=25℃,则Kw1=
(2)常温下用NaOH、氨水、CH3COOH、HCl、NH4HSO4五种溶液进行下列实验:
①浓度均为0.1mol/L的HCl和CH3COOH的pH:HCl
②将xL0.01mol/L氨水与yL0.01mol/LHCl溶液充分反应至溶液呈中性,x、y大小关系为:x
③浓度均为0.1mol/L的NH4HSO4与NaOH等体积混合,反应的离子方程式为
④用水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是
①
 ②
② ③c
③c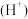 和c
和c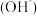 的乘积 ④
的乘积 ④ 的物质的量
的物质的量
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】请你设计实验探究促进或抑制 水解的条件,了解影响盐类水解程度的因素。
水解的条件,了解影响盐类水解程度的因素。
可供选择的仪器、用品和试剂:烧杯、试管、玻璃棒、胶头滴管、量筒、酒精灯、 计、
计、 试纸;1 mol∙L−1盐酸、氯化氢气体、1 mol∙L−1氢氧化钠溶液、1 mol∙L−1氯化铁溶液、蒸馏水。
试纸;1 mol∙L−1盐酸、氯化氢气体、1 mol∙L−1氢氧化钠溶液、1 mol∙L−1氯化铁溶液、蒸馏水。
完成下列探究过程:
(1)写出 水解的离子方程式:
水解的离子方程式:_______ 。
(2)针对影响 水解的因素提出假设:
水解的因素提出假设:
假设1:溶液的酸碱性;
假设2:_______ ;
假设3:_______ 。
(3)基于以上3个假设,设计出实验方案,将实验操作、预期现象和结论填在下表中。
 水解的条件,了解影响盐类水解程度的因素。
水解的条件,了解影响盐类水解程度的因素。可供选择的仪器、用品和试剂:烧杯、试管、玻璃棒、胶头滴管、量筒、酒精灯、
 计、
计、 试纸;1 mol∙L−1盐酸、氯化氢气体、1 mol∙L−1氢氧化钠溶液、1 mol∙L−1氯化铁溶液、蒸馏水。
试纸;1 mol∙L−1盐酸、氯化氢气体、1 mol∙L−1氢氧化钠溶液、1 mol∙L−1氯化铁溶液、蒸馏水。完成下列探究过程:
(1)写出
 水解的离子方程式:
水解的离子方程式:(2)针对影响
 水解的因素提出假设:
水解的因素提出假设:假设1:溶液的酸碱性;
假设2:
假设3:
(3)基于以上3个假设,设计出实验方案,将实验操作、预期现象和结论填在下表中。
| 步骤编号 | 实验操作 | 预期现象和结论 |
| ① | ||
| ② | ||
| ③ |
您最近一年使用:0次

 溶液中,
溶液中,
 ;
; 溶液的
溶液的
 溶液呈
溶液呈 溶液和
溶液和
 。
。


