25℃时,向20.00 mL 0.1000 mol·L-1的Na2R溶液中滴入 0.1000 mol·L-1的盐酸,溶液的pH与所加盐酸体积的关系如图所示(忽略混合过程中溶液体积的变化)。下列说法错误的是
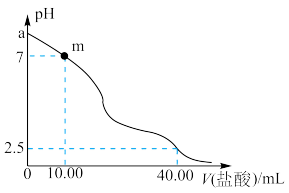

| A.Ka2(H2R)>Kh1(R2-) |
| B.Ka1(H2R)的数量级为10-4 |
| C.滴定过程中水的电离程度先减小后增大 |
| D.m点时,溶液中存在c(Cl-)+2c(R2-)+c(HR-)=c(Na+) |
2021·全国·模拟预测 查看更多[2]
更新时间:2021-05-24 19:43:54
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】表示下列变化的化学用语正确的是
A.NaHS溶液显碱性:HS-+H2O H3O++S2- H3O++S2- |
B.NaHSO4在水溶液中的电离方程式:NaHSO4=Na++HSO |
C.MgCl2溶液显酸性:Mg2++2H2O Mg(OH)2+2H+ Mg(OH)2+2H+ |
| D.铁在潮湿空气中被腐蚀的负极反应式:Fe-3e-=Fe3+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
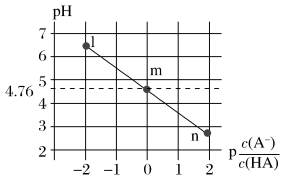
【推荐2】常温下,将NaOH溶液滴加到某一元酸(HA)溶液中,测得混合溶液的pH与离子浓度变化关系如图所示[已知:p =-lg
=-lg ]。下列叙述不正确的是
]。下列叙述不正确的是
 =-lg
=-lg ]。下列叙述不正确的是
]。下列叙述不正确的是
| A.Ka(HA)的数量级为10−5 |
| B.m点所示溶液中:c(A−)=c(HA) |
C.滴加NaOH溶液过程中,  保持不变 保持不变 |
| D.滴加NaOH溶液过程中反应为HA+OH−=A−+H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,用0.1000mol/LNaOH溶液滴定20.00mL 0.1000 mol/LCH3COOH溶液所得滴定曲线如图所示。下列说法不正确的是
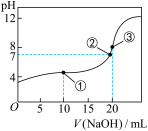

| A.滴定时应选酚酞作指示剂 |
| B.点①所示溶液中: c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+) |
| C.点②所示溶液中: c(Na+)= c(CH3COO-)> c(OH-)= c(H+) |
| D.点③所示溶液中: c(Na+)> c(CH3COO-) > c(OH-) > c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列叙述正确的是
A.常温下,将稀氨水逐滴加入稀硫酸中,当溶液的 时, 时, |
B.两种醋酸溶液的物质的量浓度分别为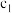 和 和 ,pH分别为a和 ,pH分别为a和 ,则 ,则 |
C.常温下, 的NaOH溶液与 的NaOH溶液与 的醋酸溶液等体积混合,滴入石蕊溶液呈红色 的醋酸溶液等体积混合,滴入石蕊溶液呈红色 |
D.向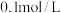 的氨水中加入少量硫酸铵固体,则溶液中 的氨水中加入少量硫酸铵固体,则溶液中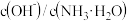 的值增大 的值增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知亚磷酸 为二元弱酸,其溶液中含磷粒子的物质的量分数与pH的关系如下图所示。
为二元弱酸,其溶液中含磷粒子的物质的量分数与pH的关系如下图所示。
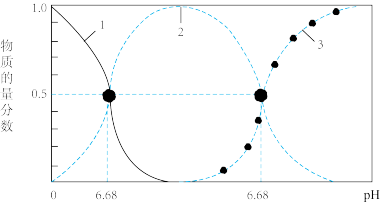
下列说法正确的是
 为二元弱酸,其溶液中含磷粒子的物质的量分数与pH的关系如下图所示。
为二元弱酸,其溶液中含磷粒子的物质的量分数与pH的关系如下图所示。
下列说法正确的是
A. 的电离方程式为 的电离方程式为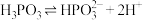 |
B.曲线1表示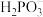 的物质的量分数变化 的物质的量分数变化 |
C. 的水溶液显碱性 的水溶液显碱性 |
D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】25°C时,NH4+的水解平衡常数为Kh=5.65×10-10.该温度下,用0.100mol/L的氨水滴定10.00ml0.050mol/L的二元酸H2A的溶液,滴定过程中加入氨水的体积V与溶液中lg 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是

 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
A.H2A的第一步电离方程式为H2A H++HA- H++HA- |
| B.P点时加入氨水的体积为10mL |
| C.25℃时,NH3·H2O的电离平衡常数Kb(NH3·H2O)=1.77×10-5 |
| D.向H2A溶液中滴加氨水的过程中,水的电离程度逐渐增大 |
您最近一年使用:0次

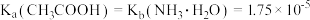 ,下列说法正确的是(
,下列说法正确的是(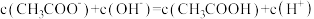
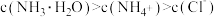
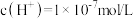

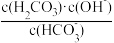 ,则该表达式对应的反应方程式为
,则该表达式对应的反应方程式为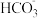 +H2O
+H2O +H3O+
+H3O+

