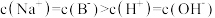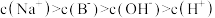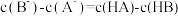室温下,将1.0mol·L-1的盐酸滴入20.00mL1.0mol/L的氨水中,溶液的pH和温度随加入盐酸体积的变化曲线如图所示。下列有关说法正确的是
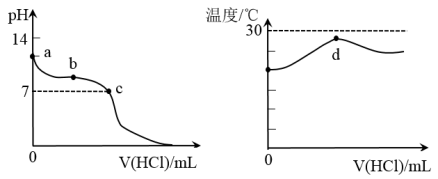

| A.a点时,由水电离出的c(H+)=1.0×10-14mol/L |
B.b点:c(NH )+c(NH3·H2O)=c(Cl-) )+c(NH3·H2O)=c(Cl-) |
C.c点:c(Cl-)=c(NH ) ) |
| D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸收热量 |
更新时间:2021-05-22 19:30:45
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】室温时,下列混合溶液的pH一定小于7的是( )
| A.pH=3的盐酸和pH=11的氨水等体积混合 |
| B.pH=3的盐酸和pH=11的氢氧化钡溶液等体积混合 |
| C.pH=3的醋酸和pH=11的氢氧化钡溶液等体积混合 |
| D.pH=3的硫酸和pH=11的氨水等体积混合 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】把80 mL NaOH溶液加入到120 mL的HCl溶液中,所得溶液的pH为2,如果混合前两溶液的浓度相同,则它们的浓度是
A.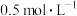 | B. | C. | D.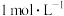 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实中,能说明HA是弱酸的是
| A.0.10 mol·L-1 HA溶液能使紫色石蕊试液变红 |
| B.0.10 mol·L-1 HA溶液能与鸡蛋壳反应生成CO2气体 |
| C.0.10 mol·L-1 NH4Cl呈酸性,0.10 mol·L-1 NH4A溶液呈中性 |
| D.等体积的0.10 mol·L-1HA溶液与0.10 mol·L-1NaOH溶液恰好完全反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】化学常用图像直观地描述化学反应的进程或结果。下列图像描述不正确 的是
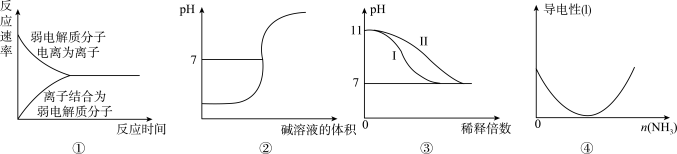

| A.图①表示弱电解质在水中建立电离平衡的过程 |
| B.图②表示强碱滴定强酸的滴定曲线 |
| C.图③表示25℃时分别稀释pH=11的NaOH溶液和氨水时溶液pH的变化,曲线Ⅱ表示氨水 |
D.图④可表示 溶液中通入 溶液中通入 至过量的过程中溶液导电性的变化 至过量的过程中溶液导电性的变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下,已知醋酸的电离常数为1.75×10-5,向20 mL 0.01mol•L-l CH3COOH溶液中逐滴加入0.01 molL-l的NaOH溶液,溶液中水电离的c(H+)随加入NaOH溶液的体积变化如图所示,下列说法不正确的是(已知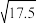 =4.2)
=4.2)
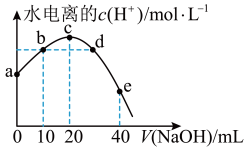
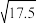 =4.2)
=4.2)
| A.b、d两点溶液的pH不相同 |
| B.a点坐标为(0,2.4×10 -11) |
| C.b点溶液中离子浓度大小顺序是:c(CH3COO- )> c(Na+)>c(H+)>c(OH- ) |
| D.e点所示溶液中,c(Na+)=2[c(CH3COO-)+c(CH3COOH)]=0.005 mol•L- 1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】亚氯酸钠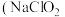 )在溶液中会生成
)在溶液中会生成 、
、 、
、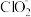 、
、 等,其中
等,其中 和
和 都是具有漂白作用。已知
都是具有漂白作用。已知 ,经测定
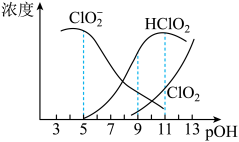
,经测定 时各组分含量随
时各组分含量随 变化情况如图所示(
变化情况如图所示( 浓度没有画出),此温度下,下列分析正确的是
浓度没有画出),此温度下,下列分析正确的是
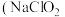 )在溶液中会生成
)在溶液中会生成 、
、 、
、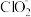 、
、 等,其中
等,其中 和
和 都是具有漂白作用。已知
都是具有漂白作用。已知 ,经测定
,经测定 时各组分含量随
时各组分含量随 变化情况如图所示(
变化情况如图所示( 浓度没有画出),此温度下,下列分析正确的是
浓度没有画出),此温度下,下列分析正确的是
A. 的电离平衡常数的数值 的电离平衡常数的数值 |
B. 时, 时,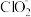 部分转化成 部分转化成 和 和 离子的方程式为: 离子的方程式为: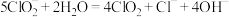 |
C. 时,溶液中含氯微粒的浓度大小为: 时,溶液中含氯微粒的浓度大小为: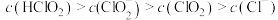 |
D.同浓度 溶液和 溶液和 溶液等体积混合,则混合溶液中有: 溶液等体积混合,则混合溶液中有: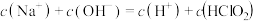 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
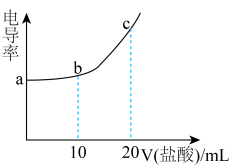
【推荐2】草酸钠( )是一种还原剂,也常作为配合物的双齿配体,使用时必须符合国家标准。用标准的盐酸、电导率仪测得滴加盐酸体积与待测草酸钠溶液(10mL)电导率的关系如图所示,溶液的浓度均为
)是一种还原剂,也常作为配合物的双齿配体,使用时必须符合国家标准。用标准的盐酸、电导率仪测得滴加盐酸体积与待测草酸钠溶液(10mL)电导率的关系如图所示,溶液的浓度均为 。已知草酸25℃其电离平衡常数
。已知草酸25℃其电离平衡常数 ,
, (其中
(其中 )。下列说法正确的是
)。下列说法正确的是
 )是一种还原剂,也常作为配合物的双齿配体,使用时必须符合国家标准。用标准的盐酸、电导率仪测得滴加盐酸体积与待测草酸钠溶液(10mL)电导率的关系如图所示,溶液的浓度均为
)是一种还原剂,也常作为配合物的双齿配体,使用时必须符合国家标准。用标准的盐酸、电导率仪测得滴加盐酸体积与待测草酸钠溶液(10mL)电导率的关系如图所示,溶液的浓度均为 。已知草酸25℃其电离平衡常数
。已知草酸25℃其电离平衡常数 ,
, (其中
(其中 )。下列说法正确的是
)。下列说法正确的是
A.a点代表正盐溶液, 的数量级为 的数量级为 |
B.b点溶液中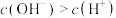 |
C.c点溶液满足 |
| D.电导率与离子浓度和离子种类有关,与离子所带电荷无关 |
您最近一年使用:0次

 的
的 溶液分别滴定
溶液分别滴定 浓度均为
浓度均为 溶液和
溶液和 溶液,所得滴定曲线如图所示。下列说法不正确的是
溶液,所得滴定曲线如图所示。下列说法不正确的是