草酸(H2C2O4)是二元中强酸,常温下用NaOH溶液滴定草酸溶液,溶液中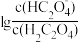 或
或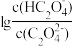 与混合溶液pH关系如图所示。下列说法中正确的是
与混合溶液pH关系如图所示。下列说法中正确的是

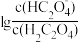 或
或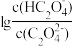 与混合溶液pH关系如图所示。下列说法中正确的是
与混合溶液pH关系如图所示。下列说法中正确的是
A.交叉点b,c(H2C2O4)=c( ) ) |
| B.常温下,NaHC2O4溶液pH>7 |
C.草酸的 |
D.a点溶液中:c(H+)-c(OH-)=c( )+c( )+c( )-c(Na+) )-c(Na+) |
更新时间:2021-08-06 12:04:10
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列说法正确的是
A.25℃时,某物质的溶液中由水电离出的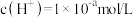 且a>7,则该溶液的pH为 且a>7,则该溶液的pH为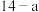 |
B. 的一元碱BOH溶液的pH=12,则BOH一定是一种弱电解质 的一元碱BOH溶液的pH=12,则BOH一定是一种弱电解质 |
| C.25℃时,pH=2的硫酸和pH=2的醋酸以体积比1:10混合,溶液pH为2 |
D.25℃时,向 溶液中加入少量水,溶液中 溶液中加入少量水,溶液中 减小 减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温下,将pH均为3,体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随1g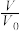 的变化如右图所示。下列说法正确的是
的变化如右图所示。下列说法正确的是
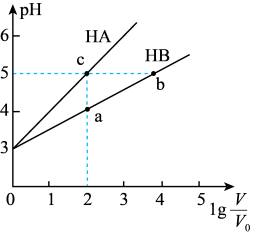
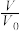 的变化如右图所示。下列说法正确的是
的变化如右图所示。下列说法正确的是
| A.稀释相同倍数时:c(Aˉ)>c(Bˉ-) |
| B.水的电离程度:b=c>a |
| C.溶液中离子总物质的量:b>c>a |
| D.溶液中离子总浓度:a>b>c |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】部分弱酸的电离平衡常数如下表:
下列说法不正确 的是
| 弱酸 | HCOOH | HCN |  |
| 电离平衡常数(25℃) |  | 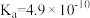 |  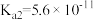 |
A.室温时,将 的稀KOH溶液与 的稀KOH溶液与 的稀HCOOH充分反应,若 的稀HCOOH充分反应,若 , ,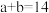 ,则反应后溶液 ,则反应后溶液 |
| B.中和等体积、等物质的量浓度的HCOOH和HCN消耗NaOH的物质的量相等 |
| C.等浓度的HCOOH和HCN稀释相同的倍数后pH前者小于后者 |
D.c(NH )相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中,c(NH4HCO3)>c(NH4CN)>c(HCOONH4) )相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中,c(NH4HCO3)>c(NH4CN)>c(HCOONH4) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列有关说法正确的是
| A.某温度下,弱酸的酸性:HA>HB,则等浓度的NaA和NaB溶液中离子总浓度前者小 |
B.常温下,将 氨水与 氨水与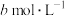 盐酸等体积混合,所得溶液pH=7,则 盐酸等体积混合,所得溶液pH=7,则 的电离常数 的电离常数 (忽略溶液混合时体积的变化) (忽略溶液混合时体积的变化) |
C.等浓度的①Na2C2O4溶液、②NaHC2O4溶液、③H2C2O4溶液中, 由大到小的顺序为①>③>② 由大到小的顺序为①>③>② |
D.等浓度的HCN和NaCN的混合溶液显碱性,则溶液中 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】部分弱电解质在常温下的电离平衡常数如表:
下列说法错误的是
| 弱电解质 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 | Ka = 1.8 ×10-4 | Ka =4.9 ×10-10 | Ka1=4.3 ×10-7 Ka2 = 5.6 ×10-11 |
A.结合H+的能力: >CN-> >CN-> >HCOO- >HCOO- |
| B.向NaCN溶液中通入少量CO2,所发生反应的化学方程式为CO2+H2O+2NaCN =Na2CO3+2HCN |
| C.pH=3 的盐酸与pH=11的氨水混合,若溶液显中性,则V(盐酸) >V( 氨水) |
| D.等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者大于后者 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】已知某酸H2A在水中存在下列电离:①H2A=H++HA- ②HA- H++A2-,下列说法一定正确的是
H++A2-,下列说法一定正确的是
 H++A2-,下列说法一定正确的是
H++A2-,下列说法一定正确的是| A.Na2A溶液中一定有:c(OH-)= c(H+)+c(HA-) |
| B.Na2A溶液呈碱性,NaHA溶液可能酸性可能呈碱性 |
| C.Na2A溶液中一定有c(Na+)+c(H+)= c(OH-)+c(A2-) +c(HA-) |
| D.NaHA溶液一定有c(Na+)>c(HA-) >c(OH-)>c(H2A) >c(H+) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】25℃时,向Na2CO3溶液中滴入盐酸,混合溶液的pH与离子浓度变化的关系如图所示。
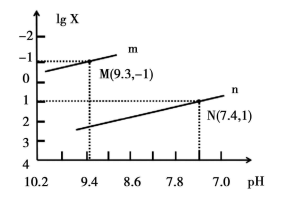
已知:lgX=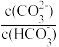 或
或 ,lg2=0.3,lg3=0.5。下列叙述正确的是
,lg2=0.3,lg3=0.5。下列叙述正确的是

已知:lgX=
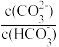 或
或 ,lg2=0.3,lg3=0.5。下列叙述正确的是
,lg2=0.3,lg3=0.5。下列叙述正确的是A.曲线m表示pH与 的变化关系 的变化关系 |
B.当溶液呈中性时,c(Na+)=c(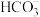 )+2c( )+2c(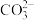 ) ) |
C.M点的溶液中:c(Na+)>c(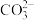 )>c( )>c(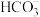 )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
D.25℃时,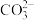 +H2O +H2O  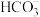 + OH-的平衡常数为2.0×10-4 + OH-的平衡常数为2.0×10-4 |
您最近一年使用:0次

 气体,溶液中
气体,溶液中 的物质的量与通入
的物质的量与通入
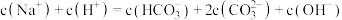
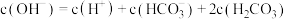
 的醋酸溶液中加入少量
的醋酸溶液中加入少量 的稀盐酸,溶液的pH会变小
的稀盐酸,溶液的pH会变小 和NaClO溶液中离子总数,前者大于后者
和NaClO溶液中离子总数,前者大于后者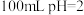 的新制氯水中:
的新制氯水中: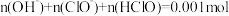
 溶液的pH一定比HClO溶液的pH小
溶液的pH一定比HClO溶液的pH小

