常温下,滴有两滴酚酞溶液的Na2CO3溶液中存在CO +H2O⇌HCO
+H2O⇌HCO +OH-平衡,溶液呈红色,下列说法不正确的是
+OH-平衡,溶液呈红色,下列说法不正确的是
 +H2O⇌HCO
+H2O⇌HCO +OH-平衡,溶液呈红色,下列说法不正确的是
+OH-平衡,溶液呈红色,下列说法不正确的是A.稀释溶液, 增大 增大 |
| B.通入CO2,或者加入少量氯化铵溶液,溶液pH均减小 |
| C.升高温度,红色变深,平衡常数增大 |
D.加入NaOH固体,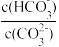 减小 减小 |
2021高三·全国·专题练习 查看更多[8]
陕西省/渭南市蒲城县尧山中学2023-2024学年高二上学期第三次月考化学试题新疆乌鲁木齐市第一中学2022-2023学年高二上学期期中考试化学试题(已下线)必刷卷03-2022年高考化学考前信息必刷卷(广东专用)2021年广东省高考化学试卷变式题1-10题(已下线)3.3.2 影响盐类水解的因素-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)专题26 盐类的水解(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练(已下线)第三章第三节 盐类的水解(第1课时 盐类的水解)(备作业)-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)(已下线)课时42 盐类的水解影响因素及应用-2022年高考化学一轮复习小题多维练(全国通用)
更新时间:2021-09-05 08:47:36
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】室温下向10 mL 0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是( )


| A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA) |
| B.a点溶液蒸发(不考虑溶质析出)c(Na+)/c(A-)增大 |
| C.pH=7时,c(Na+)=c(A-)+c(HA) |
| D.b点所示溶液中c(A-)>c(HA) |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于电解质溶液的叙述正确的是( )
| A.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| B.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| C.室温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH小 |
| D.室温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序为c(Cl-) = c(NH4+)>c(H+)=c(OH-) |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知醋酸、醋酸根离子在溶液中存在下列平衡及其对应的平衡常数:
CH3COOH CH3COO-+H+ K1=1.75×10-5
CH3COO-+H+ K1=1.75×10-5
CH3COO-+H2O CH3COOH+OH- K2=5.71×10-10
CH3COOH+OH- K2=5.71×10-10
常温下,将等体积、等物质的量浓度的醋酸和醋酸钠溶液混合,下列叙述正确的是( )
CH3COOH
 CH3COO-+H+ K1=1.75×10-5
CH3COO-+H+ K1=1.75×10-5 CH3COO-+H2O
 CH3COOH+OH- K2=5.71×10-10
CH3COOH+OH- K2=5.71×10-10 常温下,将等体积、等物质的量浓度的醋酸和醋酸钠溶液混合,下列叙述正确的是( )
| A.对混合溶液进行加热,K1增大、K2减小 |
| B.混合溶液的pH>7 |
| C.混合溶液中c(CH3COO-)>c(Na+) |
| D.温度不变,若在混合溶液中加入少量NaOH固体,c(CH3COO-)减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,将一定浓度的HA和HB分别与0.10 mol·L-1的NaOH溶液等体积混合,实验记录如下表:

下列说法中正确的是

下列说法中正确的是
| A.HA是强酸,HB是弱酸 |
B.升高温度,溶液②中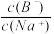 增大 增大 |
| C.溶液①中离子浓度的关系:c(A-)>c(Na+)>c(OH-)>c(H+) |
| D.溶液②中离子浓度的关系:c(Na+)+c(H+)+c(B-)=0.12 mol·L-1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温条件下,向 浓度均为
浓度均为 的
的 和
和 混合溶液中逐滴加入
混合溶液中逐滴加入 某一元碱
某一元碱 溶液,溶液的导电能力随
溶液,溶液的导电能力随 溶液加入量的变化如图所示(忽略溶液混合时的体积变化)。下列说法正确的是
溶液加入量的变化如图所示(忽略溶液混合时的体积变化)。下列说法正确的是

 浓度均为
浓度均为 的
的 和
和 混合溶液中逐滴加入
混合溶液中逐滴加入 某一元碱
某一元碱 溶液,溶液的导电能力随
溶液,溶液的导电能力随 溶液加入量的变化如图所示(忽略溶液混合时的体积变化)。下列说法正确的是
溶液加入量的变化如图所示(忽略溶液混合时的体积变化)。下列说法正确的是
A. 是强碱 是强碱 |
B.b点溶液中,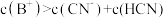 |
C.若c点溶液中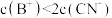 ,则 ,则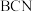 溶液显碱性 溶液显碱性 |
D.滴加 溶液过程中,水的电离程度先增大后减小 溶液过程中,水的电离程度先增大后减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
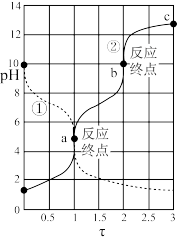
【推荐1】25℃时,0. 100 mol/L二元弱酸H2A(或其钠盐)用相同浓度的NaOH溶液(或盐酸)滴定,其pH与滴定分数τ(τ= 或
或  的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
 或
或  的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
| A.曲线①表示盐酸滴定Na2A溶液 |
| B.25℃时,Ka2(H2A)=1.0×10-10 |
C.溶液中:a点 比b点 比b点 大 大 |
| D.c点溶液中:c(Na+)>c(OH-)>c(A2-) |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,一元弱碱甲胺(CH3NH2)的电离常数Kb=4.0×10-4(lg5约为0.7)。电解质溶液的电导率与离子浓度有关,电导率越大,溶液的导电能力越强。常温下,用0.02mol/L盐酸滴定20.00mL等浓度的CH3NH2溶液,利用传感器测得滴定过程中溶液的电导率如图。下列推断正确的是


| A.F、G两点水的电离程度:F<G |
B.G点溶液4c( )+4c(CH3NH2)=5c(Cl-) )+4c(CH3NH2)=5c(Cl-) |
| C.滴定过程中可以选择酚酞做指示剂 |
| D.常温下,F点对应的溶液的pH≈6.3 |
您最近半年使用:0次


 和乙二胺(
和乙二胺( )溶液中各组分的百分含量随溶液pH的变化曲线(25℃)。
)溶液中各组分的百分含量随溶液pH的变化曲线(25℃)。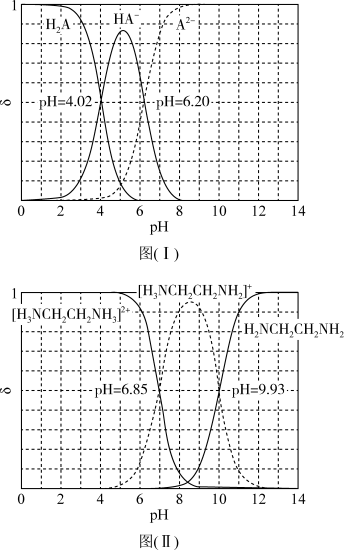
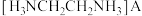 溶液显碱性
溶液显碱性
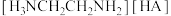 溶液中通入一定量的HCl气体,则
溶液中通入一定量的HCl气体,则 可能增大也可能减小
可能增大也可能减小

