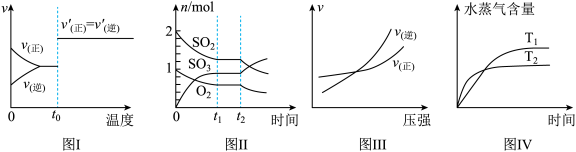
反应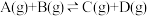 过程中的能量变化如图所示,下列说法正确的是
过程中的能量变化如图所示,下列说法正确的是
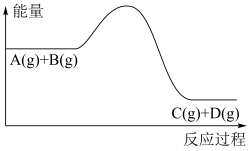
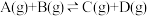 过程中的能量变化如图所示,下列说法正确的是
过程中的能量变化如图所示,下列说法正确的是
| A.该反应的逆反应为放热反应 |
| B.升高温度,利于A的转化率增大 |
| C.加入催化剂时,该反应的反应热发生改变 |
| D.增大压强,能够加快反应达到平衡状态的速率 |
更新时间:2021/10/13 15:25:35
|
相似题推荐
单选题-单题
|
适中
(0.65)
解题方法
【推荐1】中国努力2060年前实现碳中和,碳中和是指CO2的排放总量和减少总量相当。下列说法不正确的是
| A.可利用CaO或氨水捕集废气中的CO2 |
| B.积极鼓励植树造林,降低空气中CO2含量 |
| C.研发新型催化剂将CO2分解成碳和O2,同时放出热量 |
| D.一定条件下,将CO2转化为CH3OH,实现CO2的资源化利用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下图是使用不同催化剂(NiPc和CoPe)时转化过程中的能量变化,下列说法不合理的是
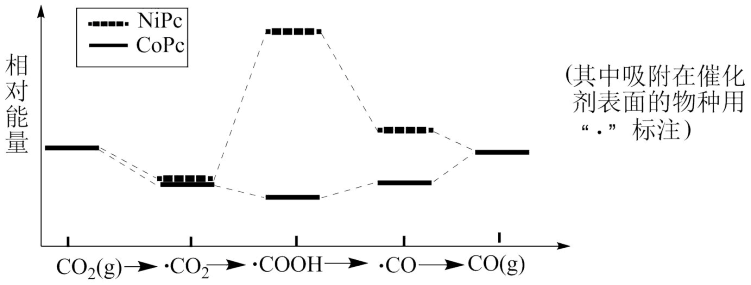

| A.·CO2经还原反应得到·COOH |
| B.该研究成果将有利于缓解温室效应,并解决能源转化问题 |
| C.相同基团的物种分别吸附在NiPc和CoPe表面,其能量可能不同 |
| D.转化过程中有共价键形成 |
您最近一年使用:0次
【推荐3】HBr被O2氧化依次由如下Ⅰ、Ⅱ、Ⅲ三步反应组成,1 mol HBr被氧化为Br2放出12.67 kJ热量,其能量与反应过程曲线如图所示。
(Ⅱ)HOOBr(g)+HBr(g)=2HOBr(g)
(Ⅲ)HOBr(g)+HBr(g)=H2O(g)+Br2(g)
下列说法中正确的是
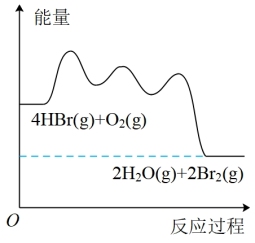
(Ⅱ)HOOBr(g)+HBr(g)=2HOBr(g)
(Ⅲ)HOBr(g)+HBr(g)=H2O(g)+Br2(g)
下列说法中正确的是
| A.三步反应均为放热反应 |
| B.步骤(Ⅰ)的反应速率最慢 |
| C.步骤(Ⅰ)中HOOBr比HBr和O2稳定 |
| D.4HBr(g)+O2(g)=2H2O(g)+2Br2(g)完全反应放出12.67 kJ的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列生产或实验事实引出的结论错误 的是
选项 | 生产或实验事实 | 结论 |
A | 其他条件相同,铁片和稀硫酸反应,适当升高溶液的温度,单位时间内产生的气泡增多 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
B | 在容积可变的密闭容器中发生反应:2NH3(g) N2H4(l)+H2(g),把容积的体积缩小一半 N2H4(l)+H2(g),把容积的体积缩小一半 | 正反应速率加快,逆反应速率减慢 |
C | Si与H2高温时反应,S与H2加热能反应 | P与H2在高温时能反应 |
D | A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】实验室用下列四种硫酸分别与锌粒制备H2 ,其中反应速率最快的是
| A.10℃ 10mL 3mol/L的硫酸 | B.10℃ 20mL 1mol/L的硫酸 |
| C.20℃ 10mL 3mol/L的硫酸 | D.20℃ 20mL 18.4 mol/L的硫酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列不能用勒夏特列原理解释的事实是
| A.红棕色的NO2加压后颜色先变深后变浅 |
| B.黄绿色的氯水光照后颜色变浅 |
| C.盐碱地(含较多NaCl、Na2CO3)通过施加适量的石膏(CaSO4•H2O),可以降低土壤碱性 |
| D.500 ℃左右比室温更有利于合成氨反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】含氮化合物的用途广泛。 下图表示两个常见固氮反应的平衡常数的对数值(lgK)与温度的关系:①N2+3H2⇌2NH3;②N2+O2⇌2NO。根据图中的数据判断下列说法正确的是
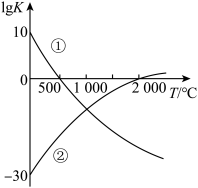

| A.反应①和②均为放热反应 |
| B.升高温度,反应①的反应速率减小 |
| C.常温下,利用反应①固氮和利用反应②固氮反应程度相差很大 |
| D.曲线的交点表示反应①和反应②体系中 N2的浓度一定相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验操作和实验现象不相匹配的是
| 实验操作 | 实验现象 | |
| A | 将一小块钠投入硫酸铜溶液中 | 有气泡冒出,产生蓝色沉淀 |
| B | 将Na2O2加入适量水中,滴入几滴酚酞 | 溶液先变红后褪色,有气泡产生 |
| C | 向重铬酸钾溶液中滴加几滴浓硫酸 | 随着浓硫酸加入,溶液颜色变浅 |
| D | 将铜丝在盛满氯气的烧瓶中点燃 | 烧瓶中充满棕黄色的烟 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在某2 L恒容密闭容器中充入2 mol X(g)和1 mol Y(g)发生反应:2X(g)+Y(g) 3Z(g) ΔH,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g) ΔH,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
 3Z(g) ΔH,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g) ΔH,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
| A.M点时Y的转化率最大 |
| B.升高温度,平衡向逆反应方向移动 |
| C.若反应开始时加入催化剂,达到平衡时Z的体积分数将比未加入时大 |
| D.W、M两点Y的正反应速率相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】反应N2O4(g)⇌2NO2(g) ΔH=+57 kJ·mol-1在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示,下列说法正确的是( )。
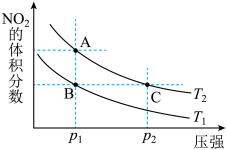

| A.A、C两点的反应速率:A>C |
| B.A、C两点气体的颜色:A深,C浅 |
| C.由状态B到状态A,可以用加热的方法 |
| D.若p2>p1,则化学平衡常数KA>KC |
您最近一年使用:0次