请按要求填写下列方程式:
(1)请写出下列物质的电离方程式(分步的所有步都写):
NH3•H2O:___________
H2CO3:___________
(2)请写出下列盐的水解离子方程式(分步的所有步都写):
AlCl3:___________
CH3COONa:___________
Na2S:___________
(1)请写出下列物质的电离方程式(分步的所有步都写):
NH3•H2O:
H2CO3:
(2)请写出下列盐的水解离子方程式(分步的所有步都写):
AlCl3:
CH3COONa:
Na2S:
更新时间:2021-11-08 15:00:22
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】乙二酸(H2C2O4)俗称草酸,在实验研究和化学工业中应用广泛。
(1)室温下,测得0.1mol/L H2C2O4溶液的pH=1.3,写出草酸的电离方程式_____ 。
(2)草酸溶液中各粒子的物质的量分数随溶液pH变化关系如下图所示:
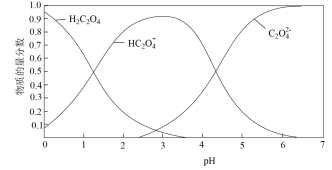
①向草酸溶液中滴加KOH溶液至pH=2.5时发生的主要反应的离子方程式是_____ 。②0.1mol/LKHC2O4溶液中,下列粒子浓度关系正确的是_____ (填序号)。
a.
b.
c.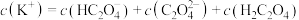
(1)室温下,测得0.1mol/L H2C2O4溶液的pH=1.3,写出草酸的电离方程式
(2)草酸溶液中各粒子的物质的量分数随溶液pH变化关系如下图所示:

①向草酸溶液中滴加KOH溶液至pH=2.5时发生的主要反应的离子方程式是
a.

b.

c.
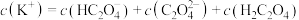
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】今有 、
、 、
、 三种弱酸,根据强酸制弱酸的反应规律,它们之间发生下列反应:
三种弱酸,根据强酸制弱酸的反应规律,它们之间发生下列反应: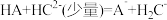 ;
;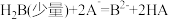 ;
; ,回答下列问题:
,回答下列问题:
(1)相同条件下, 、
、 、
、 三种酸中,酸性最强的是
三种酸中,酸性最强的是___________ ;
(2)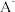 、
、 、
、 、
、 、
、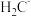 、
、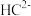 六种离子中,最容易结合质子
六种离子中,最容易结合质子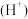 的是
的是___________ ;最难结合质子的是___________ ;
(3)完成下列反应的离子方程式
①
___________ ;
②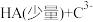
___________ 。
 、
、 、
、 三种弱酸,根据强酸制弱酸的反应规律,它们之间发生下列反应:
三种弱酸,根据强酸制弱酸的反应规律,它们之间发生下列反应: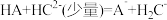 ;
;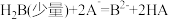 ;
; ,回答下列问题:
,回答下列问题:(1)相同条件下,
 、
、 、
、 三种酸中,酸性最强的是
三种酸中,酸性最强的是(2)
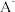 、
、 、
、 、
、 、
、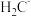 、
、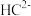 六种离子中,最容易结合质子
六种离子中,最容易结合质子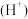 的是
的是(3)完成下列反应的离子方程式
①

②
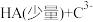
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求书写下列方程式:
(1)水溶液中的电离方程式:
①硫酸氢钠_______ 。
②一水合氨_______ 。
③碳酸_______ 。
(2)离子方程式:
①澄清石灰水与过量的碳酸氢钠溶液混合_______ 。
②碳酸氢钠溶液和氢氧化钠溶液混合_______ 。
(3)已知298 K、101 kPa时,①N2(g)+2O2(g) = 2 NO2(g);△H=+67.7 kJ·mol-1,
②N2H4(g)+O2(g) = N2(g)+2H2O (g);△H=-534 kJ·mol-1,
根据盖斯定律写出肼(N2H4)与NO2完全反应生成氮气和气态水的热化学方程式_______ 。
(1)水溶液中的电离方程式:
①硫酸氢钠
②一水合氨
③碳酸
(2)离子方程式:
①澄清石灰水与过量的碳酸氢钠溶液混合
②碳酸氢钠溶液和氢氧化钠溶液混合
(3)已知298 K、101 kPa时,①N2(g)+2O2(g) = 2 NO2(g);△H=+67.7 kJ·mol-1,
②N2H4(g)+O2(g) = N2(g)+2H2O (g);△H=-534 kJ·mol-1,
根据盖斯定律写出肼(N2H4)与NO2完全反应生成氮气和气态水的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有下列化合物①NaCl、②NaOH、③HCl、④NH4Cl、⑤CH3COONa、⑥CH3COOH、⑦NH3·H2O、⑧H2O,回答问题:
(1)NH4Cl 溶液显_______ 性,用离子方程式表示_______ 。
(2)常温下,pH=10 的 CH3COONa 溶液中,水电离出来的 c(OH- )为_______ mol/L,在 pH=3 的CH3COOH 溶液中水电离出来的 c(H+ )为_______ mol/L。
(3)已知水中存在如下平衡:H2O+H2O⇌H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,选择的方法是_______ 。
A.向水中加入 NaHSO4 固体 B.向水中加入 Na2CO3 固体
C.加热至 100℃ D.向水中加入(NH4)2SO4 固体
(4) 常温下,将 pH=12 的 NaOH 和氨水分别加水稀释 100 倍后,稀释后 NaOH 的 pH_______ 10, 氨水的 pH_______ 10(填“>”“<”或“=”)
(5)等物质的量浓度的④NH4Cl、⑤CH3COONa、⑦NH3·H2O溶液中 浓度由大到小的顺序是
浓度由大到小的顺序是____________ (填序号)
(1)NH4Cl 溶液显
(2)常温下,pH=10 的 CH3COONa 溶液中,水电离出来的 c(OH- )为
(3)已知水中存在如下平衡:H2O+H2O⇌H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,选择的方法是
A.向水中加入 NaHSO4 固体 B.向水中加入 Na2CO3 固体
C.加热至 100℃ D.向水中加入(NH4)2SO4 固体
(4) 常温下,将 pH=12 的 NaOH 和氨水分别加水稀释 100 倍后,稀释后 NaOH 的 pH
(5)等物质的量浓度的④NH4Cl、⑤CH3COONa、⑦NH3·H2O溶液中
 浓度由大到小的顺序是
浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】依据所学知识回答问题:
(1)液态 是一种似水溶剂,可以微弱电离:
是一种似水溶剂,可以微弱电离: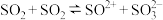 ,在液态
,在液态 中,视
中,视 为酸,
为酸,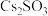 为碱,试写出二者在液态
为碱,试写出二者在液态 体系中发生反应的化学方程式:
体系中发生反应的化学方程式:___________ 。
(2)盐类水解的实质就是盐产生的阴阳离子与水电离出的 或
或 结合的过程,下列物质与水反应和盐类水解类似,写出相应的化学方程式:
结合的过程,下列物质与水反应和盐类水解类似,写出相应的化学方程式:
 与水反应:
与水反应:___________ ;
 与热水反应:
与热水反应:___________ 。
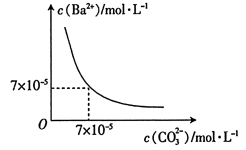
(3)常温下,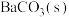 在水中的溶解平衡曲线如图所示,则该温度下,
在水中的溶解平衡曲线如图所示,则该温度下,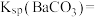
___________ ;将 的
的 溶液与
溶液与 的
的 溶液等体积混合后,混合溶液中
溶液等体积混合后,混合溶液中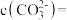
___________ 。
(1)液态
 是一种似水溶剂,可以微弱电离:
是一种似水溶剂,可以微弱电离: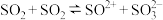 ,在液态
,在液态 中,视
中,视 为酸,
为酸,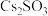 为碱,试写出二者在液态
为碱,试写出二者在液态 体系中发生反应的化学方程式:
体系中发生反应的化学方程式:(2)盐类水解的实质就是盐产生的阴阳离子与水电离出的
 或
或 结合的过程,下列物质与水反应和盐类水解类似,写出相应的化学方程式:
结合的过程,下列物质与水反应和盐类水解类似,写出相应的化学方程式: 与水反应:
与水反应: 与热水反应:
与热水反应:(3)常温下,
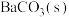 在水中的溶解平衡曲线如图所示,则该温度下,
在水中的溶解平衡曲线如图所示,则该温度下,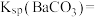
 的
的 溶液与
溶液与 的
的 溶液等体积混合后,混合溶液中
溶液等体积混合后,混合溶液中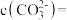

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在日常生活中,为了达到更好的清洁效果,经常有人会将洁厕液(含有盐酸)与84消毒液混合使用,从而会发生引发中毒的事故。
(1)两种日化产品主要成分中都含有氯元素,该元素在元素周期表中位置是_______ 。
(2)84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式:_______ 。
(3)洁厕灵的主要成分是HCl。下列关于卤化氢的性质比较中错误的是_______。
(4)常温下,0.1mol/L的NaClO溶液的PH=9.7,原因_______ 。常温下HClO的电离平衡常数为_______ 。洁厕液与84消毒液混合后会生成有毒的氯气。写出该反应的离子方程式_______ 。
(5)高铁酸钾是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产,反应原理为:
①在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为_______ 。
②Na2FeO4与KOH反应生成K2FeO4:Na2FeO4+2KOH=K2FeO4+2NaOH
K2FeO4在水溶液中易水解:4 +10H2O⇌4Fe(OH)3+8OH-+3O2,在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
+10H2O⇌4Fe(OH)3+8OH-+3O2,在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用_______ 溶液(填序号)
a.水 b.NH4Cl、异丙醇 c.Fe(NO3)3、异丙醇 d.CH3COONa、异丙醇
(6)消毒效率是物质单位质量得到的电子数,则Cl2与NaClO两种消毒剂的消毒效率之比为__ 。
(1)两种日化产品主要成分中都含有氯元素,该元素在元素周期表中位置是
(2)84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式:
(3)洁厕灵的主要成分是HCl。下列关于卤化氢的性质比较中错误的是_______。
| A.酸性:HF>HCl>HBr>HI | B.键能:H—F>H—Cl>H—Br>H—I |
| C.熔点:HF<HCl<HBr<HI | D.还原性:HF<HCl<HBr<HI |
(5)高铁酸钾是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产,反应原理为:
①在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为
②Na2FeO4与KOH反应生成K2FeO4:Na2FeO4+2KOH=K2FeO4+2NaOH
K2FeO4在水溶液中易水解:4
 +10H2O⇌4Fe(OH)3+8OH-+3O2,在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
+10H2O⇌4Fe(OH)3+8OH-+3O2,在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用a.水 b.NH4Cl、异丙醇 c.Fe(NO3)3、异丙醇 d.CH3COONa、异丙醇
(6)消毒效率是物质单位质量得到的电子数,则Cl2与NaClO两种消毒剂的消毒效率之比为
您最近一年使用:0次



