已知常温下 ,
,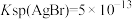 ,下列有关说法不正确的是
,下列有关说法不正确的是
 ,
,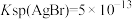 ,下列有关说法不正确的是
,下列有关说法不正确的是A.在饱和AgCl、AgBr的混合溶液中: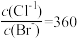 |
| B.AgCl在水中溶解度及Ksp均比在NaCl溶液中的小 |
| C.向AgCl悬浊液中滴加浓NaBr溶液会产生淡黄色沉淀 |
D.欲用1L NaCl溶液将0.01mol AgBr全部转化为AgCl,则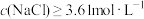 |
更新时间:2021-11-15 21:09:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在恒容密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)⇌Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
下列说法正确的是
| 温度/℃ | 25 | 80 | 220 |
| 平衡常数 | 5×104 | 2 | 2× 10-5 |
下列说法正确的是
| A.由表中数据分析知生成Ni(CO)4(g)的反应为吸热反应 |
| B.25℃时反应Ni(CO)4(g)⇌Ni(s)+4CO(g)的平衡常数为2×10-4 |
| C.80C℃达到平衡时,测得c(CO)=1mol·L-1,则c[Ni(CO)4]=2mol·L-1 |
| D.80℃,若测得Ni(CO)4、CO浓度均为0.5mol·L-1,则此时v(正)>v(逆) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】T℃,体积均为1L的甲、乙、丙容器中发生反应: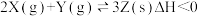 ,
,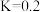 。t1时刻容器中X、Y与Z的物质的量如下表,下列说法正确的是
。t1时刻容器中X、Y与Z的物质的量如下表,下列说法正确的是
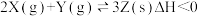 ,
,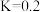 。t1时刻容器中X、Y与Z的物质的量如下表,下列说法正确的是
。t1时刻容器中X、Y与Z的物质的量如下表,下列说法正确的是| X | Y | Z | |
| 甲 |  |  |  |
| 乙 |  |  |  |
| 丙 |  |  |  |
A.甲容器中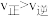 |
B.乙容器若降低温度,达到平衡时 可能为 可能为 |
| C.乙、丙容器达到平衡后,X的浓度不相等 |
| D.若丙容器中X的体积分数不变,则该反应已达平衡 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】以MnO2为原料发生反应制得的MnCl2溶液,当中常含有Cu2+、Pb2+、Cd2+等金属离子,通过添加过量难溶电解质MnS,可使这些金属离子形成硫化物沉淀,经过滤除去包括MnS在内的沉淀,再经蒸发、结晶,可得纯净的MnCl2.根据上述实验事实,下列分析正确的是
| A.MnS的溶解度小于CuS、PbS、CdS等硫化物的溶解度 |
| B.除杂试剂MnS也可用Na2S替代 |
| C.MnS与Cu2+反应的离子方程式是Cu2++S2-=CuS↓ |
| D.整个过程中涉及的反应类型有氧化还原反应和复分解反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】实验小组设计实验除去粗盐溶液中的Ca2+、Mg2+、SO 并进行定性检验。
并进行定性检验。
已知:Ksp[Mg(OH)2]=5.6×10-12,Ksp(BaSO4)=1.1×10-10,Ksp(BaCO3)=2.6×10-9。不正确 的是
 并进行定性检验。
并进行定性检验。已知:Ksp[Mg(OH)2]=5.6×10-12,Ksp(BaSO4)=1.1×10-10,Ksp(BaCO3)=2.6×10-9。

| A.调节溶液的pH>12,可使滤液中c(Mg2+)<1×10-5mol/L |
B.加入Na2CO3溶液发生的反应是Ba2++CO =BaCO3↓、Ca2++CO =BaCO3↓、Ca2++CO =CaCO3↓ =CaCO3↓ |
C.加入盐酸发生的反应是2H++CO =CO2↑+H2O、H++OH-=H2O =CO2↑+H2O、H++OH-=H2O |
| D.若步骤①加入BaCl2溶液后进行过滤,可以避免白色沉淀M的生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作和现象不相符的是
| 选项 | 实验操作 | 现象 |
| A | 向溴的氯仿溶液中通入足量乙烯 | 溴的氯仿溶液颜色逐渐变浅,最终变为无色 |
| B | 向淀粉溶液中先加入足量稀硫酸,再加入少量新制氢氧化铜悬浊液,加热 | 产生砖红色沉淀 |
| C | 向盛有大量水的烧杯中加入少量钠块 | 钠块熔化成银白色小球 |
| D | 常温下,向AgCl浊液中加入KI浓溶液,振荡已知:[Ksp(AgCl)>Ksp(AgI)] | 白色浊液变成淡黄色浊液(或沉淀) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列解释事实的离子方程式不正确的是( )
| A.铝片放入NaOH溶液中有气体产生:2Al+2OH﹣+2H2O=2AlO2−+3H2↑ |
| B.向K2Cr2O7溶液中滴加少量浓H2SO4,溶液橙色加深:Cr2O72−(橙色)+H2O⇌2CrO42−(黄色)+2H+ |
| C.向Na2SiO3溶液中通入过量CO2制备硅酸凝胶:SiO32- +CO2+H2O=H2SiO3(胶体)+ CO32- |
D.用Na2CO3溶液浸泡锅炉水垢(含CaSO4):CaSO4+CO32- CaCO3+SO42- CaCO3+SO42- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,将一定浓度的氨水逐滴加入
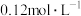
 溶液中,该过程中溶液
溶液中,该过程中溶液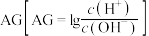 与加入氨水体积V的关系如图所示,已知e点对应的溶液迅速由浑浊变澄清,且此时溶液中的
与加入氨水体积V的关系如图所示,已知e点对应的溶液迅速由浑浊变澄清,且此时溶液中的 与
与 均约为
均约为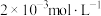 ,下列叙述错误的是
,下列叙述错误的是

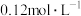
 溶液中,该过程中溶液
溶液中,该过程中溶液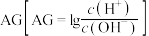 与加入氨水体积V的关系如图所示,已知e点对应的溶液迅速由浑浊变澄清,且此时溶液中的
与加入氨水体积V的关系如图所示,已知e点对应的溶液迅速由浑浊变澄清,且此时溶液中的 与
与 均约为
均约为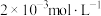 ,下列叙述错误的是
,下列叙述错误的是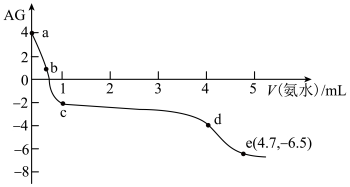
A.a点对应溶液中由水电离出的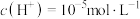 |
B.b点对应溶液中: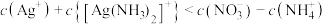 |
C.由e点可知,反应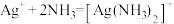 的平衡常数约为 的平衡常数约为 |
| D.最好选择d~e段溶液与葡萄糖等含有醛基的有机物发生银镜反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】H2A是一种二元弱酸,H2A由于与空气中的某种成分作用其浓度基本保持不变。某天然水体中lgc(X)(X为H2A、HA-、A2-、M2+)与pH的关系如图所示。下列说法正确的是
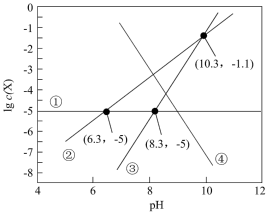

| A.H2A为H2SO3 |
| B.曲线②代表A2- |
| C.Ksp(MA)的数量级约为10-9 |
| D.H2A的二级电离常数为10-8.3 |
您最近一年使用:0次
【推荐3】黄铁矿(主要成分FeS2),在空气中会被缓慢氧化,氧化过程如图所示。下列说法正确的是
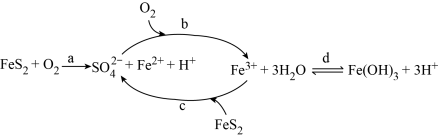

| A.发生反应a时,每1 mol FeS2被还原,转移14 mol e- |
| B.已知25°C时,Ksp[Fe(OH)3]=2.79 ×10-39,则该温度下d逆反应的平衡常数为K=2.79 ×103 |
C.c发生反应的离子方程式为:4Fe3++FeS2+8H2O=5Fe2++2 +16H+ +16H+ |
| D.为了验证b过程反应后溶液中是否含Fe2+,可选用氯水和KSCN溶液 |
您最近一年使用:0次

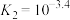
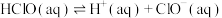
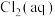 、
、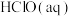 和
和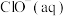 分别在三者总量中所占物质的量分数
分别在三者总量中所占物质的量分数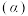 随pH变化的关系如图所示。下列表述正确的是
随pH变化的关系如图所示。下列表述正确的是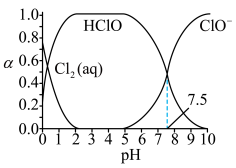
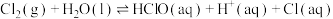
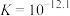
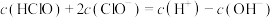
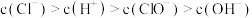
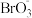 )
)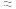 0.025mol/L
0.025mol/L 10-4
10-4

