向绝热恒容密闭容器中通入 和
和 ,一定条件下使反应
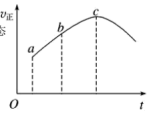
,一定条件下使反应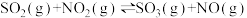 达到平衡,在此过程中正反应速率随时间变化的曲线如图所示。由图得出的结论正确的是
达到平衡,在此过程中正反应速率随时间变化的曲线如图所示。由图得出的结论正确的是
 和
和 ,一定条件下使反应
,一定条件下使反应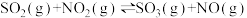 达到平衡,在此过程中正反应速率随时间变化的曲线如图所示。由图得出的结论正确的是
达到平衡,在此过程中正反应速率随时间变化的曲线如图所示。由图得出的结论正确的是
| A.反应在a、b点均未建立平衡,c点恰好达到平衡状态 |
| B.反应物浓度:a点小于b点 |
| C.反应物的总能量低于生成物的总能量 |
D.若在恒温恒容密闭容器中,以相同的投料进行该反应,平衡时 转化率大于绝热恒容密闭容器中 转化率大于绝热恒容密闭容器中 转化率 转化率 |
更新时间:2021-11-17 00:09:51
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】知:CH4(g)+2H2S(g)⇌CS2(g)+4H2(g)。向恒容密闭容器中充入0.1molCH4和0.2molH2S,测得平衡时体系中各物质的物质的量分数与温度的关系如图所示。

下列说法不正确的是

下列说法不正确的是
| A.该反应的ΔH>0 |
| B.X点CH4的转化率为20% |
| C.X点与Y点容器内压强比为51∶55 |
| D.维持Z点温度,向容器中再充入CH4、H2S、CS2、H2各0.1mol时v(正)<v(逆) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
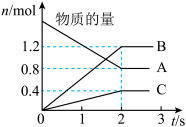
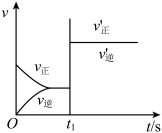
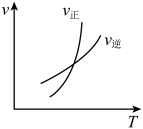
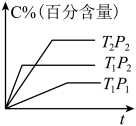
【推荐2】以下图像对应的叙述正确的是
 |  |  |  |
 |  |   |   |
| 甲 | 乙 | 丙 | 丁 |
| A.图丁:该正向反应在任何温度下都能自发进行 |
| B.图丙:对图中反应升高温度,该反应平衡常数减小 |
C.图乙: 时刻改变的条件只能是加入催化剂 时刻改变的条件只能是加入催化剂 |
D.图甲: 的平衡转化率为 的平衡转化率为 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】工业上用乙苯催化脱氢制取苯乙烯的反应如下: (g)
(g)
 (g)+H2(g)。现将 x mol乙苯蒸气通入体积可变的密闭容器中发生反应,维持体系总压强p总恒定。在某催化剂作用下,乙苯的平衡转化率随温度的变化如图所示。不考虑副反应,下列说法错误的是[已知:气体分压(p分)=气体总压(p总)×体积分数]
(g)+H2(g)。现将 x mol乙苯蒸气通入体积可变的密闭容器中发生反应,维持体系总压强p总恒定。在某催化剂作用下,乙苯的平衡转化率随温度的变化如图所示。不考虑副反应,下列说法错误的是[已知:气体分压(p分)=气体总压(p总)×体积分数]

 (g)
(g)
 (g)+H2(g)。现将 x mol乙苯蒸气通入体积可变的密闭容器中发生反应,维持体系总压强p总恒定。在某催化剂作用下,乙苯的平衡转化率随温度的变化如图所示。不考虑副反应,下列说法错误的是[已知:气体分压(p分)=气体总压(p总)×体积分数]
(g)+H2(g)。现将 x mol乙苯蒸气通入体积可变的密闭容器中发生反应,维持体系总压强p总恒定。在某催化剂作用下,乙苯的平衡转化率随温度的变化如图所示。不考虑副反应,下列说法错误的是[已知:气体分压(p分)=气体总压(p总)×体积分数]
| A.400℃时,再向体系中通入水蒸气,v正、v逆均减少,且乙苯的转化率升高 |
| B.500 ℃时,再向体系中通入 0.2 x mol乙苯,平衡时各物质的体积分数保持不变 |
C.500 ℃时,用平衡分压代替平衡浓度表示的化学平衡常数 |
| D.550℃时平衡体系中苯乙烯的体积分数是 450℃时的2.25 倍 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
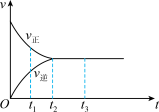
【推荐1】如图是可逆反应X2+3Y2  2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不正确的是
2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不正确的是
 2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不正确的是
2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不正确的是
| A.t1时,只有正方向反应 |
| B.t2~t3,反应仍在进行 |
| C.t2时,反应到达限度 |
| D.t2~t3,各物质的浓度不再发生变化 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】一定条件下,对于可逆反应:X(g)+3Y(g) 2Z(g),若 X、Y、Z 的起始浓度分别为 c1、c2、c3(均不为 0,单位 mol/L),达到平衡时,X、Y、Z 的浓度分别为 0.1 mol/L、0.3 mol/L、0.08mol/L,则下列判断不正确的是
2Z(g),若 X、Y、Z 的起始浓度分别为 c1、c2、c3(均不为 0,单位 mol/L),达到平衡时,X、Y、Z 的浓度分别为 0.1 mol/L、0.3 mol/L、0.08mol/L,则下列判断不正确的是
 2Z(g),若 X、Y、Z 的起始浓度分别为 c1、c2、c3(均不为 0,单位 mol/L),达到平衡时,X、Y、Z 的浓度分别为 0.1 mol/L、0.3 mol/L、0.08mol/L,则下列判断不正确的是
2Z(g),若 X、Y、Z 的起始浓度分别为 c1、c2、c3(均不为 0,单位 mol/L),达到平衡时,X、Y、Z 的浓度分别为 0.1 mol/L、0.3 mol/L、0.08mol/L,则下列判断不正确的是| A.c1∶c2=1∶3 | B.平衡时 Y 和 Z 的生成速率之比为 3∶2 |
| C.X、Y 的转化率之比等于 1:3 | D.c2 的取值范围为 0<c2<0.42 mol/L |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】温度为T时,在三个容积均为1L的恒容密闭容器中仅发生反应:2SO2(g)+O2(g) 2SO3(g) ΔH<0,达到平衡时,下列说法
2SO3(g) ΔH<0,达到平衡时,下列说法不正确 的是
 2SO3(g) ΔH<0,达到平衡时,下列说法
2SO3(g) ΔH<0,达到平衡时,下列说法| 容器 编号 | 容器类型 | 起始物质的量 / mol | 平衡时SO3的物质的量 / mol | ||
| SO2 | O2 | SO3 | |||
| I | 恒温恒容 | 2 | 1 | 0 | 1.8 |
| II | 恒温恒压 | 2 | 1 | 0 | a |
| III | 绝热恒容 | 0 | 0 | 2 | b |
| A.容器I中SO2的转化率小于容器II中SO2的转化率 |
| B.容器II的平衡常数大于容器III中的平衡常数 |
| C.平衡时SO3的物质的量:a>1.8、b>1.8 |
| D.若起始时向容器I中充入0.10 mol SO2(g)、0.20mol O2(g)和2.0 mol SO3(g),则此时v正<v逆 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在特制的密闭真空容器中加入一定量纯净的氨基甲酸铵固体(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g) ΔH>0。下列说法中正确的是
2NH3(g)+CO2(g) ΔH>0。下列说法中正确的是
 2NH3(g)+CO2(g) ΔH>0。下列说法中正确的是
2NH3(g)+CO2(g) ΔH>0。下列说法中正确的是| A.密闭容器中气体的平均相对分子质量不变则该反应达到平衡状态 |
| B.该反应在任何条件下都能自发进行 |
| C.再加入一定量氨基甲酸铵,可加快反应速率 |
| D.保持温度不变,压缩体积,达到新的平衡时,NH3的浓度不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】一定温度、体积的密闭容器中,可逆反应A(s)+3B(g) 2C(g)达到平衡时,下列说法能判断该反应达到平衡的是( )
2C(g)达到平衡时,下列说法能判断该反应达到平衡的是( )
①C的生成速率和C的分解速率相等
②单位时间内生成amolA,同时生成3amolB
③混合气体的密度不再变化
④混合气体的总压强不再变化
⑤A、B、C物质的量之比为1∶3∶2
⑥混合气体的平均相对分子质量不变
⑦容器中C的体积分数不变
 2C(g)达到平衡时,下列说法能判断该反应达到平衡的是( )
2C(g)达到平衡时,下列说法能判断该反应达到平衡的是( )①C的生成速率和C的分解速率相等
②单位时间内生成amolA,同时生成3amolB
③混合气体的密度不再变化
④混合气体的总压强不再变化
⑤A、B、C物质的量之比为1∶3∶2
⑥混合气体的平均相对分子质量不变
⑦容器中C的体积分数不变
| A.②④⑤⑦ | B.①③④⑥⑦ | C.①④⑥⑦ | D.①③④⑤ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】向一恒容密闭容器中加入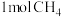 和一定量的
和一定量的 ,发生反应
,发生反应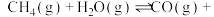
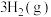 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比 随温度的变化曲线如图所示。下列说法正确的是
随温度的变化曲线如图所示。下列说法正确的是

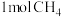 和一定量的
和一定量的 ,发生反应
,发生反应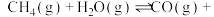
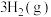 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比 随温度的变化曲线如图所示。下列说法正确的是
随温度的变化曲线如图所示。下列说法正确的是
A. |
B.反应速率: |
C.点a、b、c对应的平衡常数: |
D.反应温度为 ,当容器内压强不变时,反应达到平衡状态 ,当容器内压强不变时,反应达到平衡状态 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】对于可逆反应mA(s)+nB(g) eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
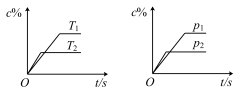
 eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
| A.达到平衡后,若使用催化剂,C的质量分数将增大 |
| B.达到平衡后,增加A的量有利于化学平衡向正方向移动 |
| C.化学方程式中n>e+f |
| D.达到平衡后,若升高温度,化学平衡向逆方向移动 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列关于各图的叙述正确的是
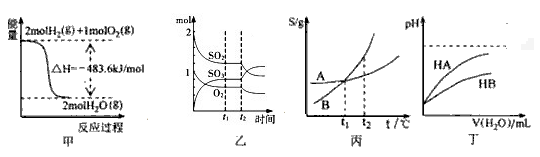

| A.图甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8 kJ•mol-1 |
B.图乙表示一定条件下进行的反应2SO2+O2 2SO3各成分的物质的量变化,t2时刻改变的条件一定是缩小容器体积 2SO3各成分的物质的量变化,t2时刻改变的条件一定是缩小容器体积 |
| C.图丙表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数ω(B)>ω(A) |
| D.图丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度的NaB溶液的pH |
您最近一年使用:0次




