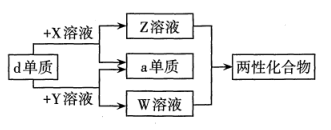
常温下,向20mL0.1mol•L﹣1CH3COOH溶液中逐滴加入0.1mol•L﹣1的NaOH溶液,溶液中由水电离出的OH﹣浓度在此滴定过程的变化如图所示。下列说法错误的是
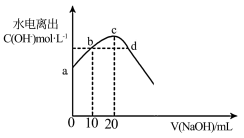

| A.a~d点,a点时水的电离受抑制最强 |
| B.b、c、d三点溶液中离子、分子种类相同 |
| C.c点表示酸碱恰好完全反应,溶液中c(OH﹣)=c(CH3COOH)+c(H+) |
| D.b、d两点溶液的pH相同 |
更新时间:2022/01/16 22:55:04
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】水的电离平衡曲线如图所示,下列说法正确的是


A.图中五点 间的关系:B>C>A=D=E 间的关系:B>C>A=D=E |
B.若从A点到C点,可采用温度不变时在水中加入适量 的方法 的方法 |
C.若从A点到D点,可采用在水中加入少量 的方法 的方法 |
D.若处在B点温度时,将 的硫酸与 的硫酸与 的 的 等体积混合后,溶液显中性 等体积混合后,溶液显中性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时,水中存在平衡: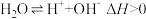 。下列叙述正确的是
。下列叙述正确的是
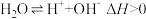 。下列叙述正确的是
。下列叙述正确的是A.向水中加入稀氨水,平衡逆向移动, 降低 降低 |
B.将水加热, 增大, 增大,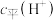 不变 不变 |
C.向水中加入少量 固体,平衡逆向移动, 固体,平衡逆向移动,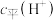 降低 降低 |
D.向水中加入少量固体 , ,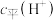 增大, 增大, 不变 不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
A.纯碱溶液中:c(Na+)+c(H+)=c( )+c( )+c( )+c(OH-) )+c(OH-) |
| B.0.2 mol/LCH3COOH溶液和0.1 mol/LNaOH溶液等体积混合:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH) |
| C.0.1 mol/LpH=4的NaHB的溶液中c(Na+)>c(HB-)>c(H2B)>c(B2-) |
| D.Na2CO3和NaHCO3溶液中,粒子种类不完全相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述错误的是
A. 稀溶液加水稀释,溶液的碱性减弱 稀溶液加水稀释,溶液的碱性减弱 |
| B.稀溶液中,盐的浓度越小,水解程度越大,其溶液酸性(或碱性)也越强 |
C.在滴有酚酞的 溶液中慢慢滴入 溶液中慢慢滴入 溶液,溶液的红色逐渐褪去 溶液,溶液的红色逐渐褪去 |
D.pH相等的① ② ② ③ ③ 溶液的物质的量浓度大小:①>②>③ 溶液的物质的量浓度大小:①>②>③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,向20ml0.1 的CH3COOH溶液中逐滴加入0.1
的CH3COOH溶液中逐滴加入0.1 NaOH溶液,pH随加入NaOH溶液体积的变化如图1,某时刻滴定管的读数如图2,下列说法错误的是
NaOH溶液,pH随加入NaOH溶液体积的变化如图1,某时刻滴定管的读数如图2,下列说法错误的是
 的CH3COOH溶液中逐滴加入0.1
的CH3COOH溶液中逐滴加入0.1 NaOH溶液,pH随加入NaOH溶液体积的变化如图1,某时刻滴定管的读数如图2,下列说法错误的是
NaOH溶液,pH随加入NaOH溶液体积的变化如图1,某时刻滴定管的读数如图2,下列说法错误的是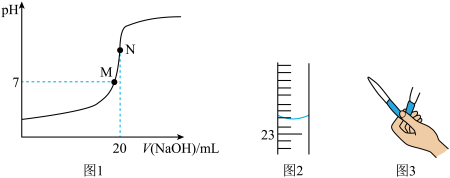
A.M点对应溶液: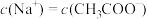 |
| B.N点水的电离程度大于M点 |
| C.图2所示液面读数为23.20mL |
| D.装NaOH标准液时,用图3所示方法排除滴定管内的气泡 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】 的
的 溶液用
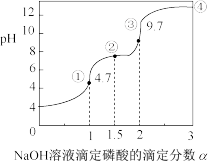
溶液用 的NaOH溶液进行滴定,其滴定曲线如图所示
的NaOH溶液进行滴定,其滴定曲线如图所示 已知:滴定分数
已知:滴定分数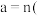 滴定液中溶质
滴定液中溶质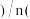 被滴定溶质
被滴定溶质 。下列说法正确的是
。下列说法正确的是
 的
的 溶液用
溶液用 的NaOH溶液进行滴定,其滴定曲线如图所示
的NaOH溶液进行滴定,其滴定曲线如图所示 已知:滴定分数
已知:滴定分数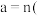 滴定液中溶质
滴定液中溶质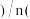 被滴定溶质
被滴定溶质 。下列说法正确的是
。下列说法正确的是
A. 时, 时,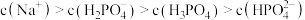 |
B.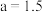 时, 时,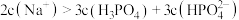 |
C. 时, 时,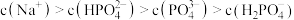 |
D. 时, 时,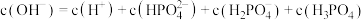 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】在某温度时,将x mol/L氨水滴入10 mL1.0 mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是
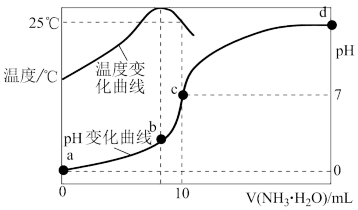

A.a点: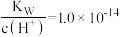 |
| B.氨水的浓度一定大于1.0 mol/L |
C.b~d点过程中离子浓度大小关系一定为 |
| D.b、c、d三点水的电离程度大小关系是c>b>d |
您最近一年使用:0次