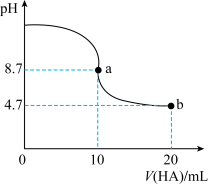
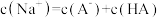下列有关电解质溶液的说法正确的是
A.常温下 的HA溶液与 的HA溶液与 的BOH溶液等体积混合,溶液 的BOH溶液等体积混合,溶液 ,则BOH为强碱 ,则BOH为强碱 |
B.向某 溶液中加入少量 溶液中加入少量 晶体,所得溶液中 晶体,所得溶液中 水解程度增大,pH增大 水解程度增大,pH增大 |
| C.用同浓度的NaOH溶液分别中和等体积等pH的盐酸和醋酸溶液,盐酸消耗的NaOH溶液体积多 |
D.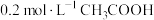 溶液与 溶液与 溶液等体积混合后存在: 溶液等体积混合后存在: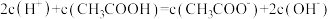 |
更新时间:2022-01-17 09:58:48
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验能达到预期目的的是
| 编号 | 实验内容 | 实验目的 |
| A | 快速拉伸装有 的针筒活塞,气体颜色变浅 的针筒活塞,气体颜色变浅 | 证明压强改变对平衡的影响 |
| B | 常温下,测物质的量浓度相等的HA和HB溶液的 | 比较HA与HB的酸性强弱 |
| C | 用 稀硫酸与足量纯锌反应,产生气泡速率较慢,加入 稀硫酸与足量纯锌反应,产生气泡速率较慢,加入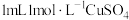 溶液后,迅速产生较多气泡 溶液后,迅速产生较多气泡 | 证明反应速率会随反应物浓度的增大而加快 |
| D | 向 硝酸银溶液中加入 硝酸银溶液中加入 溶液,出现白色沉淀,再加入几滴 溶液,出现白色沉淀,再加入几滴 的 的 溶液,有黑色沉淀生成 溶液,有黑色沉淀生成 | 证明在相同温度下的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法不正确 的是
A.稀氨水滴入稀盐酸中,当溶液呈中性时, |
B.将 溶液从常温加热至80℃,溶液的pH变小但仍保持中性 溶液从常温加热至80℃,溶液的pH变小但仍保持中性 |
C.常温下, 溶液呈碱性,说明 溶液呈碱性,说明 是弱电解质 是弱电解质 |
| D.常温下,pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】25℃时,pH=2的盐酸和醋酸溶液各1mL分别加水稀释,pH随溶液体积变化的曲线如图所示。下列说法正确的是
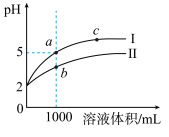

| A.曲线Ⅰ代表醋酸溶液的稀释过程 |
| B.a点溶液的导电性比c点溶液的导电能力差 |
C.与足量的锌反应,最终盐酸产生 的量较多 的量较多 |
| D.与相同浓度的NaOH溶液恰好中和时,醋酸消耗的NaOH溶液的体积大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】同为pH=1的醋酸与盐酸,加水分别稀释至溶液的pH相同,加入醋酸中水的体积为a,加入盐酸中水的体积为b,则a和b的关系为
| A.a>b | B.a<b | C.a=b | D.无法判断 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】向0.1mol/L的CH3COOH溶液中加水或加入少量CH3COONa晶体时,下列有关叙述不正确的是
| A.都能使溶液的pH增大 |
| B.都能使溶液中c(H+)·c(CH3COO-)增大 |
| C.溶液中c(H+)·c(OH-)不变 |
D.都能使溶液中 增大 增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一定温度下,将一定质量的冰醋酸加水稀释的过程中,溶液的导电能力变化如图所示,下列说法中正确的是


| A.a,b,c三点CH3COOH的电离平衡常数:c<a<b |
| B.a,b,c三点醋酸的电离程度:c<a<b |
| C.用湿润的pH试纸测量a处溶液的pH,测量结果偏小 |
| D.a,b,c三点溶液用1mol·L-1的氢氧化钠溶液中和,消耗氢氧化钠溶液的体积:c<a<b |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温时,一定浓度的一元酸HA、HB对应的钠盐和一元碱MOH、NOH对应的盐酸盐加水稀释过程中的pH变化如图所示(V0为初始体积,V为稀释后的体积),下列说法不正确 的是


A.lg 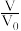 =0时,NaA溶液中:c(Na+)>c(A-)>c(OH-)>c(HA)>c(H+) =0时,NaA溶液中:c(Na+)>c(A-)>c(OH-)>c(HA)>c(H+) |
| B.若b+c=14,则Ka(HB)=Kb(MOH),MB溶液呈中性 |
C.加水稀释过程中,水的电离度不断减小,lg 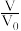 =2时,NCl溶液中水的电离度为:102-a% =2时,NCl溶液中水的电离度为:102-a% |
D.lg 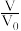 =0时,c(A-)>c(B-);c(N+)>c(M+) =0时,c(A-)>c(B-);c(N+)>c(M+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏伽德罗常数的值,下列叙述正确的是
| A.常温下1LpH=11的氨水中含有阳离子总数为0.001NA |
| B.4g 2H2中所含的质子数为4NA |
C.1mol甲醇中含有 键的数目为4NA 键的数目为4NA |
| D.常温常压下,22.4L的NO2和CO2混合气体含有2NA个氧原子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】H2C2O4为二元弱酸。20℃时,有一组H2C2O4和NaOH的混合溶液,其中c (H2C2O4) +c (HC2O4)+c (C2O42-)=0.1mol/L,溶液中部分微粒的物质的量浓度随pH 的变化如图所示。[电离度=( 已电离电解质分子数/原弱电解质分子数) x 100%] 下列说法不正确的是


| A.H2C2O4的Ka2数量级为10-5 |
| B.在NaHC2O4溶液中,c (Na+)>c(HC2O4)>c (H+)>c(C2O42-)>c (OH-) |
| C.0.1mol/L 的H2C2O4溶液,H2C2O4的电离度约为80% |
| D.pH=7.0的溶液中,c (Na+)=0.1+c(C2O42-)-c (H2C2O4) |
您最近一年使用:0次

 的值增大,可以采取的措施是
的值增大,可以采取的措施是