CuCl2溶液呈黄绿色,其中存在如下平衡:[CuCl4]2-(黄色)+4H2O [Cu(H2O)4]2-(蓝色)+4Cl- ∆H<0,下列可使溶液变成蓝色的方法是
[Cu(H2O)4]2-(蓝色)+4Cl- ∆H<0,下列可使溶液变成蓝色的方法是
 [Cu(H2O)4]2-(蓝色)+4Cl- ∆H<0,下列可使溶液变成蓝色的方法是
[Cu(H2O)4]2-(蓝色)+4Cl- ∆H<0,下列可使溶液变成蓝色的方法是| A.升温 | B.加NaCl(s) | C.加水稀释 | D.加压 |
更新时间:2022-02-17 08:39:04
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】一定条件下的密闭容器中:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH=-905.9 kJ/mol,下列叙述正确的是
4NO(g)+6H2O(g) ΔH=-905.9 kJ/mol,下列叙述正确的是
 4NO(g)+6H2O(g) ΔH=-905.9 kJ/mol,下列叙述正确的是
4NO(g)+6H2O(g) ΔH=-905.9 kJ/mol,下列叙述正确的是| A.向容器中充入4 mol NH3和5 mol O2进行反应,达到平衡时放出的热量为905.9 kJ。 |
| B.平衡时v正(O2)=v逆(NO)。 |
| C.平衡后降低压强,混合气体平均摩尔质量增大。 |
| D.平衡后升高温度,混合气体中NO含量降低。 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】取浓度均为 的
的 、
、 溶液各
溶液各 混合于试管中,发生反应:
混合于试管中,发生反应: 。将所得溶液分为四等份,进行如下实验。相关说法正确的是
。将所得溶液分为四等份,进行如下实验。相关说法正确的是
 的
的 、
、 溶液各
溶液各 混合于试管中,发生反应:
混合于试管中,发生反应: 。将所得溶液分为四等份,进行如下实验。相关说法正确的是
。将所得溶液分为四等份,进行如下实验。相关说法正确的是A.第一份溶液中加入 固体,平衡逆向移动,溶液颜色变浅 固体,平衡逆向移动,溶液颜色变浅 |
| B.第二份溶液中加水,溶液颜色变浅,但平衡不移动 |
| C.第三份溶液中加铁粉,平衡逆向移动,溶液颜色变浅 |
D.第四份溶液中加入氯水,溶液颜色变深(已知:还原性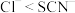 ) ) |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】NH3是重要的化工原料,可用于某些配合物的制备,如NiSO4溶于氨水形成[Ni(NH3)6]SO4。工业上常采用氨氧化法制硝酸,其流程是将氨和空气混合后通入灼热的铂铑合金网,反应生成NO(g),生成的一氧化氮与残余的氧气继续反应生成二氧化氮:2NO(g)+O2(g)=2NO2(g);ΔH=-116.4kJ·mol-1。随后将二氧化氮通入水中制取硝酸。工业上一般用石灰乳吸收硝酸工业尾气(NO和NO2),由于NO不能被碱吸收,一般控制NO和NO2约为1∶1通入石灰乳,净化尾气的同时又可制得混凝土添加剂Ca(NO2)2。对于反应2NO(g)+O2(g) 2NO2(g),下列说法正确的是
2NO2(g),下列说法正确的是
 2NO2(g),下列说法正确的是
2NO2(g),下列说法正确的是| A.该反应能够自发的原因是ΔS>0 |
| B.工业上使用合适的催化剂可提高NO2的生产效率 |
| C.升高温度,该反应v(逆)增大,v(正)减小,平衡向逆反应方向移动 |
| D.2molNO(g)和1molO2(g)中所含化学键键能总和比2molNO2(g)中大116.4kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】一定条件下,反应 3A(g)+3B(g)⇌ c(g)+D(g) ΔH<0 达到平衡,欲提高B的转化率,可采取的措施是
| A.升高温度 | B.增大 B 的浓度 | C.增大压强 | D.使用合适的催化剂 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】加热 溶液,发生反应:
溶液,发生反应: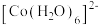 (粉红色)
(粉红色)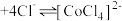 (蓝色)
(蓝色)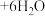 ,溶液颜色由粉红色变为蓝色。下列说法错误的是
,溶液颜色由粉红色变为蓝色。下列说法错误的是
 溶液,发生反应:
溶液,发生反应: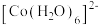 (粉红色)
(粉红色)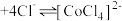 (蓝色)
(蓝色)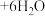 ,溶液颜色由粉红色变为蓝色。下列说法错误的是
,溶液颜色由粉红色变为蓝色。下列说法错误的是A.基态 原子的价电子排布式为 原子的价电子排布式为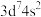 |
| B.该反应为吸热反应 |
C.向冷 溶液中加入 溶液中加入 固体,溶液变蓝 固体,溶液变蓝 |
| D.加水稀释,平衡正移 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】已知:CO2(g)+3H2(g) ⇌CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。一定条件下,向体积为1 L的密闭容器中充入1mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是
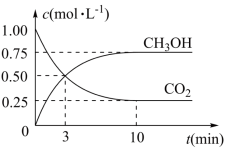

A.升高温度能使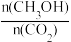 增大 增大 |
| B.反应达到平衡状态时,CO2的平衡转化率为75% |
| C.3min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率 |
| D.从反应开始到平衡,H2的平均反应速率v(H2)=0.075mol·L-1·min-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】反应CO(g)+H2O(g) CO2(g)+H2(g) ΔH=-41.2kJ·mol-1,在800℃时的化学平衡常数K=1.0。某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
CO2(g)+H2(g) ΔH=-41.2kJ·mol-1,在800℃时的化学平衡常数K=1.0。某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
此时反应中正、逆反应速率的关系式是
 CO2(g)+H2(g) ΔH=-41.2kJ·mol-1,在800℃时的化学平衡常数K=1.0。某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
CO2(g)+H2(g) ΔH=-41.2kJ·mol-1,在800℃时的化学平衡常数K=1.0。某时刻测得该温度下的密闭容器中各物质的物质的量见下表:| CO | H2O | CO2 | H2 |
| 0.5 mol | 8.5 mol | 2.0 mol | 2.0 mol |
此时反应中正、逆反应速率的关系式是
| A.v(正)>v(逆) | B.v(正)<v(逆) | C.v(正)=v(逆) | D.无法判断 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】某温度下,可逆反应mA(g)+nB(g) pC(g)的平衡常数为K,下列对K的说法正确的是( )
pC(g)的平衡常数为K,下列对K的说法正确的是( )
 pC(g)的平衡常数为K,下列对K的说法正确的是( )
pC(g)的平衡常数为K,下列对K的说法正确的是( )| A.K值越大,表明该反应越有利于C的生成 |
| B.若缩小反应器的容积,能使平衡正向移动,则K增大 |
| C.温度越高,K一定越大 |
| D.如果m+n=p,则K=1 |
您最近一年使用:0次

 (g)+ O2(g)
(g)+ O2(g) 

