按一定的速率用 溶液滴定
溶液滴定 溶液,溶液
溶液,溶液 和温度随
和温度随 的变化曲线如图所示。下列说法正确的是
的变化曲线如图所示。下列说法正确的是
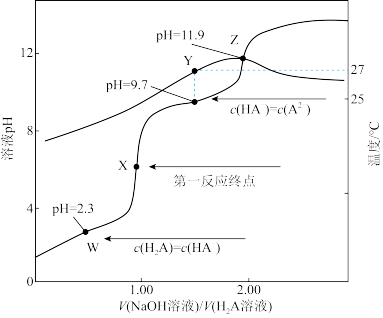
 溶液滴定
溶液滴定 溶液,溶液
溶液,溶液 和温度随
和温度随 的变化曲线如图所示。下列说法正确的是
的变化曲线如图所示。下列说法正确的是
A.根据溶液 和温度随 和温度随 的变化曲线图,滴定分析时,X点可用甲基橙、Z点可用酚酞作指示剂指示滴定终点 的变化曲线图,滴定分析时,X点可用甲基橙、Z点可用酚酞作指示剂指示滴定终点 |
B.当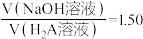 时溶液的 时溶液的 ,且溶液中 ,且溶液中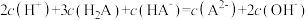 |
C.25℃时, 的电离常数 的电离常数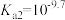 |
D.从W至Z点,Z点水的电离程度和 都最大 都最大 |
更新时间:2022-04-23 19:18:14
|
相似题推荐
单选题
|
较难
(0.4)
名校
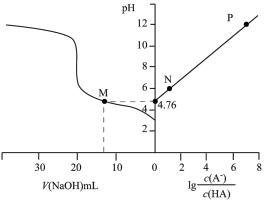
【推荐1】常温下,用 氢氧化钠溶液滴定一定浓度的
氢氧化钠溶液滴定一定浓度的 溶液,溶液的
溶液,溶液的 与加入氢氧化钠溶液的体积
与加入氢氧化钠溶液的体积 、
、 的关系如图。下列说法错误的是
的关系如图。下列说法错误的是
 氢氧化钠溶液滴定一定浓度的
氢氧化钠溶液滴定一定浓度的 溶液,溶液的
溶液,溶液的 与加入氢氧化钠溶液的体积
与加入氢氧化钠溶液的体积 、
、 的关系如图。下列说法错误的是
的关系如图。下列说法错误的是
A.从 点到 点到 点,水的电离程度逐渐变大 点,水的电离程度逐渐变大 | B.M点对应的溶液中 |
C.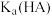 数量级为 数量级为 | D.滴定过程可采用酚酞作为指示剂 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】常温下,用浓度为 的盐酸滴定浓度均为
的盐酸滴定浓度均为 的
的 和
和 的混合溶液,滴定过程中溶液的
的混合溶液,滴定过程中溶液的 随
随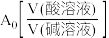 的变化曲线如图所示,下列说法正确的是
的变化曲线如图所示,下列说法正确的是
 的盐酸滴定浓度均为
的盐酸滴定浓度均为 的
的 和
和 的混合溶液,滴定过程中溶液的
的混合溶液,滴定过程中溶液的 随
随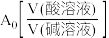 的变化曲线如图所示,下列说法正确的是
的变化曲线如图所示,下列说法正确的是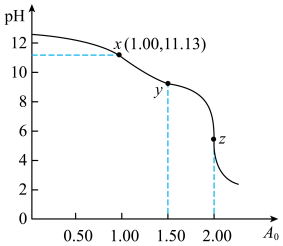
A.该温度下,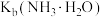 约为 约为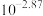 |
B.水的电离程度: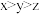 |
C.点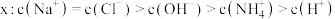 |
D.点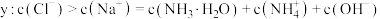 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】根据下列实验操作和现象,得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 常温下,用pH计分别测定等体积1  溶液和0.1 溶液和0.1  溶液的pH,测得的pH值相同 溶液的pH,测得的pH值相同 | 浓度对水的电离程度无影响 |
| B | 灼烧铜丝至其表面变黑、灼热,伸入盛有某有机物的试管中,铜丝恢复亮红色 | 该有机物中可能有醇羟基或羧基 |
| C | 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去,试管里出现凝胶 | 非金属性:Cl>Si |
| D | 加热麦芽糖和稀 混合溶液,冷却;加入NaOH溶液后加入银氨溶液,加热,出现银镜 混合溶液,冷却;加入NaOH溶液后加入银氨溶液,加热,出现银镜 | 麦芽糖发生了水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】某温度时,分别调节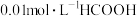 溶液、
溶液、 氨水的pH,系统中各种粒子浓度的负对数值
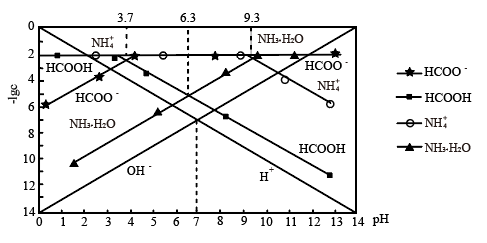
氨水的pH,系统中各种粒子浓度的负对数值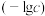 与pH的关系如图所示。下列说法正确的是
与pH的关系如图所示。下列说法正确的是
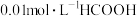 溶液、
溶液、 氨水的pH,系统中各种粒子浓度的负对数值
氨水的pH,系统中各种粒子浓度的负对数值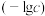 与pH的关系如图所示。下列说法正确的是
与pH的关系如图所示。下列说法正确的是
| A.系统温度高于25℃ |
B.该温度下,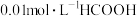 溶液的pH为3.7 溶液的pH为3.7 |
C.用标准 溶液滴定一定浓度的 溶液滴定一定浓度的 溶液用酚酞作指示剂 溶液用酚酞作指示剂 |
D.向 溶液中加入 溶液中加入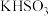 溶液至溶液呈中性: 溶液至溶液呈中性: |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】298 K时,分别向体积、浓度均为20mL0.1mol·L-1的HX溶液、HY溶液中滴加等浓度的NaOH 溶液,混合溶液的pH与加入NaOH溶液体积(V)之间的关系如图所示。(注明:弱电解质的电离度等于已电离的电解质的量与电解质总量之比)下列说法正确的是
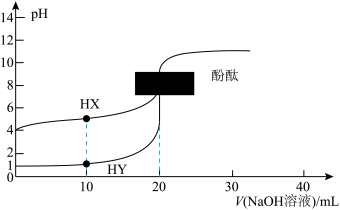

| A.298K 时,0.1mol·L-1HX 溶液中HX的电离度为1% |
B.V=10mL时,同时微热溶液(忽略体积变化),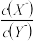 逐渐增大 逐渐增大 |
| C.V=20mL 时,HX曲线对应的溶液中c(Na+)=c(X-)>c(H+)=c(OH-) |
| D.滴定这两种溶液时都可以选择甲基橙替代酚酞作指示剂 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】25°C时,体积均为25.00mL,浓度均为0.0100mol·L-1的HA、H3B溶液分别用0.0100mol·L-1NaOH溶液滴定。溶液的pH随V(NaOH)变化曲线如图所示。下列说法中正确的是
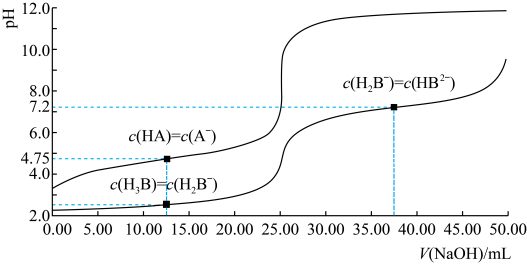

| A.NaOH溶液滴定HA溶液可选甲基橙作指示剂 |
| B.均为0.0100mol·L-1HA、H3B溶液中,酸性较强的是HA |
| C.25℃时,0.0100mol·L-1Na2HB溶液的pH<7 |
| D.25℃时,向Na2HB溶液中滴加HA溶液反应的离子方程式为HB2—+HA=H2B—+A— |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】室温时,向20mL0.1000mol·L-1H2C2O4溶液中滴加0.1000mol·L-1NaOH溶液,混合溶液的pH随滴加NaOH溶液体积的变化如图所示。下列有关叙述错误的是
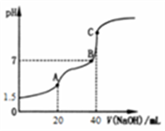
| A.忽略H2C2O4的第二步电离,由题给信息,可以计算出常温下H2C2O4的电离常数 |
| B.A、B、C三点所对应的溶液中,水的电离程度最小的是A点 |
| C.A、B、C三点所对应的溶液中,均有c(Na+)<c(OH-)+c(HC2O4-)+2c(C2O42-) |
| D.在B点溶液中,生成的含钠化合物有两种,且n(HC2O4-)+n(C2O42-)=2.0×10-3mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】向20mL 0.5mol/L的氨水中逐滴加入等物质的量浓度的盐酸,测定混合溶液的温度变化如图所示.下列关于混合溶液的说法错误的是
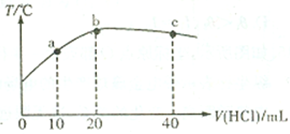

| A.从a点到b点,混合溶液不可能存在:c(Cl-)=c(NH4+) |
| B.由水电离的c(H+):b点>c点 |
| C.NH3·H2O的电离程度:b点>a点 |
| D.b点到c点,混合溶液中可能存在:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】25℃时,向20mL浓度均为0.1mol•L-1的盐酸和醋酸的混合溶液中逐滴加入0.1mol•L-1的NaOH溶液(醋酸的Ka=1.8×10-5;用0.1mol•L-1的NaOH溶液滴定20mL等浓度的盐酸,滴定终点的pH突跃范围4.3~9.7)。下列说法不正确的是
| A.恰好中和时,溶液中醋酸根离子浓度为a,向其中加入0.002mol的醋酸钠固体,醋酸根离子浓度大于2a |
| B.滴加NaOH溶液至pH=4.3的过程中,发生反应的离子方程式为:H++OH-=H2O |
| C.滴定过程中,c(Cl-)=c(Ac-)+c(HAc) |
| D.pH=7时,c(Na+)>c(Cl-)>c(Ac-)>c(HAc) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),向20mL0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液,根据图示判断,下列说法正确的是( )
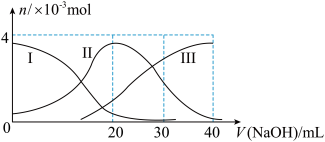

A.H2A在水中的电离方程式是:H2A=H++HA-;HA- H++A2- H++A2- |
| B.当V(NaOH)=20 mL时,溶液中各离子浓度的大小顺序为:c(OH-) >c(H+) |
| C.当V(NaOH)=40 mL时,溶液中水的电离程度比纯水大 |
| D.当V(NaOH)=30 mL时,溶液中存在以下关系:2c(H+)+c(HA-)+2c(H2A)=c(A2-)+2c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
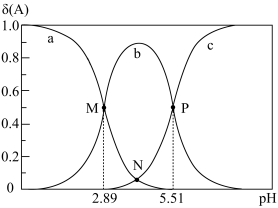
【推荐2】邻苯二甲酸(用 表示)为二元酸,室温下,向
表示)为二元酸,室温下,向 邻苯二甲酸溶液中逐渐加入氢氧化钠固体,溶液中的各粒子浓度的物质的量分数
邻苯二甲酸溶液中逐渐加入氢氧化钠固体,溶液中的各粒子浓度的物质的量分数 (A)随pH的变化如图所示(已知
(A)随pH的变化如图所示(已知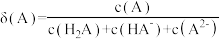 )。下列说法正确的是
)。下列说法正确的是
 表示)为二元酸,室温下,向
表示)为二元酸,室温下,向 邻苯二甲酸溶液中逐渐加入氢氧化钠固体,溶液中的各粒子浓度的物质的量分数
邻苯二甲酸溶液中逐渐加入氢氧化钠固体,溶液中的各粒子浓度的物质的量分数 (A)随pH的变化如图所示(已知
(A)随pH的变化如图所示(已知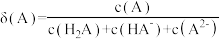 )。下列说法正确的是
)。下列说法正确的是
A.曲线b表示的是 的变化 的变化 |
B. 的数量级为 的数量级为 |
C.将相同物质的量的NaHA与 配成溶液,pH=5.51 配成溶液,pH=5.51 |
D.pH<7时,溶液中可能存在: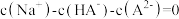 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】甘氨酸盐酸盐(HOOCCH2NH3Cl)的水溶液呈酸性,溶液中存在以下平衡:
HOOCCH2NH
 -OOCCH2NH
-OOCCH2NH +H+ K1
+H+ K1
-OOCCH2NH
 -OOCCH2NH2+H+ K2
-OOCCH2NH2+H+ K2
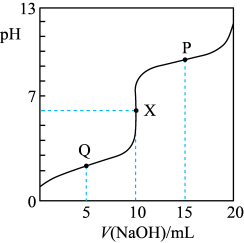
常温时,向10mL一定浓度的HOOCCH2NH3Cl的水溶液中滴入同浓度的NaOH溶液。混合溶液pH随加入NaOH溶液体积的变化如图所示。下列说法不正确的是
HOOCCH2NH

 -OOCCH2NH
-OOCCH2NH +H+ K1
+H+ K1-OOCCH2NH

 -OOCCH2NH2+H+ K2
-OOCCH2NH2+H+ K2常温时,向10mL一定浓度的HOOCCH2NH3Cl的水溶液中滴入同浓度的NaOH溶液。混合溶液pH随加入NaOH溶液体积的变化如图所示。下列说法不正确的是

A.Q→X过程中: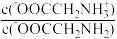 逐渐减小 逐渐减小 |
B.X点的溶液中:c(-OOCCH2NH2)>c(HOOCCH2NH ) ) |
C.P点的溶液中:c(HOOCCH2NH )+c(H+)=c(-OOCCH2NH2)+c(OH-) )+c(H+)=c(-OOCCH2NH2)+c(OH-) |
| D.当V(NaOH)=20mL时,混合溶液中的溶质主要为NaOOCCH2NH2和NaCl |
您最近一年使用:0次



