 是一种高效多功能的饮用水处理剂。已知:①一种干法制备
是一种高效多功能的饮用水处理剂。已知:①一种干法制备 的反应为
的反应为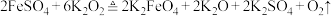 ,②
,② 处理水时发生反应
处理水时发生反应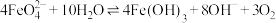 。下列说法错误的是
。下列说法错误的是A.干法制备 的反应中,还原剂与氧化剂的物质的量之比为 的反应中,还原剂与氧化剂的物质的量之比为 |
B.干法制备 的反应中,每生成 的反应中,每生成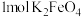 ,有 ,有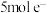 转移 转移 |
C. 在强碱性溶液中能稳定存在 在强碱性溶液中能稳定存在 |
D. 处理水时,既能杀菌消毒,又能起絮凝作用除去水中悬浮杂质 处理水时,既能杀菌消毒,又能起絮凝作用除去水中悬浮杂质 |
2022·湖南·模拟预测 查看更多[3]
湖南省市(州)部分学校2022届高三下学期“一起考”大联考(模拟三)化学试题(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点14 铁及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
更新时间:2022-05-21 19:01:59
|
相似题推荐
单选题
|
适中
(0.65)
名校
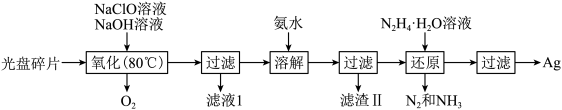
【推荐1】利用如下流程可从废光盘中回收金属层中的银(金属层中其他金属含量过低,对实验影响可忽略):
已知: 溶液在加热时易分解生成
溶液在加热时易分解生成 和
和 。下列说法不正确的是
。下列说法不正确的是
已知:
 溶液在加热时易分解生成
溶液在加热时易分解生成 和
和 。下列说法不正确的是
。下列说法不正确的是
| A.若省略第一次过滤,会使氨水的用量增加 |
B.若“还原”工序利用原电池来实现,则 是正极产物 是正极产物 |
C.“还原”时,每生成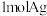 ,理论上消耗 ,理论上消耗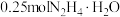 |
D.“溶解”工序发生的反应: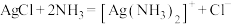 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的值。下列叙述错误的是
A.在电解精炼粗铜的过程中,当阴极质量增重32g时转移的电子数为 |
B.标准状况下,11.2LSO3分子数目大于 |
C.15g乙烯和20g丙烯的混合气体中含有C—H共价键的数目为 |
D.4.6gNa与足量O2充分反应,反应中转移的电子数介于 和 和 之间 之间 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】利用NaClO氧化尿素制备N2H4•H2O(水合肼)的实验流程如图所示:

已知:①氯气与烧碱溶液的反应是放热反应;
②N2H4•H2O有强还原性,能与NaClO剧烈反应生成N2。下列说法正确的是

已知:①氯气与烧碱溶液的反应是放热反应;
②N2H4•H2O有强还原性,能与NaClO剧烈反应生成N2。下列说法正确的是
| A.步骤I中无需控制反应的温度 |
| B.步骤I制备NaClO溶液时,测得产物中NaClO与NaClO3的物质的量之比为5∶1,则参与反应的氧化剂与还原剂的物质的量之比为3∶5 |
| C.步骤II中可将尿素水溶液逐滴滴入NaClO碱性溶液中 |
D.生成水合肼反应的离子方程式为:ClO-+CO(NH2)2+2OH-=Cl-+N2H4•H2O+CO |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知羟胺( 其中氮元素的化合价为-1)在碱性条件下能发生热分解反应:
其中氮元素的化合价为-1)在碱性条件下能发生热分解反应:
 。若还原剂比氧化剂多0.5mol,则下列判断正确的是( )
。若还原剂比氧化剂多0.5mol,则下列判断正确的是( )
 其中氮元素的化合价为-1)在碱性条件下能发生热分解反应:
其中氮元素的化合价为-1)在碱性条件下能发生热分解反应: 。若还原剂比氧化剂多0.5mol,则下列判断正确的是( )
。若还原剂比氧化剂多0.5mol,则下列判断正确的是( )| A.有0.5mol羟胺被氧化 | B.氧化产物比还原产物多0.5mol |
| C.反应生成标准状况下22.4L气体 | D.每生成18g水转移 个电子 个电子 |
您最近一年使用:0次
【推荐1】Na2FeO4是一种高效多功能水处理剂。制备方法之一为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,下列说法正确的是
| A.Na2O2只作氧化剂 | B.1 mol FeSO4可还原2 mol Na2O2 |
| C.转移0.8 mol电子时生成33.2 g Na2FeO4 | D.还原剂与氧化剂的物质的量之比为1:3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式与所述事实相符且正确的是
| A.漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3- |
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl- Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
C.向Na[Al(OH)4]溶液中通入过量CO2制Al(OH)3∶[Al(OH)4]-+CO2=Al(OH)3↓+ |
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3=2 +3Cl-+H2O+4H+ +3Cl-+H2O+4H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列现象不能用平衡移动原理解释的是
A.室温下,将 平衡体系压缩体积后颜色加深 平衡体系压缩体积后颜色加深 |
B. ,把 ,把 球浸泡在冰水中,气体颜色变浅 球浸泡在冰水中,气体颜色变浅 |
C.工业制取钾 ,选取合适的温度,使 ,选取合适的温度,使 变成蒸气从体系逸出 变成蒸气从体系逸出 |
| D.实验室制备氯气,用排饱和食盐水收集氯气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列生产生活的实际应用中,不能用勒夏特列原理解释的是
| A.用饱和食盐水除去Cl2中的HCl |
| B.使用更有效的催化剂,提高可逆反应的转化率 |
| C.工业合成NH3是放热反应,为提高NH3的产率,理论上应采取低温的措施 |
D.工业生产硫酸的过程中,使用过量的空气,以提高二氧化硫的利用率(2SO2+O2  2SO3) 2SO3) |
您最近一年使用:0次

 和SO
和SO 的离子数之比为1:3时正好完全发生氧化还原反应(已如SO
的离子数之比为1:3时正好完全发生氧化还原反应(已如SO );X在还原产物中的化合价为( )
);X在还原产物中的化合价为( ) ,使用光纤进行通讯传输可以节约有色金属
,使用光纤进行通讯传输可以节约有色金属 作为水处理剂,不仅可以消毒、净水,还可以将硬水软化
作为水处理剂,不仅可以消毒、净水,还可以将硬水软化

