下列对各种平衡体系的叙述中,不正确的是
A.一定浓度的醋酸钠溶液可使酚酞试液变红,其原因是溶液中存在如下平衡:CH3COO- +H2O CH3COOH+OH-,使得溶液中的c(OH-)>c(H+) CH3COOH+OH-,使得溶液中的c(OH-)>c(H+) |
B.某温度下,容积一定的密闭容器中进行可逆反应,X(g) +Y(g) 2Z(g)+W(s) 平衡后,升高温度,c(Z)增大 2Z(g)+W(s) 平衡后,升高温度,c(Z)增大 |
| C.常温下,在醋酸溶液中加入少量的CH3COONa固体,会使其电离平衡正向移动C在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,平衡向溶解的方向移动 |
| D.在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,平衡向溶解的方向移动 |
2013·天津·二模 查看更多[1]
(已下线)2013届天津市十二校高三第二次模拟联考化学试卷
更新时间:2016-12-09 04:23:55
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】对于一定条件下的氧化还原反应:2Fe3++2I- 2Fe2++I2,下列说法
2Fe2++I2,下列说法不正确 的是
 2Fe2++I2,下列说法
2Fe2++I2,下列说法| A.该反应达到平衡后,改变溶液的酸碱性不会影响平衡状态 |
| B.该反应达到平衡后,加入CCl4充分振荡可使平衡向右移动 |
| C.该反应达到平衡后,体系中Fe3+和I2的氧化性强弱相当 |
| D.将该反应设计成原电池,当电流计示数刚好变为“0”时,达到该反应进行的限度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】氨气是化肥工业和基础有机合成工业的重要原料。诺贝尔奖获得者埃特尔提出了合成氨反应吸附解离的机理,通过实验测得合成氨反应势能如图所示:
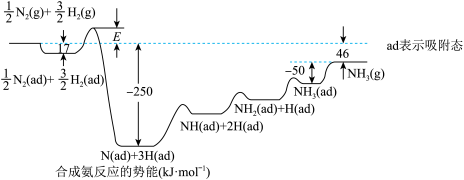
下列说法正确的是

下列说法正确的是
| A.反应中既有非极性共价键的断裂,又有非极性共价键的生成 |
B.在合成氨吸附解离的过程中,状态最稳定的是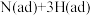 |
C.该反应的热化学方程式为 |
| D.研发更加高效的催化剂,可进一步降低该反应的活化能,提高氮气的平衡转化率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】在HNO2溶液中存在如下平衡:HNO2 H++
H++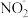 ,向该溶液中加入少量的下列物质后,能使电离平衡向右移动且使H+ 数目增多的是
,向该溶液中加入少量的下列物质后,能使电离平衡向右移动且使H+ 数目增多的是
 H++
H++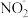 ,向该溶液中加入少量的下列物质后,能使电离平衡向右移动且使H+ 数目增多的是
,向该溶液中加入少量的下列物质后,能使电离平衡向右移动且使H+ 数目增多的是| A.水 | B.NaOH | C.NaNO2 | D.HNO3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】25℃时,水中存在电离平衡:H2O  H++OH-△H>0。下列叙述正确的是
H++OH-△H>0。下列叙述正确的是
 H++OH-△H>0。下列叙述正确的是
H++OH-△H>0。下列叙述正确的是| A.将水加热,Kw增大,pH不变 |
| B.向水中加入少量NaOH固体,平衡逆向移动,c(OH-)降低 |
| C.向水中加入少量NH4Cl固体,平衡正向移动,溶液呈碱性 |
| D.向0.1mol/L的醋酸溶液中加入一定量醋酸钠晶体,溶液中c(OH-)增大,Kw不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列实验设计不能达目的的是
| 实验设计 | 目的 | |
| A | 室温下,用pH试纸测定浓度均为0.1 mol/L的NaClO溶液和CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| B | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入足量的相同体积、不同浓度的稀硫酸 | 探究浓度对反应速率的影响 |
| C | 用铁片、铜片、稀硫酸等组成原电池 | 比较铁、铜的金属性强弱 |
| D | 向1mL 0.1 mol/L AgNO3溶液中滴加0.1 mol/L NaCl溶液,至不再有白色沉淀生成,再向其中滴加几滴0.1 mol/L KI溶液 | 验证:Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列物质溶于水,由于水解而使溶液呈酸性的是( )
| A.P2O5 | B.NaHSO4 | C.NaF | D.CuCl2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】当氢氧化钙固体在水中达到溶解平衡时,为使Ca(OH)2固体的量减少,可以加入少量的
| A.NaOH固体 | B.CaCl2固体 | C.NH4NO3固体 | D.Ca(OH)2固体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知t ℃时,Ksp(AgCl)=4×10-10,该温度下AgBr在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
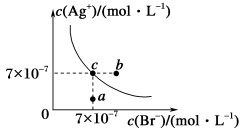

| A.图中a点对应的是t ℃时AgBr的不饱和溶液 |
| B.向AgBr饱和溶液中加入NaBr固体,可使溶液由c点变为b点 |
| C.t ℃时,AgBr的Ksp为4.9×10-13 |
D.t ℃时,AgCl(s)+Br-(aq)  AgBr(s)+Cl-(aq)的平衡常数K≈816 AgBr(s)+Cl-(aq)的平衡常数K≈816 |
您最近一年使用:0次

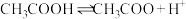 ,下列叙述
,下列叙述 醋酸加水稀释,溶液中导电粒子的数目增大
醋酸加水稀释,溶液中导电粒子的数目增大

