 和
和 在一定条件下合成甲醇的反应为;
在一定条件下合成甲醇的反应为; 。现在容积均为
。现在容积均为 的a、b、c、d、e五个密闭容器中分别充入
的a、b、c、d、e五个密闭容器中分别充入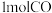 和
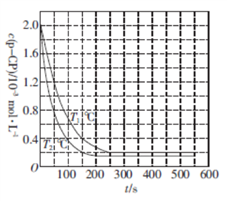
和 的混合气体,控制温度,进行实验,测得相关数据如图(图1:温度分别为300℃、500℃的密闭容器中,甲醇的物质的量:图2:温度分别为
的混合气体,控制温度,进行实验,测得相关数据如图(图1:温度分别为300℃、500℃的密闭容器中,甲醇的物质的量:图2:温度分别为 的密闭容器中,反应均进行到
的密闭容器中,反应均进行到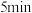 时甲醇的体积分数)。下列叙述正确的是
时甲醇的体积分数)。下列叙述正确的是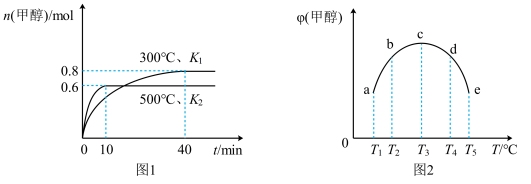
A.该反应的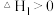 ,且 ,且 |
B.将容器c中的平衡状态转变到容器 中的平衡状态,可采取的措施有升温或加压 中的平衡状态,可采取的措施有升温或加压 |
C.300℃时,向平衡后的容器中再充入 , ,  ,平衡正向移动 ,平衡正向移动 |
D.500℃时,向平衡后的容器中再充入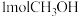 ,重新平衡后, ,重新平衡后, 的百分含量增大 的百分含量增大 |
更新时间:2022-04-13 11:26:29
|
相似题推荐
单选题
|
较难
(0.4)
名校
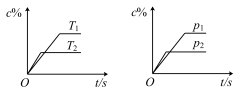
【推荐1】对于可逆反应mA(s)+nB(g) eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
 eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
| A.达到平衡后,若使用催化剂,C的质量分数将增大 |
| B.达到平衡后,增加A的量有利于化学平衡向正方向移动 |
| C.化学方程式中n>e+f |
| D.达到平衡后,若升高温度,化学平衡向逆方向移动 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在恒容密闭容器中充入2 mol CO2和0.5 mol H2发生如下反应: CO2(g)+H2(g) CO(g)+H2O(g) ΔH>0如图所示为该反应正反应的平衡常数K正和逆反应的平衡常数K逆随温度变化的曲线。下列分析正确的是
CO(g)+H2O(g) ΔH>0如图所示为该反应正反应的平衡常数K正和逆反应的平衡常数K逆随温度变化的曲线。下列分析正确的是
 CO(g)+H2O(g) ΔH>0如图所示为该反应正反应的平衡常数K正和逆反应的平衡常数K逆随温度变化的曲线。下列分析正确的是
CO(g)+H2O(g) ΔH>0如图所示为该反应正反应的平衡常数K正和逆反应的平衡常数K逆随温度变化的曲线。下列分析正确的是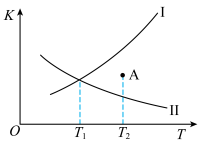
| A.曲线Ⅰ为K逆,曲线Ⅱ为K正 |
B.T2时,A点 正> 正> 逆 逆 |
| C.T1时,CO2的平衡转化率为40% |
| D.其他条件不变,在原平衡基础上再充入2 mol CO2和1 mol H2,达新平衡时CO2转化率将减小 |
您最近一年使用:0次
【推荐1】 时,向恒容容器中加入A发生反应:①
时,向恒容容器中加入A发生反应:①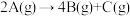 ,②
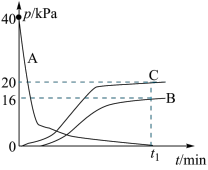
,②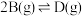 。反应体系中A、B、C的分压随时间t的变化曲线如图所示。下列说法错误的是
。反应体系中A、B、C的分压随时间t的变化曲线如图所示。下列说法错误的是
 时,向恒容容器中加入A发生反应:①
时,向恒容容器中加入A发生反应:①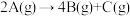 ,②
,②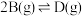 。反应体系中A、B、C的分压随时间t的变化曲线如图所示。下列说法错误的是
。反应体系中A、B、C的分压随时间t的变化曲线如图所示。下列说法错误的是
| A.容器内压强保持不变,表明反应达到平衡状态 |
| B. t1时刻A物质反应完全 |
C. 时,反应②的分压平衡常数 时,反应②的分压平衡常数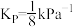 |
D.当C、D的分压相等时,反应②中B的转化率为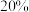 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】实验是化学的灵魂,通过实验认识化学原理是化学学科的特点。通过测定电导率可以学习沉淀溶解平衡。本地室内气温是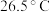 。已知:
。已知: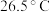 时
时 饱和溶液的电导率为
饱和溶液的电导率为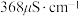 ,
,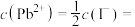
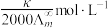 ,
,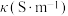 为电导率,
为电导率,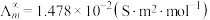 ,
,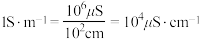 。
。
实验1: 悬浊液加水稀释过程中电导率的测定装置如图1所示,测定结果如图2所示。
悬浊液加水稀释过程中电导率的测定装置如图1所示,测定结果如图2所示。 饱和溶液中分别滴加相同浓度的
饱和溶液中分别滴加相同浓度的 溶液,测定电导率的增量,实验结果如下表:
溶液,测定电导率的增量,实验结果如下表:
实验3:验证温度对电导率的影响,实验数据如下表:
若实验过程测得蒸馏水的电导率是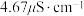 ,结合实验数据,下列说法正确的是
,结合实验数据,下列说法正确的是
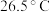 。已知:
。已知: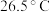 时
时 饱和溶液的电导率为
饱和溶液的电导率为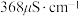 ,
,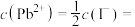
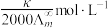 ,
,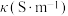 为电导率,
为电导率,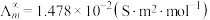 ,
,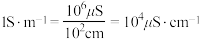 。
。实验1:
 悬浊液加水稀释过程中电导率的测定装置如图1所示,测定结果如图2所示。
悬浊液加水稀释过程中电导率的测定装置如图1所示,测定结果如图2所示。 
 饱和溶液中分别滴加相同浓度的
饱和溶液中分别滴加相同浓度的 溶液,测定电导率的增量,实验结果如下表:
溶液,测定电导率的增量,实验结果如下表: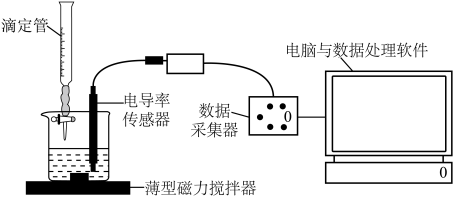
序号 |
| 电导率/ | 电导率增量/ | ||
饱和溶液 | 蒸馏水 | 饱和溶液 | 蒸馏水 | ||
0 | 0 | 368 | 4 | 0 | 0 |
1 | 0.100 | 392 | 49 | 24 | 45 |
2 | 0.200 | 421 | 100 | 53 | 96 |
3 | 0.300 | 447 | 149 | 79 | 145 |
4 | 0.400 | 470 | 206 | 102 | 202 |
序号 | 实验温度 | 电导率 | |
悬浊液 | 澄清液 | ||
1 | 25.5 | 334 | 334 |
2 | 30.0 | 395 | 368 |
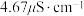 ,结合实验数据,下列说法正确的是
,结合实验数据,下列说法正确的是A.实验过程中为了测定 的 的 ,不需要测定水的电导率 ,不需要测定水的电导率 |
B.该实验条件下测得饱和 溶液的浓度约是 溶液的浓度约是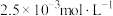 |
C.该实验条件下测得 的溶度积常数的数量级是 的溶度积常数的数量级是 |
D. 在蒸馏水和 在蒸馏水和 溶液中的溶解度相同 溶液中的溶解度相同 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】我国提出“CO2排放力争于2023年前达到峰值,努力争取2060年前实现碳中和”。研发CO2的利用技术,降低空气中CO2的含量是实现该目标的重要途径。
(1)下面是用H2捕捉CO2时发生的两个反应:
I.CO2(g)+4H2(g) CH4(g)+2H2O(g) ∆H1
CH4(g)+2H2O(g) ∆H1
II.CO2(g)+H2(g) CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2
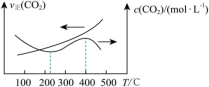
①反应I、II的lnK随1/T的变化如图所示,则ΔH2___________ 0(填“>”“<”或“=”)0;有利于反应I自发进行的温度是___________ (填“高温”或“低温”)。___________ ,而速率仍然增大的可能原因是___________ ___________ ,反应II的平衡常数Kp为___________ (保留两位有效数字)。[已知:CH4的选择性=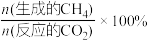 ]
]
(2)利用化学链将高炉废气中的CO2转化为CO的示意图如下。___________ ,该化学链的总反应是___________ 。
(1)下面是用H2捕捉CO2时发生的两个反应:
I.CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ∆H1
CH4(g)+2H2O(g) ∆H1II.CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2①反应I、II的lnK随1/T的变化如图所示,则ΔH2
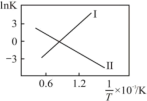
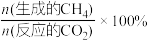 ]
](2)利用化学链将高炉废气中的CO2转化为CO的示意图如下。

您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
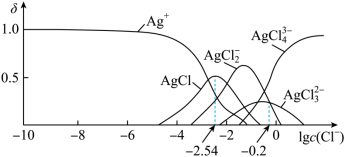
【推荐1】湿法提银工艺中,浸出的Ag+需加入Cl-进行沉淀。25℃时,平衡体系中含Ag微粒的分布系数δ[如δ(AgCl )=
)=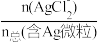 ]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
 )=
)=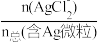 ]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
| A.AgCl溶解度随c(Cl-)增大而不断减小 |
| B.沉淀最彻底时,溶液中c(Ag+)=10-7.21mol•L-1 |
C.当c(Cl-)=10-2mol•L-1时,溶液中c(AgCl )>c(Ag+)>c(AgCl )>c(Ag+)>c(AgCl ) ) |
D.25℃时,AgCl +Cl- +Cl- AgCl AgCl 的平衡常数K=100.2 的平衡常数K=100.2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列图示与对应的叙述相符的是
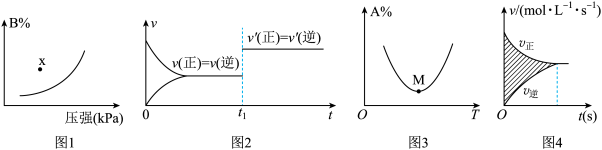

A.图1表示反应: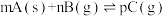  在一定温度下B的百分含量与压强变化的关系如图所示,则x点正反应速率小于逆反应速率 在一定温度下B的百分含量与压强变化的关系如图所示,则x点正反应速率小于逆反应速率 |
B.图2是可逆反应:  的速率时间图像,在 的速率时间图像,在 时刻改变条件只能是加入催化剂 时刻改变条件只能是加入催化剂 |
C.图3表示对于化学反应 ,A的百分含量与温度(T)的变化情况,则该反应的 ,A的百分含量与温度(T)的变化情况,则该反应的 |
| D.图4所示图中的阴影部分面积的含义是该物质物质的量的变化量 |
您最近一年使用:0次

 10-5 mol • L-1 • s-1
10-5 mol • L-1 • s-1
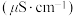

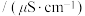

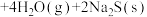
 。在压强为
。在压强为 的条件下,测得达到平衡时的有关气体体积分数的变化如图中实线所示:
的条件下,测得达到平衡时的有关气体体积分数的变化如图中实线所示:
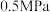 时,虚线Ⅱ可能为
时,虚线Ⅱ可能为 的变化曲线
的变化曲线

