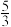在容积为2 L的恒容密闭容器中充入P(g)和Q(g),发生反应P(g)+2Q(g)⇌3R(g)+4S(s) ΔH。所得数据如下表:
下列说法正确的是
| 组号 | 温度/℃ | 起始量/mol | 平衡量/mol | ||
| n(P) | n(Q) | n(R) | n(S) | ||
| ① | 500 | 0.10 | 0.80 | 0.24 | 0.32 |
| ② | 500 | 0.20 | 1.60 | x | 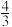 x x |
| ③ | 700 | 0.10 | 0.30 | 0.18 | 0.24 |
| A.该反应的ΔH>0 | B.反应达到平衡后增大压强,平衡逆向移动 |
| C.②中反应的平衡常数K=6.0 | D.根据题目信息不能确定x的值 |
22-23高二上·山东威海·阶段练习 查看更多[3]
更新时间:2022-09-24 21:23:52
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列实验中,对现象的解释不正确 的是
| 选项 | A | B | C | D |
| 装置及操作 |  向右轻轻推动活塞压缩体积 | 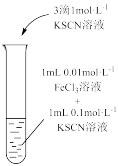 | 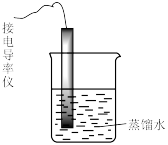 分别测定20℃和80℃蒸馏水的电导率 | 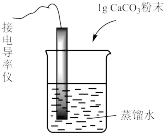 |
| 现象 | 气体红棕色先变深再变浅 | 溶液血红色加深 | 80℃蒸馏水的电导率大于20℃的 | 加入 粉末后电导率增大 粉末后电导率增大 |
| 解释 | 压强增大, 平衡先逆向移动,再正向移动 平衡先逆向移动,再正向移动 | 增大反应物浓度,  平衡正向移动 平衡正向移动 | 温度升高,水的电离平衡正向移动 |  在水中存在 在水中存在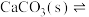  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】向甲、乙两个容积均为 的恒容密闭容器中分别充入
的恒容密闭容器中分别充入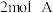 、
、 和
和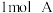 、
、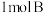 。相同条件下,发生反应
。相同条件下,发生反应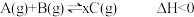 。测得两容器中
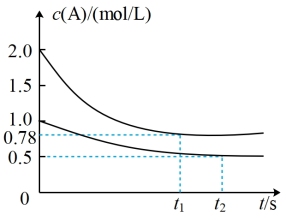
。测得两容器中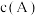 随时间t的变化关系如图所示。下列说法不正确的是
随时间t的变化关系如图所示。下列说法不正确的是
 的恒容密闭容器中分别充入
的恒容密闭容器中分别充入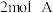 、
、 和
和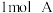 、
、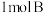 。相同条件下,发生反应
。相同条件下,发生反应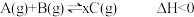 。测得两容器中
。测得两容器中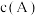 随时间t的变化关系如图所示。下列说法不正确的是
随时间t的变化关系如图所示。下列说法不正确的是
| A.x等于3 |
| B.向平衡后的乙容器中充入氦气,平衡不移动 |
C.向平衡后的乙容器中再加入 ,达到平衡后各物质的体积分数与甲容器中的相同 ,达到平衡后各物质的体积分数与甲容器中的相同 |
D.若向甲容器中再充入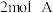 、 、 ,则达到化学平衡时甲容器中 ,则达到化学平衡时甲容器中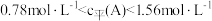 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):A2(g)+3B2(g) 2AB3(g) ΔH<0,相关数据如下表所示:
2AB3(g) ΔH<0,相关数据如下表所示:
下列说法正确的是
 2AB3(g) ΔH<0,相关数据如下表所示:
2AB3(g) ΔH<0,相关数据如下表所示:| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1mol A2、3molB2 | 2molAB3 | 2mol AB3 |
| 反应物的转化率 | α甲 | α乙 | α丙 |
| 反应的平衡常数K | K甲 | K乙 | K丙 |
| 平衡时AB3的浓度/mol·L-1 | c甲 | c乙 | c丙 |
| 平衡时AB3的反应速率/mol·L-1·min-1 | υ甲 | υ乙 | υ丙 |
| A.υ甲=υ丙 | B.c乙< c丙 | C.α甲 +α乙<1 | D.K乙≤K丙 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
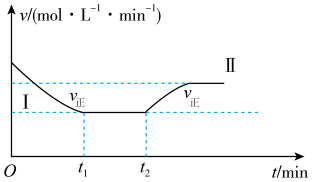
【推荐1】在某一恒温、恒容的密闭容器中发生反应:3H2(g)+N2(g) 2NH3(g) ΔH<0。t1时刻反应达到平衡,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是
2NH3(g) ΔH<0。t1时刻反应达到平衡,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是
 2NH3(g) ΔH<0。t1时刻反应达到平衡,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是
2NH3(g) ΔH<0。t1时刻反应达到平衡,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是
| A.Ⅰ、Ⅱ两过程达到平衡时,平衡常数:KⅠ<KⅡ |
| B.Ⅰ、Ⅱ两过程达到平衡时,NH3的体积分数:Ⅰ<Ⅱ |
| C.Ⅰ、Ⅱ两过程达到平衡的标志:气体的平均密度不再发生变化 |
| D.t2时刻改变的条件可以是向密闭容器中加H2和N2的混合气 |
您最近一年使用:0次
单选题
|
较难
(0.4)
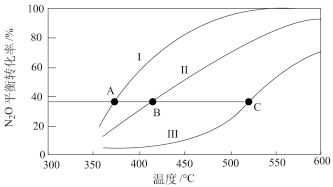
【推荐2】在四个恒容密闭容器中按下表相应量充入气体,发生反应2N2O 2N2(g)+O2(g),容器I、II、III中N2O平衡转化率如图所示。下列说法正确的是
2N2(g)+O2(g),容器I、II、III中N2O平衡转化率如图所示。下列说法正确的是
 2N2(g)+O2(g),容器I、II、III中N2O平衡转化率如图所示。下列说法正确的是
2N2(g)+O2(g),容器I、II、III中N2O平衡转化率如图所示。下列说法正确的是| 容器 | 容积/L | 起始物质的量/mol | ||
| N2O | N2 | O2 | ||
| I | V1 | 0.1 | 0 | 0 |
| II | 1.0 | 0.1 | 0 | 0 |
| III | V3 | 0.1 | 0 | 0 |
| IV | 1.0 | 0.06 | 0.06 | 0.04 |

| A.该反应的正反应为放热反应 |
| B.相同温度下反应时,平均反应速率:v(I)>v(III) |
| C.图中A、B、C三点处容器内总压强:pA(I)>pB(II)>pC(III) |
| D.470℃时气体在容器IV中进行反应,起始速率:v前(N2O)>v后(N2O) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】湿法提银工艺中,浸出的Ag+需加入Cl-进行沉淀。Ag+与Cl-可结合生成多种络合物,在水溶液中存在如下平衡:AgCl43-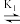 AgCl32-
AgCl32-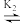 AgCl2-
AgCl2-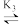 AgCl
AgCl Ag+。25℃时,平衡体系中含Ag微粒的分布系数δ随lgc(Cl-)的变化曲线如图所示。下列说法错误的是
Ag+。25℃时,平衡体系中含Ag微粒的分布系数δ随lgc(Cl-)的变化曲线如图所示。下列说法错误的是

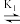 AgCl32-
AgCl32-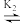 AgCl2-
AgCl2-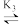 AgCl
AgCl Ag+。25℃时,平衡体系中含Ag微粒的分布系数δ随lgc(Cl-)的变化曲线如图所示。下列说法错误的是
Ag+。25℃时,平衡体系中含Ag微粒的分布系数δ随lgc(Cl-)的变化曲线如图所示。下列说法错误的是
| A.25℃时,Ksp(AgCl)=10-5.08 |
B.曲线c表示AgCl |
C.当c(Cl-)=10-2mol·L-1时,溶液中(AgCl )>c(Ag+)>c(AgCl )>c(Ag+)>c(AgCl ) ) |
| D.25℃时,平衡常数K2=10-0.2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温下,用 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的KCl、
的KCl、 溶液,所得的沉淀溶解平衡图象如图所示(不考虑的水解)。
溶液,所得的沉淀溶解平衡图象如图所示(不考虑的水解)。
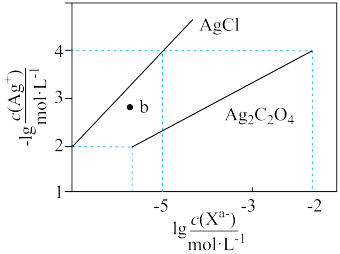
下列叙述正确的是
 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的KCl、
的KCl、 溶液,所得的沉淀溶解平衡图象如图所示(不考虑的水解)。
溶液,所得的沉淀溶解平衡图象如图所示(不考虑的水解)。
下列叙述正确的是
| A.b点表示AgCl的不饱和溶液 |
B. 数量级为 数量级为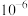 |
C. 的平衡常数为 的平衡常数为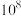 |
D.向 的混合液中滴入 的混合液中滴入 溶液时,先生成 溶液时,先生成 沉淀 沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】将2molH2和1molCO2充入体积为10L的恒容密闭容器中,在一定条件下发生反应:
①CO2(g)+ H2(g) CO(g) + H2O(g) △H1=+41.2kJ·moL-1;
CO(g) + H2O(g) △H1=+41.2kJ·moL-1;
②CO2(g)+ 3H2(g) CH3OH(g) + H2O(g) △H2=-49kJ·moL-1。
CH3OH(g) + H2O(g) △H2=-49kJ·moL-1。
反应100min后达到平衡,测得下表数据:下列说法正确的是
①CO2(g)+ H2(g)
 CO(g) + H2O(g) △H1=+41.2kJ·moL-1;
CO(g) + H2O(g) △H1=+41.2kJ·moL-1;②CO2(g)+ 3H2(g)
 CH3OH(g) + H2O(g) △H2=-49kJ·moL-1。
CH3OH(g) + H2O(g) △H2=-49kJ·moL-1。反应100min后达到平衡,测得下表数据:下列说法正确的是
| 温度 | 转化率(%) | 物质的量(mol) | ||
| H2 | CO2 | CH3OH | CO | |
| 240℃ | 10 | 0.05 | 0.05 | |
| A.升高温度,反应①的平衡常数减小 |
| B.升高温度,CH3OH的含量提高 |
| C.H2转化率为10% |
| D.100min内,反应②的速率为v(CO2)=0.0001 mol·L-1·min-1 |
您最近一年使用:0次