一定条件下,向甲、乙、丙三个恒容容器中加入一定量初始物质,发生反应C(s)+H2O(g) CO(g)+H2(g) ∆H>0,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。
CO(g)+H2(g) ∆H>0,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。
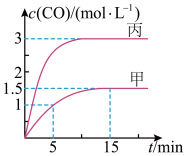
下列说法正确的是
 CO(g)+H2(g) ∆H>0,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。
CO(g)+H2(g) ∆H>0,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。
| 容器 | 甲 | 乙 | 丙 |
| 容积/L | 0.5 | 0.5 | V |
| 温度/K |  |  |  |
| 起始量 | 1molC(s),1mol H2O (g) | 1molCO(g),1mol H2(g) | 3molC(s),2mol H2O (g) |
A.甲容器中,从反应开始到平衡的平均反应速率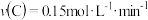 |
| B.温度为T1时,反应的平衡常数K=9 mol∙L-1, |
C.乙容器中,若平衡时n(C)=0.19mol,则 |
| D.V=0.4 |
更新时间:2022-10-24 10:41:02
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在四个不同的密闭容器中,采用不同条件进行反应N2(g)+3H2(g) 2NH3(g),根据下列在相同时间内测定的结果判断,生成氨的速率最快的是
2NH3(g),根据下列在相同时间内测定的结果判断,生成氨的速率最快的是
 2NH3(g),根据下列在相同时间内测定的结果判断,生成氨的速率最快的是
2NH3(g),根据下列在相同时间内测定的结果判断,生成氨的速率最快的是| A.v(N2)=0.2mol/(L∙s) | B.v(NH3)=0.8mol/(L∙min) |
| C.v(H2)=0.3mol/(L∙s) | D.v(H2)=1.3mol/(L∙min) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】将5.6 g铁粉投入盛有100mL 2mol/L稀硫酸的烧杯中,经2min反应完全。如果反应前后浓液的体积不变,则该反应的平均反应速率可表示为
| A.v(Fe)=0.5mol/(L·min) | B.v(H2SO4)=1mol/(L·min) |
| C.v(FeSO4)=0.5mol/(L·min) | D.v(H2)=0.5mol/(L·min) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列变化不能用勒夏特列原理解释的是
| A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 |
| B.工业上合成氨要在高温、催化剂条件下进行 |
| C.实验室可用排饱和食盐水的方法收集氯气 |
D.向氯水中加 后,溶液漂白性增强 后,溶液漂白性增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关实验的说法正确的是
A.可用加热的方法除去 中混有的 中混有的 固体 固体 |
B.将盛有 气体的密闭烧瓶放入热水中,红色加深 气体的密闭烧瓶放入热水中,红色加深 |
C.用盐酸滴定 溶液时,滴入盐酸,当含有酚酞的 溶液时,滴入盐酸,当含有酚酞的 溶液红色刚好褪去,即停止滴定 溶液红色刚好褪去,即停止滴定 |
| D.测定中和反应的反应热时,温度计测量酸的温度后可直接测量碱的温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
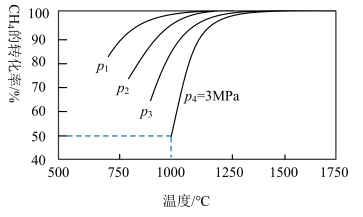
【推荐1】工业合成氨的原料气来源于化石燃料,如采用甲烷与二氧化碳反应:
 。(在某容器中,充入等物质的量的
。(在某容器中,充入等物质的量的 和
和 )下列说法正确的是( )
)下列说法正确的是( )

 。(在某容器中,充入等物质的量的
。(在某容器中,充入等物质的量的 和
和 )下列说法正确的是( )
)下列说法正确的是( )
A.该原料气的制备反应为放热反应, |
B.压强关系: |
C.恒温、恒压条件下,充入 ,平衡向逆反应方向移动 ,平衡向逆反应方向移动 |
D. 时的平衡常数 时的平衡常数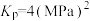 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】t ℃时,在一固定容积的密闭容器中发生反应:A(g)+B(g) C(s) ΔH<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
C(s) ΔH<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
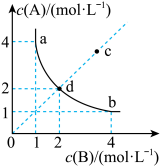
 C(s) ΔH<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
C(s) ΔH<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
| A.t ℃时,该反应的平衡常数值为0.35 |
| B.c点没有达到平衡,此时反应向逆向进行 |
| C.若c为平衡点,则此时容器内的温度高于t ℃ |
| D.t ℃时,直线cd上的点均为平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定温度下,向体积为2 L的恒容密闭容器里充入2 mol M和一定量的N,发生反应: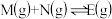 。当反应进行到4 min时达到平衡,测得M的浓度为0.2 mol·L-1,气体的平衡压强是起始压强的
。当反应进行到4 min时达到平衡,测得M的浓度为0.2 mol·L-1,气体的平衡压强是起始压强的 。下列说法中错误的是
。下列说法中错误的是
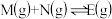 。当反应进行到4 min时达到平衡,测得M的浓度为0.2 mol·L-1,气体的平衡压强是起始压强的
。当反应进行到4 min时达到平衡,测得M的浓度为0.2 mol·L-1,气体的平衡压强是起始压强的 。下列说法中错误的是
。下列说法中错误的是| A.M的平衡转化率为80% | B.起始时,N的加入量为2.8 mol |
C.前4 min内,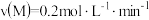 | D.2 min时,E的物质的量是0.8 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向 刚性密闭容器中充入
刚性密闭容器中充入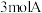 气体,发生反应
气体,发生反应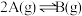 。不同温度下,反应达平衡,平衡体系中各物质的物质的量分数如下表:(已知A有颜色,B无色)
。不同温度下,反应达平衡,平衡体系中各物质的物质的量分数如下表:(已知A有颜色,B无色)
下列说法不正确的是
 刚性密闭容器中充入
刚性密闭容器中充入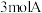 气体,发生反应
气体,发生反应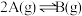 。不同温度下,反应达平衡,平衡体系中各物质的物质的量分数如下表:(已知A有颜色,B无色)
。不同温度下,反应达平衡,平衡体系中各物质的物质的量分数如下表:(已知A有颜色,B无色) ℃ ℃ | 25 | 40 | 50 | 60 |
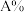 | 20 | 25 | 40 | 66 |
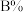 | 80 | 75 | 60 | 34 |
A.25℃,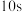 反应达平衡, 反应达平衡, 速率 速率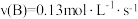 |
| B.室温时,将此容器放入冰水中,颜色变浅 |
| C.向40℃的平衡体系中再充入A,达新平衡时平均分子量减小 |
D.50℃达平衡时,A的转化率为 |
您最近一年使用:0次

 反应中,表示该反应速率最快的是
反应中,表示该反应速率最快的是

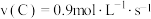

 在一定条件下反应生成化合物B与
在一定条件下反应生成化合物B与 ,其反应历程如图所示,其中TS表示过渡态,I表示中间体。下列说法正确的是
,其反应历程如图所示,其中TS表示过渡态,I表示中间体。下列说法正确的是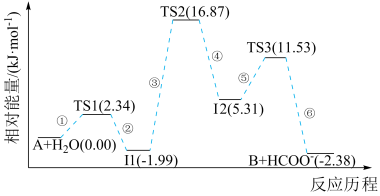

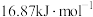
 的恒容密闭容器M(恒温
的恒容密闭容器M(恒温 )、N(起始
)、N(起始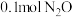 和
和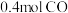 及相同催化剂发生反应:
及相同催化剂发生反应: 。实验测得两个容器中
。实验测得两个容器中 的物质的量随时间的变化关系如表所示。该反应的反应速率
的物质的量随时间的变化关系如表所示。该反应的反应速率 、
、 (
( 、
、 分别是正、逆反应的速率常数)。下列说法错误的是
分别是正、逆反应的速率常数)。下列说法错误的是







 时
时


