工业上常用天然气作为制备CH3OH的原料。已知:
①CH4(g)+O2(g) CO(g)+H2(g)+H2O(g) △H=-321.5kJ•mol-1
CO(g)+H2(g)+H2O(g) △H=-321.5kJ•mol-1
②CH4(g)+H2O(g) CO(g)+3H2(g) △H=+250.3kJ•mol-1
CO(g)+3H2(g) △H=+250.3kJ•mol-1
③CO(g)+2H2(g) CH3OH(g) △H=-90.0kJ•mol-1
CH3OH(g) △H=-90.0kJ•mol-1
(1)CH4(g)与O2(g)化合生成CH3OH(g)的热化学方程式是____ 。
(2)利用③的原理,向密闭容器中充入1molCO与2molH2,在不同压强下合成甲醇。CO的平衡转化率与温度、压强(p)的关系如图所示:
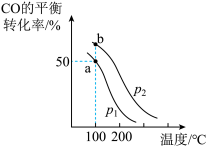
①压强p1____ p2(填“<”或“>”)。
②根据图中a点的数据(此时容器体积为1L),将表中空格处填写完整。
③若反应刚好至a点时,所需时间为tmin,则tmin内用H2表示该反应的化学反应速率v(H2)=____ 。
④b点时,该反应的平衡常数K=____ 。
①CH4(g)+O2(g)
 CO(g)+H2(g)+H2O(g) △H=-321.5kJ•mol-1
CO(g)+H2(g)+H2O(g) △H=-321.5kJ•mol-1②CH4(g)+H2O(g)
 CO(g)+3H2(g) △H=+250.3kJ•mol-1
CO(g)+3H2(g) △H=+250.3kJ•mol-1③CO(g)+2H2(g)
 CH3OH(g) △H=-90.0kJ•mol-1
CH3OH(g) △H=-90.0kJ•mol-1(1)CH4(g)与O2(g)化合生成CH3OH(g)的热化学方程式是
(2)利用③的原理,向密闭容器中充入1molCO与2molH2,在不同压强下合成甲醇。CO的平衡转化率与温度、压强(p)的关系如图所示:

①压强p1
②根据图中a点的数据(此时容器体积为1L),将表中空格处填写完整。
| c(CO) | c(H2) | c(CH3OH) | |
| 起始时 | 1 | 2 | 0 |
| 转化 | 0.5 | ||
| 平衡时 |
④b点时,该反应的平衡常数K=
更新时间:2022-11-05 16:39:56
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】二氧化碳是常见的温室气体,其回收利用是环保领域研究的热点课题。
Ⅰ.CO2可以与H2反应合成C2H4,该转化分两步进行:
第一步:CO2(g)+H2(g) CO(g)+H2O(g)△H=+41.3kJ·mol-1
CO(g)+H2O(g)△H=+41.3kJ·mol-1
第二步:2CO(g)+4H2(g) C2H4(g)+2H2O(g)△H=–210.5kJ·mol-1
C2H4(g)+2H2O(g)△H=–210.5kJ·mol-1
(1)CO2与H2反应反应合成乙烯的热化学方程式为___ 。
(2)一定条件下的密闭容器中,要提高CO2合成乙烯的转化率,可以采取的措施是____ (填标号)。
①减小压强②增大H2的浓度③加入适当催化剂④分离出H2O(g)
(3)已知温度对CO2合成乙烯的平衡转化率及催化剂的催化效率的影响如图所示,下列说法正确的是____ (填标号)。

①N点的速率最大
②M点的平衡常数比N点的平衡常数大
③温度低于250℃时,随温度升高乙烯的平衡产率增大
④实际反应尽可能在较低的温度下进行,以提高CO2的转化率
Ⅱ.研究表明CO2和H2在一定条件下可以合成甲醇,反应方程式为CO2(g)+3H2(g) CH3OH(g)+H2O(g)[反应①]。一定条件下,往2L恒容密闭容器中充入2.0molCO2和4.0molH2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化如图所示:
CH3OH(g)+H2O(g)[反应①]。一定条件下,往2L恒容密闭容器中充入2.0molCO2和4.0molH2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化如图所示:

(4)催化效果最佳的是催化剂____ (填“A”、“B”或“C”)。
(5)T2温度下,若反应进行10min达到图中a点状态,用CO2的浓度表示的反应速率v(CO2)=____ 。
(6)图中b点已达平衡状态,则该温度下反应的平衡常数K=____ 。
(7)在某催化剂作用下,CO2和H2除发生反应①外,还发生如下反应:CO2(g)+H2(g) CO(g)+H2O(g)[反应②]。维持压强不变,按固定初始投料比将CO2和H2按一定流速通过该催化剂,经过相同时间测得如下实验数据:
CO(g)+H2O(g)[反应②]。维持压强不变,按固定初始投料比将CO2和H2按一定流速通过该催化剂,经过相同时间测得如下实验数据:
注:甲醇的选择性是指发生反应的CO2中转化为甲醇的百分比。表中数据说明,升高温度CO2的实际转化率提高而甲醇的选择性降低,其原因是____ 。
Ⅰ.CO2可以与H2反应合成C2H4,该转化分两步进行:
第一步:CO2(g)+H2(g)
 CO(g)+H2O(g)△H=+41.3kJ·mol-1
CO(g)+H2O(g)△H=+41.3kJ·mol-1第二步:2CO(g)+4H2(g)
 C2H4(g)+2H2O(g)△H=–210.5kJ·mol-1
C2H4(g)+2H2O(g)△H=–210.5kJ·mol-1(1)CO2与H2反应反应合成乙烯的热化学方程式为
(2)一定条件下的密闭容器中,要提高CO2合成乙烯的转化率,可以采取的措施是
①减小压强②增大H2的浓度③加入适当催化剂④分离出H2O(g)
(3)已知温度对CO2合成乙烯的平衡转化率及催化剂的催化效率的影响如图所示,下列说法正确的是

①N点的速率最大
②M点的平衡常数比N点的平衡常数大
③温度低于250℃时,随温度升高乙烯的平衡产率增大
④实际反应尽可能在较低的温度下进行,以提高CO2的转化率
Ⅱ.研究表明CO2和H2在一定条件下可以合成甲醇,反应方程式为CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)[反应①]。一定条件下,往2L恒容密闭容器中充入2.0molCO2和4.0molH2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化如图所示:
CH3OH(g)+H2O(g)[反应①]。一定条件下,往2L恒容密闭容器中充入2.0molCO2和4.0molH2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化如图所示:
(4)催化效果最佳的是催化剂
(5)T2温度下,若反应进行10min达到图中a点状态,用CO2的浓度表示的反应速率v(CO2)=
(6)图中b点已达平衡状态,则该温度下反应的平衡常数K=
(7)在某催化剂作用下,CO2和H2除发生反应①外,还发生如下反应:CO2(g)+H2(g)
 CO(g)+H2O(g)[反应②]。维持压强不变,按固定初始投料比将CO2和H2按一定流速通过该催化剂,经过相同时间测得如下实验数据:
CO(g)+H2O(g)[反应②]。维持压强不变,按固定初始投料比将CO2和H2按一定流速通过该催化剂,经过相同时间测得如下实验数据:| T(K) | CO2实际转化率(%) | 甲醇选择性(%) |
| 543 | 12.3 | 42.3 |
| 553 | 15.3 | 39.1 |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】反应 过程中的能量变化如下图所示,回答下列问题。
过程中的能量变化如下图所示,回答下列问题。_______ 热反应(填“吸”、“放”)。
②在反应体系中加入催化剂,反应速率增大,
_______ ,
_______ (填增大”、“减小”或“不变”)。
③当反应达到平衡时,升高温度,A的转化率_______ (填“增大”、“减小”或“不变”)。
(2)一定条件下,一氧化碳与氢气反应可以合成甲醇。已知:
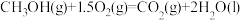
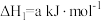
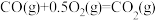
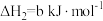
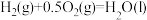
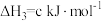
则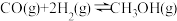

_______  (用a、b、c表示)。
(用a、b、c表示)。
(3)一定压强下,在容积为 的密闭容器中充入
的密闭容器中充入 与
与 ,在催化剂作用下发生反应:
,在催化剂作用下发生反应: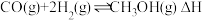 ,平衡转化率与温度、压强的关系如图所示。则
,平衡转化率与温度、压强的关系如图所示。则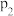
_______  (填“>”、“<”或“=”);
(填“>”、“<”或“=”);
 过程中的能量变化如下图所示,回答下列问题。
过程中的能量变化如下图所示,回答下列问题。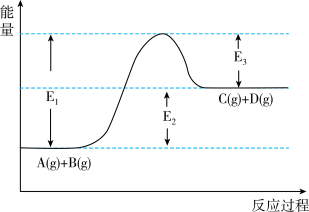
②在反应体系中加入催化剂,反应速率增大,


③当反应达到平衡时,升高温度,A的转化率
(2)一定条件下,一氧化碳与氢气反应可以合成甲醇。已知:
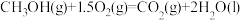
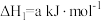
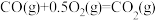
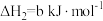
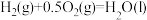
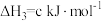
则
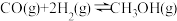

 (用a、b、c表示)。
(用a、b、c表示)。(3)一定压强下,在容积为
 的密闭容器中充入
的密闭容器中充入 与
与 ,在催化剂作用下发生反应:
,在催化剂作用下发生反应: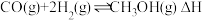 ,平衡转化率与温度、压强的关系如图所示。则
,平衡转化率与温度、压强的关系如图所示。则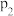
 (填“>”、“<”或“=”);
(填“>”、“<”或“=”);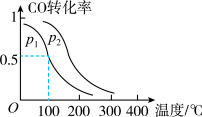
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐3】CO2与人类息息相关。近年来,为了缓解温室效应,CO2的资源化利用是化学研究热点之一。科学家提出了多种回收和利用CO2的方案。
(1)已知:①2NaOH(s)+CO2(g)=Na2CO3(s)+H2O(g) △H1=-127.4kJ/mol
②NaOH(s)+CO2(g)=NaHCO3(s) △H2=-131.5kJ/mol
则:反应2NaHCO3(s)=Na2CO3(s)+H2O(g)+CO2(g) △H3=_______ kJ/mol。
(2)人体血液中存在平衡CO2+H2O H2CO3
H2CO3 H++HCO
H++HCO ,当人呼吸过快或过深,体内失去二氧化碳太多,引发呼吸性碱中毒,导致手脚发麻、头晕。试用平衡移动原理解释上述现象:
,当人呼吸过快或过深,体内失去二氧化碳太多,引发呼吸性碱中毒,导致手脚发麻、头晕。试用平衡移动原理解释上述现象:_______ 。
(3)利用CO2制备CH4可以实现变废为宝,300℃时,向2L恒容密闭容器中充入2molCO2和8molH2发生反应: CO2(g)+4H2(g) CH4(g)+ 2H2O(g) △H4,混合气体中CH4的浓度与反应时间的关系如图所示,回答下列问题:
CH4(g)+ 2H2O(g) △H4,混合气体中CH4的浓度与反应时间的关系如图所示,回答下列问题:
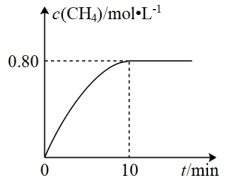
①下列说法正确的是_______ 。
A.容器内密度不变,说明反应达到平衡状态
B.容器内压强不变,说明反应达到平衡状态
C.断开2molC=O键的同时断开4molC-H键,说明反应达到平衡状态
D.300℃时,向平衡后的容器中再充入2molCO2和8molH2,重新达到平衡时CH4的浓度小于1.6mol/L
②从反应开始到10min,H2的平均反应速率v(H2)=_______ 。
③300℃时,反应的平衡常数K=_______ 。
④500℃该反应达到平衡时,上述容器中有1.6molCO2、2.0molH2、5.6molCH4、4.0molH2O。则△H4_______ 0(填“>”“<”或“=”)
(1)已知:①2NaOH(s)+CO2(g)=Na2CO3(s)+H2O(g) △H1=-127.4kJ/mol
②NaOH(s)+CO2(g)=NaHCO3(s) △H2=-131.5kJ/mol
则:反应2NaHCO3(s)=Na2CO3(s)+H2O(g)+CO2(g) △H3=
(2)人体血液中存在平衡CO2+H2O
 H2CO3
H2CO3 H++HCO
H++HCO ,当人呼吸过快或过深,体内失去二氧化碳太多,引发呼吸性碱中毒,导致手脚发麻、头晕。试用平衡移动原理解释上述现象:
,当人呼吸过快或过深,体内失去二氧化碳太多,引发呼吸性碱中毒,导致手脚发麻、头晕。试用平衡移动原理解释上述现象:(3)利用CO2制备CH4可以实现变废为宝,300℃时,向2L恒容密闭容器中充入2molCO2和8molH2发生反应: CO2(g)+4H2(g)
 CH4(g)+ 2H2O(g) △H4,混合气体中CH4的浓度与反应时间的关系如图所示,回答下列问题:
CH4(g)+ 2H2O(g) △H4,混合气体中CH4的浓度与反应时间的关系如图所示,回答下列问题:
①下列说法正确的是
A.容器内密度不变,说明反应达到平衡状态
B.容器内压强不变,说明反应达到平衡状态
C.断开2molC=O键的同时断开4molC-H键,说明反应达到平衡状态
D.300℃时,向平衡后的容器中再充入2molCO2和8molH2,重新达到平衡时CH4的浓度小于1.6mol/L
②从反应开始到10min,H2的平均反应速率v(H2)=
③300℃时,反应的平衡常数K=
④500℃该反应达到平衡时,上述容器中有1.6molCO2、2.0molH2、5.6molCH4、4.0molH2O。则△H4
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐1】在2 L密闭容器内,800 ℃时反应2NO(g)+O2(g) ⇌2NO2(g)体系中,n(NO)随时间的变化如表所示:
(1)在第5 s时,NO的转化率为_________________________________ 。
(2)如图中表示NO2变化曲线的是______________________ 。
用O2表示0~2 s内该反应的平均速率v=______________________ 。
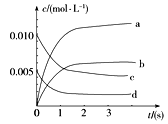
(3)能说明该反应已达到平衡状态的是________ 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
| 时间/(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)在第5 s时,NO的转化率为
(2)如图中表示NO2变化曲线的是
用O2表示0~2 s内该反应的平均速率v=

(3)能说明该反应已达到平衡状态的是
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐2】Ⅰ.在5L的密闭容器内充入10mol A气体和5mol B气体发生如下反应:
2A(g) + B(g) 2C(g),2s后达到平衡,此时测得平衡混合物中C的浓度为0.6mol/L。则:
2C(g),2s后达到平衡,此时测得平衡混合物中C的浓度为0.6mol/L。则:
(1)用A的浓度变化表示该反应的平均反应速率_____________ ;
(2)达到平衡后A的转化率为_____________ 。
(3)平衡混合物中B的浓度为_____________ 。
Ⅱ.在密闭容器中进行下列反应:CO2(g)+C(s) 2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡及指定物质的浓度如何变化?
2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡及指定物质的浓度如何变化?
(4)增加C(s),平衡___________ (填“正向移动、逆向移动、不移动”,下同)。
(5)减小密闭容器容积,保持温度不变,则平衡___________ ,c(CO)___________ (填“增大、减小、不变”)
(6)通入N2,保持密闭容器容积和温度不变,则平衡___________ 。
(7)保持密闭容器容积不变,升高温度,则平衡___________ 。
2A(g) + B(g)
 2C(g),2s后达到平衡,此时测得平衡混合物中C的浓度为0.6mol/L。则:
2C(g),2s后达到平衡,此时测得平衡混合物中C的浓度为0.6mol/L。则:(1)用A的浓度变化表示该反应的平均反应速率
(2)达到平衡后A的转化率为
(3)平衡混合物中B的浓度为
Ⅱ.在密闭容器中进行下列反应:CO2(g)+C(s)
 2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡及指定物质的浓度如何变化?
2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡及指定物质的浓度如何变化?(4)增加C(s),平衡
(5)减小密闭容器容积,保持温度不变,则平衡
(6)通入N2,保持密闭容器容积和温度不变,则平衡
(7)保持密闭容器容积不变,升高温度,则平衡
您最近一年使用:0次
【推荐3】I.按要求填写下列空白:
(1)在常温常压下,1 g 氢气在足量氯气中完全燃烧生成氯化氢气体,放出91.5 kJ 的热量。写出相应的热化学方程式为___________ 。
(2)已知: ①2Mg(s) + O2(g) = 2MgO(s) ΔH2 = -1203.4 kJ/mol
②C(s) + O2(g) = CO2(g) ΔH1 = -393.5 kJ/mol
写出Mg与CO2反应的热化学方程式___________ 。
(3)氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:___________ 。
II.某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白。

(4)该反应的化学方程式为___________ 。
(5)反应开始至2 min,气体Z的平均反应速率v(Z)=___________ 。
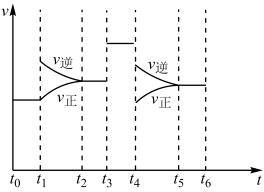
(6)上述反应在t1~t6内反应速率与时间图象如图所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是___________ (填字母)。
(1)在常温常压下,1 g 氢气在足量氯气中完全燃烧生成氯化氢气体,放出91.5 kJ 的热量。写出相应的热化学方程式为
(2)已知: ①2Mg(s) + O2(g) = 2MgO(s) ΔH2 = -1203.4 kJ/mol
②C(s) + O2(g) = CO2(g) ΔH1 = -393.5 kJ/mol
写出Mg与CO2反应的热化学方程式
(3)氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:
II.某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白。

(4)该反应的化学方程式为
(5)反应开始至2 min,气体Z的平均反应速率v(Z)=
(6)上述反应在t1~t6内反应速率与时间图象如图所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是___________ (填字母)。

| A.在t1时增大了压强 |
| B.在t3时加入催化剂 |
| C.在t4时降低了温度 |
| D.t2~t3时X的转化率最高 |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐1】硫化氢的回收、转化是环境保护和资源利用的重要研究课题。
(1) 溶于水分步电离出
溶于水分步电离出 、
、 。产生
。产生 的电离方程式是
的电离方程式是___________ 。
(2)脱除 有多种方法,其中沉淀氧化法过程如图所示:
有多种方法,其中沉淀氧化法过程如图所示:

a.反应Ⅱ的离子方程式是___________ 。
b.资料显示 在反应Ⅲ中起催化作用:
在反应Ⅲ中起催化作用:
i.
ii.___________ (将反应ii补充完整)
(3)已知:
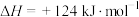 ,若反应体系达到平衡后,各物质的浓度在不同条件下(只改变一种条件)的变化状况如图所示(第10min到14min的
,若反应体系达到平衡后,各物质的浓度在不同条件下(只改变一种条件)的变化状况如图所示(第10min到14min的 浓度变化曲线未表示出):
浓度变化曲线未表示出):

①第2min反应温度T(2)与第8min反应温度T(8)的高低:T(2)___________ (填“<”、“>”或“=”)T(8);第10min时反应改变的条件是___________ 。
(4)页岩气的主要成分为 ,请回答下列问题:
,请回答下列问题:
①已知甲烷的燃烧热为890kJ/mol; 与
与 反应生成NO的过程如下:
反应生成NO的过程如下:

则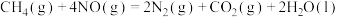 ΔH=
ΔH=___________ kJ/mol。
②页岩气可用于生产合成气(CO和 )其反应的热化学方程式为
)其反应的热化学方程式为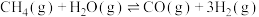 ΔH=+206.2kJ/mol。对于气相反应,用各组分的平衡压强(p)表示平衡常教(记作Kp),则生产合成气的
ΔH=+206.2kJ/mol。对于气相反应,用各组分的平衡压强(p)表示平衡常教(记作Kp),则生产合成气的 =
=___________ (写出表达式),你认为可同时提高化学反应速率和 转化率的措施是
转化率的措施是___________ (答出一条即可)。
③在某一给定进料比的情况下,温度、压强对平衡时 物质的量分数的影响如图所示。
物质的量分数的影响如图所示。

由图可知,在相同温度下, 的转化率随压强的增大而
的转化率随压强的增大而___________ (填“增大”“小”或“不变”)。若要达到 的物质的量分数>65%,以下条件中最合适的是
的物质的量分数>65%,以下条件中最合适的是___________ (填序号)。
a.600℃,0.2MPa b.600℃,0.9MPa c.700℃,0.9MPa d.800℃,1.5MPa
(1)
 溶于水分步电离出
溶于水分步电离出 、
、 。产生
。产生 的电离方程式是
的电离方程式是(2)脱除
 有多种方法,其中沉淀氧化法过程如图所示:
有多种方法,其中沉淀氧化法过程如图所示:
a.反应Ⅱ的离子方程式是
b.资料显示
 在反应Ⅲ中起催化作用:
在反应Ⅲ中起催化作用:i.

ii.
(3)已知:

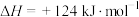 ,若反应体系达到平衡后,各物质的浓度在不同条件下(只改变一种条件)的变化状况如图所示(第10min到14min的
,若反应体系达到平衡后,各物质的浓度在不同条件下(只改变一种条件)的变化状况如图所示(第10min到14min的 浓度变化曲线未表示出):
浓度变化曲线未表示出):
①第2min反应温度T(2)与第8min反应温度T(8)的高低:T(2)
(4)页岩气的主要成分为
 ,请回答下列问题:
,请回答下列问题:①已知甲烷的燃烧热为890kJ/mol;
 与
与 反应生成NO的过程如下:
反应生成NO的过程如下:
则
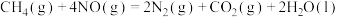 ΔH=
ΔH=②页岩气可用于生产合成气(CO和
 )其反应的热化学方程式为
)其反应的热化学方程式为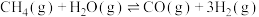 ΔH=+206.2kJ/mol。对于气相反应,用各组分的平衡压强(p)表示平衡常教(记作Kp),则生产合成气的
ΔH=+206.2kJ/mol。对于气相反应,用各组分的平衡压强(p)表示平衡常教(记作Kp),则生产合成气的 =
= 转化率的措施是
转化率的措施是③在某一给定进料比的情况下,温度、压强对平衡时
 物质的量分数的影响如图所示。
物质的量分数的影响如图所示。
由图可知,在相同温度下,
 的转化率随压强的增大而
的转化率随压强的增大而 的物质的量分数>65%,以下条件中最合适的是
的物质的量分数>65%,以下条件中最合适的是a.600℃,0.2MPa b.600℃,0.9MPa c.700℃,0.9MPa d.800℃,1.5MPa
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
I.下表中的数据是破坏1 物质中的化学键所消耗的能量,回答下列问题
物质中的化学键所消耗的能量,回答下列问题
(1)下列氢化物中最稳定的是___________ (填字母代号)。
A. B.
B. C.
C.
(2)按照反应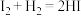 ,生成2
,生成2

_________ (填“吸收”或“放出”)的热量为_______  。
。
II.某温度时,在一个2L的密闭容器中, A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据填写下列空白:

(3)该反应的化学方程式为__________________ ;
(4)从开始至2min,A的平均反应速率为_____________ ;
(5)2min反应达平衡容器内混合气体的平均相对分子质量比起始时___________ (填“大”,“小”或“相等”,下同),混合气体密度比起始时___________ 。
(6)在某一时刻采取下列措施能使该反应速率减小的是___________。
(7)下列叙述能说明该反应已达到化学平衡状态的是___________ (填序号);
A.A、B、C的物质的量之比为3∶1∶3
B.相同时间内消耗3 A,同时生成n
A,同时生成n B
B
C.容器内的压强不再变化
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
I.下表中的数据是破坏1
 物质中的化学键所消耗的能量,回答下列问题
物质中的化学键所消耗的能量,回答下列问题物质 |
|
|
|
|
|
|
|
键能/ | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
A.
 B.
B. C.
C.
(2)按照反应
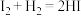 ,生成2
,生成2

 。
。II.某温度时,在一个2L的密闭容器中, A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据填写下列空白:

(3)该反应的化学方程式为
(4)从开始至2min,A的平均反应速率为
(5)2min反应达平衡容器内混合气体的平均相对分子质量比起始时
(6)在某一时刻采取下列措施能使该反应速率减小的是___________。
| A.加催化剂 | B.降低温度 |
| C.容积不变,充入A | D.容积不变,从容器中分离出A |
A.A、B、C的物质的量之比为3∶1∶3
B.相同时间内消耗3
 A,同时生成n
A,同时生成n B
BC.容器内的压强不再变化
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐3】乙醇水蒸气重整制氢是制备氢气的常用方法,体系中发生的主要反应如下:
I.C2H5OH(g)+H2O(g)=2CO(g)+4H2(g) △H1
II.C2H5OH(g)+3H2O(g)=2CO2(g)+6H2(g) △H2=+173 kJ∙mol−1
III.CO(g)+H2O(g)=CO2(g)+H2(g) △H3=−41.2 kJ∙mol−1
IV.C2H5OH(g)+2H2(g)=2CH4(g)+H2O(g) △H4=−156.2kJ∙mol−1
(1)△H1=_______ kJ∙mol−1。
(2)压强为100kPa的条件下,图1是平衡时体系中各产物的物质的量分数与温度的关系,图2是H2的平衡产率与温度及起始时 的关系。
的关系。

①图1中c线对应的产物为_______ (填“CO2”、“H2”或“CH4”)。
②图2中B点H2的产率与A点相等的原因是_______ 。
(3)反应温度T℃、0.1MPa的恒压密闭容器中,充入1molCH3CH2OH(g)和xmolH2O(g),若只发生反应CH3CH2OH(g)+3H2O(g) 2CO2(g)+6H2(g),平衡时,乙醇转化率为α,则该反应的平衡常数Kp=
2CO2(g)+6H2(g),平衡时,乙醇转化率为α,则该反应的平衡常数Kp=_______ (列出计算式即可。)
(4)选择合适的催化剂能够加快反应的速率,请在下图画出上述反应I.C2H5OH(g)+H2O(g)=2CO(g)+4H2(g)不使用催化剂和使用催化剂反应过程中体系能量的变化图_______ 。

I.C2H5OH(g)+H2O(g)=2CO(g)+4H2(g) △H1
II.C2H5OH(g)+3H2O(g)=2CO2(g)+6H2(g) △H2=+173 kJ∙mol−1
III.CO(g)+H2O(g)=CO2(g)+H2(g) △H3=−41.2 kJ∙mol−1
IV.C2H5OH(g)+2H2(g)=2CH4(g)+H2O(g) △H4=−156.2kJ∙mol−1
(1)△H1=
(2)压强为100kPa的条件下,图1是平衡时体系中各产物的物质的量分数与温度的关系,图2是H2的平衡产率与温度及起始时
 的关系。
的关系。
①图1中c线对应的产物为
②图2中B点H2的产率与A点相等的原因是
(3)反应温度T℃、0.1MPa的恒压密闭容器中,充入1molCH3CH2OH(g)和xmolH2O(g),若只发生反应CH3CH2OH(g)+3H2O(g)
 2CO2(g)+6H2(g),平衡时,乙醇转化率为α,则该反应的平衡常数Kp=
2CO2(g)+6H2(g),平衡时,乙醇转化率为α,则该反应的平衡常数Kp=(4)选择合适的催化剂能够加快反应的速率,请在下图画出上述反应I.C2H5OH(g)+H2O(g)=2CO(g)+4H2(g)不使用催化剂和使用催化剂反应过程中体系能量的变化图

您最近一年使用:0次
【推荐1】汽车尾气污染、室内污染是与人们生活密切相关的问题。请按要求回答下列问题:

(1)利用某分子筛作催化剂,NH3可脱除工厂废气中的NO、NO2,反应机理如图1所示。A包含的物质为N2和___________ (填化学式)。
(2)汽车尾气净化的主要原理为2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH<0,若该反应在绝热、恒容的密闭体系中进行,所列示意图(如图2)中t1时刻是否处于平衡状态?
2CO2(g)+N2(g) ΔH<0,若该反应在绝热、恒容的密闭体系中进行,所列示意图(如图2)中t1时刻是否处于平衡状态?________ (选填“是”或“否”),原因是___________ 。
(3)工业合成NH3的反应,解决了世界约三分之一的人口粮食问题。已知:N2+3H2 2NH3(ΔH<0),500℃时,向容积为2L的密闭容器中通入1molN2和3molH2,模拟合成氨的反应。随着反应的进行,合成氨的正反应速率与NH3的体积分数的关系如图3所示,若降低温度再次达到平衡时,可能的点为
2NH3(ΔH<0),500℃时,向容积为2L的密闭容器中通入1molN2和3molH2,模拟合成氨的反应。随着反应的进行,合成氨的正反应速率与NH3的体积分数的关系如图3所示,若降低温度再次达到平衡时,可能的点为___________ (从点“A、B、C、D”中选择)。
(4)将CO2和H2混合,在一定温度下可以制取甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0,往2L恒容密闭容器中充入1molCO2和3molH2,在不同催化剂作用下发生反应I、反应II与反应III,相同时间内CO2的转化率随温度变化如图4所示:
CH3OH(g)+H2O(g) ΔH<0,往2L恒容密闭容器中充入1molCO2和3molH2,在不同催化剂作用下发生反应I、反应II与反应III,相同时间内CO2的转化率随温度变化如图4所示:
①反应I、反应II与反应III中催化剂效果最佳的是___________ (选填“反应I”“反应II”或“反应III”)。
②若此反应在a点时达到化学平衡状态。则此时该反应的化学平衡常数为___________ 。(计算结果保留到小数点后一位)

(1)利用某分子筛作催化剂,NH3可脱除工厂废气中的NO、NO2,反应机理如图1所示。A包含的物质为N2和
(2)汽车尾气净化的主要原理为2NO(g)+2CO(g)
 2CO2(g)+N2(g) ΔH<0,若该反应在绝热、恒容的密闭体系中进行,所列示意图(如图2)中t1时刻是否处于平衡状态?
2CO2(g)+N2(g) ΔH<0,若该反应在绝热、恒容的密闭体系中进行,所列示意图(如图2)中t1时刻是否处于平衡状态?(3)工业合成NH3的反应,解决了世界约三分之一的人口粮食问题。已知:N2+3H2
 2NH3(ΔH<0),500℃时,向容积为2L的密闭容器中通入1molN2和3molH2,模拟合成氨的反应。随着反应的进行,合成氨的正反应速率与NH3的体积分数的关系如图3所示,若降低温度再次达到平衡时,可能的点为
2NH3(ΔH<0),500℃时,向容积为2L的密闭容器中通入1molN2和3molH2,模拟合成氨的反应。随着反应的进行,合成氨的正反应速率与NH3的体积分数的关系如图3所示,若降低温度再次达到平衡时,可能的点为(4)将CO2和H2混合,在一定温度下可以制取甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH<0,往2L恒容密闭容器中充入1molCO2和3molH2,在不同催化剂作用下发生反应I、反应II与反应III,相同时间内CO2的转化率随温度变化如图4所示:
CH3OH(g)+H2O(g) ΔH<0,往2L恒容密闭容器中充入1molCO2和3molH2,在不同催化剂作用下发生反应I、反应II与反应III,相同时间内CO2的转化率随温度变化如图4所示:①反应I、反应II与反应III中催化剂效果最佳的是
②若此反应在a点时达到化学平衡状态。则此时该反应的化学平衡常数为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】CO和NO是汽车尾气中的主要污染物,易引起酸雨、温室效应和光化学烟雾等环境污染问题。随着我国机动车保有量的飞速发展,汽车尾气的有效处理变得迫在眉睫。其中的一种方法为2CO(g)+2NO(g)=N2(g)+2CO2(g),请回答下列问题:
(1)已知该反应为自发反应,则该反应的反应热△H___________ 0(填“>”或“<”或“=”)
(2)已知:N2 (g) + O2(g)=2NO(g) △H= a kJ•mol-1
C(s) + O2 (g)=CO2 (g) △H= b kJ•mol-1
2C(s) + O2 (g)=2CO(g) △H= c kJ•mol-1
则 2CO(g)+2NO(g)=N2 (g)+2CO2 (g) △H=___________ kJ•mol-1 (用含 a、b、c 的表达式表示)。
(3)一定温度下,将 2molCO、4molNO 充入一恒压密闭容器。已知起始压强为 1MPa,到达平衡时, 测得N2的物质的量为 0.5 mol,则:
①该温度此反应用平衡分压代替平衡浓度的平衡常数Kp=___________ (可用分数表示)
②该条件下,可判断此反应到达平衡的标志是___________
A.单位时间内,断裂 2 molC=O 同时形成 1 mol N≡N。
B.混合气体的密度不再改变。
C.混合气体的平均相对分子质量不再改变。
D.CO与NO的转化率比值不再改变。
(4)某研究小组探究催化剂对 CO、NO 转化的影响。将 CO 和 NO 以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中 N2的含量,从而确定尾气脱氮率(即 NO 的转化率),结果如图所示:

①由图可知:要达到最大脱氮率,该反应应采取的最佳实验条件为___________ ,
②高于 200℃,图中曲线 I 脱氮率随温度升高降低的主要原因为___________ 。
(5)已知常温下,Kb(NH3·H2O)=1.8×10-5,Ka1(H2CO3) =4.4×10-7,Ka2(H2CO3) =4.4×10-11。此温度下某氨水的浓度为 2mol/L,则溶液中c(OH-)=___________ mol/L,将脱氮反应后生成CO2通入氨水中使溶液恰好呈中性,则此时 =
=___________ 。(保留小数点后4位数字)
(6)电解NO制备NH4NO3,其工作原理如图所示:

写出阳极反应的电极反应方程式___________ ,为使电解产物全部转化为NH4NO3,需要补充物质A,A是___________ 。
(1)已知该反应为自发反应,则该反应的反应热△H
(2)已知:N2 (g) + O2(g)=2NO(g) △H= a kJ•mol-1
C(s) + O2 (g)=CO2 (g) △H= b kJ•mol-1
2C(s) + O2 (g)=2CO(g) △H= c kJ•mol-1
则 2CO(g)+2NO(g)=N2 (g)+2CO2 (g) △H=
(3)一定温度下,将 2molCO、4molNO 充入一恒压密闭容器。已知起始压强为 1MPa,到达平衡时, 测得N2的物质的量为 0.5 mol,则:
①该温度此反应用平衡分压代替平衡浓度的平衡常数Kp=
②该条件下,可判断此反应到达平衡的标志是
A.单位时间内,断裂 2 molC=O 同时形成 1 mol N≡N。
B.混合气体的密度不再改变。
C.混合气体的平均相对分子质量不再改变。
D.CO与NO的转化率比值不再改变。
(4)某研究小组探究催化剂对 CO、NO 转化的影响。将 CO 和 NO 以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中 N2的含量,从而确定尾气脱氮率(即 NO 的转化率),结果如图所示:

①由图可知:要达到最大脱氮率,该反应应采取的最佳实验条件为
②高于 200℃,图中曲线 I 脱氮率随温度升高降低的主要原因为
(5)已知常温下,Kb(NH3·H2O)=1.8×10-5,Ka1(H2CO3) =4.4×10-7,Ka2(H2CO3) =4.4×10-11。此温度下某氨水的浓度为 2mol/L,则溶液中c(OH-)=
 =
=(6)电解NO制备NH4NO3,其工作原理如图所示:

写出阳极反应的电极反应方程式
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】节能减排已经成为全社会的共识,有一种思路是将一氧化碳(CO)转化成可燃物质甲醇,甲醇汽油能减少有害气体(CO)排放。现有一种利用煤气化过程中生成的CO和H2来制备甲醇的方案,其反应原理为:CO(g)+2H2(g) CH3OH(g)。请根据下列图示回答问题:
CH3OH(g)。请根据下列图示回答问题:
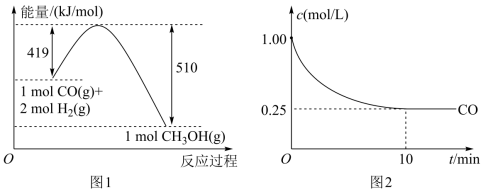
(1)根据(图1),写出此反应的热化学方程式___________ 。下列关于此反应的说法中,正确的是___________ (填字母)
A.任何条件都能自发进行 B.高温条件能够自发进行
C.任何条件都不自发进行 D.低温条件能够自发进行
(2)现进行如下实验,在体积为1L的密闭容器中,充入1
 和3
和3
 ,测得
,测得 的浓度随时间变化如(图2)所示,从反应开始到平衡,
的浓度随时间变化如(图2)所示,从反应开始到平衡, 的平均反应速率
的平均反应速率
___________ 
(3)恒容条件下,上述反应达到平衡后,以下措施中能使 增大的有___________。
增大的有___________。
(4)已知在常温常压下:化学反应①②的平衡常数分别为 ,
,
①2CH3OH(l)+O2(g) CO2(g)+4H2(g) K1
CO2(g)+4H2(g) K1
②2CO(g)+O2(g) CO2(g) K2
CO2(g) K2
则CO(g)+2H2(g) CH3OH(l)的
CH3OH(l)的
___________ (用含有K1,K2的代数式表达)
 CH3OH(g)。请根据下列图示回答问题:
CH3OH(g)。请根据下列图示回答问题:
(1)根据(图1),写出此反应的热化学方程式
A.任何条件都能自发进行 B.高温条件能够自发进行
C.任何条件都不自发进行 D.低温条件能够自发进行
(2)现进行如下实验,在体积为1L的密闭容器中,充入1

 和3
和3
 ,测得
,测得 的浓度随时间变化如(图2)所示,从反应开始到平衡,
的浓度随时间变化如(图2)所示,从反应开始到平衡, 的平均反应速率
的平均反应速率

(3)恒容条件下,上述反应达到平衡后,以下措施中能使
 增大的有___________。
增大的有___________。| A.升高温度 | B.充入 气 气 |
C.再充入1  和3 和3  | D.使用催化剂 |
 ,
,
①2CH3OH(l)+O2(g)
 CO2(g)+4H2(g) K1
CO2(g)+4H2(g) K1②2CO(g)+O2(g)
 CO2(g) K2
CO2(g) K2则CO(g)+2H2(g)
 CH3OH(l)的
CH3OH(l)的
您最近一年使用:0次






