亚硫酸盐与硫酸盐在工农业生产、生活中具有广泛应用。
(1) 溶液呈酸性,在
溶液呈酸性,在 溶液中,下列关系不正确的
溶液中,下列关系不正确的_______ (填字母)。
a.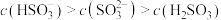
b.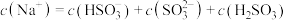
c.
d.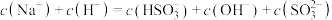
(2)已知: ,
,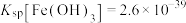 ,
, 时
时 开始沉淀,室温下,除去
开始沉淀,室温下,除去 溶液中的
溶液中的 ,
, (使其浓度均小于
(使其浓度均小于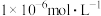 ),需调节溶液pH的范围为
),需调节溶液pH的范围为_______ 。
(3)如图是某温度下,将足量的 固体溶于一定量水中达到溶解平衡后,假定溶液体积不变的情况下,加入
固体溶于一定量水中达到溶解平衡后,假定溶液体积不变的情况下,加入 使
使 增大过程中,溶液中
增大过程中,溶液中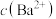 和
和 的变化曲线,根据图中的数据分析、计算。
的变化曲线,根据图中的数据分析、计算。
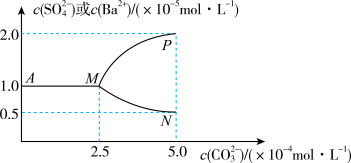
①该温度下, 的
的
_______ 。
②当 大于
大于_______  时开始有
时开始有 沉淀生成。
沉淀生成。
③图像中代表沉淀转化过程中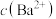 随
随 变化的曲线是
变化的曲线是_______ (填“MP”或“MN”);沉淀转化的离子方程式为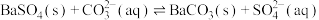 ,该反应的平衡常数
,该反应的平衡常数
_______ 。
(1)
 溶液呈酸性,在
溶液呈酸性,在 溶液中,下列关系不正确的
溶液中,下列关系不正确的a.
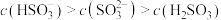
b.
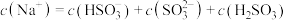
c.

d.
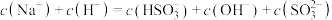
(2)已知:
 ,
,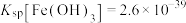 ,
, 时
时 开始沉淀,室温下,除去
开始沉淀,室温下,除去 溶液中的
溶液中的 ,
, (使其浓度均小于
(使其浓度均小于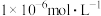 ),需调节溶液pH的范围为
),需调节溶液pH的范围为(3)如图是某温度下,将足量的
 固体溶于一定量水中达到溶解平衡后,假定溶液体积不变的情况下,加入
固体溶于一定量水中达到溶解平衡后,假定溶液体积不变的情况下,加入 使
使 增大过程中,溶液中
增大过程中,溶液中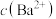 和
和 的变化曲线,根据图中的数据分析、计算。
的变化曲线,根据图中的数据分析、计算。
①该温度下,
 的
的
②当
 大于
大于 时开始有
时开始有 沉淀生成。
沉淀生成。③图像中代表沉淀转化过程中
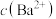 随
随 变化的曲线是
变化的曲线是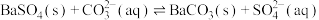 ,该反应的平衡常数
,该反应的平衡常数
更新时间:2022-12-06 11:31:30
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.现有下列物质:①稀硫酸 ② 固体 ③氨水 ④二氧化碳 ⑤
固体 ③氨水 ④二氧化碳 ⑤ 固体 ⑥稀
固体 ⑥稀 溶液 ⑦
溶液 ⑦ 溶液。回答下列问题:
溶液。回答下列问题:
(1)属于强电解质的物质是_______ (填序号)。
(2)用离子方程式表示 溶液显酸性的原因
溶液显酸性的原因_______ 。
(3)NaHSO3溶液溶液显酸性的原因是_______ 。
(4)浓度均为 的下列四种溶液中
的下列四种溶液中 由大到小的顺序为
由大到小的顺序为_______ (填序号)。
① ②
② ③
③ ④氨水
④氨水
(5)常温下,下列说法正确的是_______ (填字母序号)。
a.pH相等的氨水和NaOH溶液,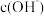 相等
相等
b.稀释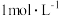 的硫酸溶液,溶液中的离子浓度均下降
的硫酸溶液,溶液中的离子浓度均下降
c.pH=2的 溶液和pH=2的
溶液和pH=2的 溶液,
溶液,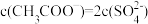
II.在水的电离平衡中,c(H+)和c(OH−)的关系如图所示:
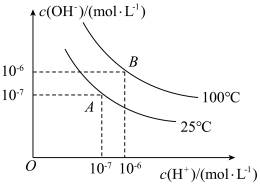
(6)A点水的离子积常数为1×10−14,B点水的离子积常数为_______ 。造成水的离子积常数变化的原因是_______ 。
(7)100 ℃时,若向水中滴加盐酸,_______ (填“能”或“不能”)使体系处于B点状态,原因是_______ 。
 固体 ③氨水 ④二氧化碳 ⑤
固体 ③氨水 ④二氧化碳 ⑤ 固体 ⑥稀
固体 ⑥稀 溶液 ⑦
溶液 ⑦ 溶液。回答下列问题:
溶液。回答下列问题:(1)属于强电解质的物质是
(2)用离子方程式表示
 溶液显酸性的原因
溶液显酸性的原因(3)NaHSO3溶液溶液显酸性的原因是
(4)浓度均为
 的下列四种溶液中
的下列四种溶液中 由大到小的顺序为
由大到小的顺序为①
 ②
② ③
③ ④氨水
④氨水(5)常温下,下列说法正确的是
a.pH相等的氨水和NaOH溶液,
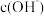 相等
相等b.稀释
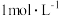 的硫酸溶液,溶液中的离子浓度均下降
的硫酸溶液,溶液中的离子浓度均下降c.pH=2的
 溶液和pH=2的
溶液和pH=2的 溶液,
溶液,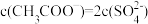
II.在水的电离平衡中,c(H+)和c(OH−)的关系如图所示:

(6)A点水的离子积常数为1×10−14,B点水的离子积常数为
(7)100 ℃时,若向水中滴加盐酸,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按照要求回答下列问题
(1)硫酸铁溶液显酸性的原因_____ (用离子方程式表示).
(2)物质的量浓度相同的醋酸和氢氧化钠溶液混合溶液中c(CH3COO﹣)=c(Na+),则混合后溶液显_____ 性.
(3)浓度均为0.1mol/L①氯化铵②醋酸铵③硫酸氢铵④氨水四种溶液中,c(NH4+)由大到小的顺序_____ (填序号).
(4)将化合物A的蒸气1mol充入0.5L容器中加热分解:2A(g)⇌B(g)+nC(g),反应到3min时,容器内A的浓度为0.8mol/L,测得这段时间内,平均速率ν(C)=0.6mol/(L•min),则化学方程式中的n值为_____ ,ν(B)=_____ ,此时A的分解率为_____ .
(1)硫酸铁溶液显酸性的原因
(2)物质的量浓度相同的醋酸和氢氧化钠溶液混合溶液中c(CH3COO﹣)=c(Na+),则混合后溶液显
(3)浓度均为0.1mol/L①氯化铵②醋酸铵③硫酸氢铵④氨水四种溶液中,c(NH4+)由大到小的顺序
(4)将化合物A的蒸气1mol充入0.5L容器中加热分解:2A(g)⇌B(g)+nC(g),反应到3min时,容器内A的浓度为0.8mol/L,测得这段时间内,平均速率ν(C)=0.6mol/(L•min),则化学方程式中的n值为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】乙二酸 俗称草酸,为无色晶体,是二元弱酸,广泛分布于植物、动物和真菌体中,在实验研究和化学工业中应用广泛。回答下列问题:
俗称草酸,为无色晶体,是二元弱酸,广泛分布于植物、动物和真菌体中,在实验研究和化学工业中应用广泛。回答下列问题:
(1)工业上可由以下反应制取草酸:
Ⅰ.4CO(g)+4C4H9OH(l)+O2(g) 2(COOC4H9)2(l)+2H2O(l)
2(COOC4H9)2(l)+2H2O(l)
Ⅱ. (COOC4H9)2(l)+2H2O(l) H2C2O4(l)+2 C4H9OH(l)
H2C2O4(l)+2 C4H9OH(l)
①下列有关反应Ⅰ的说法正确是___________ 。
a.适当升高温度可以加快该反应速率
b.改变压强对该反应的速率没有影响
c.可以选用合适的催化剂加快该反应速率
②反应Ⅱ的浓度化学平衡常数的表达式为___________ 。
(2)已知: 的
的
①写出草酸第一步电离的方程式:___________ 。
②下列有关说法正确的是___________ (填字母序号)。
a. 溶液中:
溶液中: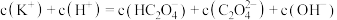
b. 溶液中:
溶液中:
c.浓度均为 和
和 的混合溶液中:
的混合溶液中:
d. 溶液中滴加等浓度
溶液中滴加等浓度 溶液至中性:
溶液至中性:
(3)实验室常以硫酸亚铁和草酸为原料制备草酸亚铁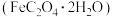 。通过测定产品中
。通过测定产品中 和
和 的含量来判断晶体的纯度,其测定过程示意图如图,
的含量来判断晶体的纯度,其测定过程示意图如图, 可与
可与 形成无色的
形成无色的 ,使滴定的终点更容易判断。
,使滴定的终点更容易判断。

① “滴定Ⅰ”过程中做还原剂的离子为___________ 。
② “滴定Ⅱ”过程离子方程式为___________ 。
③样品中
___________ 。
 俗称草酸,为无色晶体,是二元弱酸,广泛分布于植物、动物和真菌体中,在实验研究和化学工业中应用广泛。回答下列问题:
俗称草酸,为无色晶体,是二元弱酸,广泛分布于植物、动物和真菌体中,在实验研究和化学工业中应用广泛。回答下列问题:(1)工业上可由以下反应制取草酸:
Ⅰ.4CO(g)+4C4H9OH(l)+O2(g)
 2(COOC4H9)2(l)+2H2O(l)
2(COOC4H9)2(l)+2H2O(l)Ⅱ. (COOC4H9)2(l)+2H2O(l)
 H2C2O4(l)+2 C4H9OH(l)
H2C2O4(l)+2 C4H9OH(l)①下列有关反应Ⅰ的说法正确是
a.适当升高温度可以加快该反应速率
b.改变压强对该反应的速率没有影响
c.可以选用合适的催化剂加快该反应速率
②反应Ⅱ的浓度化学平衡常数的表达式为
(2)已知:
 的
的
①写出草酸第一步电离的方程式:
②下列有关说法正确的是
a.
 溶液中:
溶液中: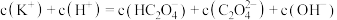
b.
 溶液中:
溶液中:
c.浓度均为
 和
和 的混合溶液中:
的混合溶液中:
d.
 溶液中滴加等浓度
溶液中滴加等浓度 溶液至中性:
溶液至中性:
(3)实验室常以硫酸亚铁和草酸为原料制备草酸亚铁
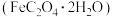 。通过测定产品中
。通过测定产品中 和
和 的含量来判断晶体的纯度,其测定过程示意图如图,
的含量来判断晶体的纯度,其测定过程示意图如图, 可与
可与 形成无色的
形成无色的 ,使滴定的终点更容易判断。
,使滴定的终点更容易判断。
① “滴定Ⅰ”过程中做还原剂的离子为
② “滴定Ⅱ”过程离子方程式为
③样品中

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,CaS的 ,饱和溶液中存在平衡:
,饱和溶液中存在平衡: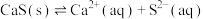 。试根据沉淀溶解平衡知识回答问题:
。试根据沉淀溶解平衡知识回答问题:
(1)该温度下,将 氯化钙溶液
氯化钙溶液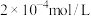 硫化钠溶液等体积混合,
硫化钠溶液等体积混合,___________ (填“能”或“不能”)产生沉淀。滴加少量盐酸,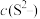
___________ (填“增大”或“减小”),请从平衡移动原理的角度解释:___________ 。
(2)若向CaS悬浊液中加入CuSO4溶液,生成一种黑色固体物质,写出该过程中反应的离子方程式___________ 。
(3)已知 ,在
,在 的溶液中,当
的溶液中,当 刚开始沉淀时,溶液的pH为
刚开始沉淀时,溶液的pH为___________ (保留1为小数,下同);若要使其沉淀完全,pH的范围是___________ 。
 ,饱和溶液中存在平衡:
,饱和溶液中存在平衡: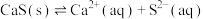 。试根据沉淀溶解平衡知识回答问题:
。试根据沉淀溶解平衡知识回答问题:(1)该温度下,将
 氯化钙溶液
氯化钙溶液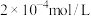 硫化钠溶液等体积混合,
硫化钠溶液等体积混合,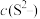
(2)若向CaS悬浊液中加入CuSO4溶液,生成一种黑色固体物质,写出该过程中反应的离子方程式
(3)已知
 ,在
,在 的溶液中,当
的溶液中,当 刚开始沉淀时,溶液的pH为
刚开始沉淀时,溶液的pH为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】研究碳、氮、硫及其化合物的转化对改善环境有重大意义。回答下列问题:
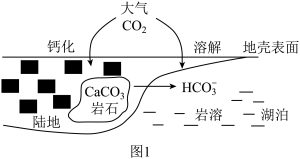
(1)某处碳循环如图1所示,CaCO3转化为HCO 的离子方程式为
的离子方程式为____ 。结合平衡移动原理分析CaCO3溶解的原因_____ 。
(2)利用“亚硫酸盐法”吸收工业废气中的SO2。常温下,将工业废气通入(NH4)2SO3溶液中,测得溶液pH与含硫组分物质的量分数[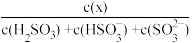 ]的变化关系如图2所示。
]的变化关系如图2所示。
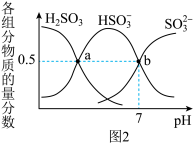
①Ka2(H2SO3)=_____ 。b点溶液中n(NH ):n(SO
):n(SO )=
)=____ 。
②常温下,Ka1(H2SO3)=1.5×10-2;Kb(NH3•H2O)=1.8×10-5。0.1mol•L-1的(NH4)2SO3溶液中离子浓度由大到小的顺序为____ (不考虑OH-)。
(3)尿素溶于水缓慢水解产生碳酸铵,碳酸铵溶液显碱性,原因是____ 。向浓度均为0.1mol•L-1的CdCl2和ZnCl2混合液中滴加碳酸铵溶液,当加入碳酸铵溶液至生成两种沉淀,则溶液中c(Zn2+):c(Cd2+)=____ 。[已知Ksp(CdCO3)=1.0×10-12,Ksp(ZnCO3)=1.5×10-10]
(4)工业废水中含有甲醛,某厂降解甲醛的反应机理如图3所示,则X表示的粒子是_____ 。

(1)某处碳循环如图1所示,CaCO3转化为HCO
 的离子方程式为
的离子方程式为
(2)利用“亚硫酸盐法”吸收工业废气中的SO2。常温下,将工业废气通入(NH4)2SO3溶液中,测得溶液pH与含硫组分物质的量分数[
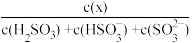 ]的变化关系如图2所示。
]的变化关系如图2所示。
①Ka2(H2SO3)=
 ):n(SO
):n(SO )=
)=②常温下,Ka1(H2SO3)=1.5×10-2;Kb(NH3•H2O)=1.8×10-5。0.1mol•L-1的(NH4)2SO3溶液中离子浓度由大到小的顺序为
(3)尿素溶于水缓慢水解产生碳酸铵,碳酸铵溶液显碱性,原因是
(4)工业废水中含有甲醛,某厂降解甲醛的反应机理如图3所示,则X表示的粒子是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知在25℃的水溶液中,AgCl、AgBr、AgI均难溶于水,且Ksp(AgCl)= 1.8×10-10,Ksp(AgBr)= 1.0×10-12,Ksp(AgI)= 8.7×10-17;
(1) 若向AgBr的饱和溶液中加入少量的AgCl固体,则c(Br-)_______________ 。 (填“增大”、“减小”或“不变”)。
(2)在25℃时,若取0.188 g的AgBr(相对分子质量188)固体放入100 mL水中(忽略溶液体积的变化),则溶液中Br-的物质的量浓度为_____________ 。
(3)① 由上述Ksp判断,在上述(2)的体系中,能否实现AgBr向AgI的转化_______ (填“能”或“否”),简述理由:_____________________________________________________________ 。
② 若某KCl溶液的浓度为 1.0×10-2 mol·L-1 ,将等体积的该KCl溶液与AgNO3 溶液混合,则生成沉淀所需AgNO3 溶液的最小浓度为__________ mol·L-1。
(1) 若向AgBr的饱和溶液中加入少量的AgCl固体,则c(Br-)
(2)在25℃时,若取0.188 g的AgBr(相对分子质量188)固体放入100 mL水中(忽略溶液体积的变化),则溶液中Br-的物质的量浓度为
(3)① 由上述Ksp判断,在上述(2)的体系中,能否实现AgBr向AgI的转化
② 若某KCl溶液的浓度为 1.0×10-2 mol·L-1 ,将等体积的该KCl溶液与AgNO3 溶液混合,则生成沉淀所需AgNO3 溶液的最小浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)25℃时,M(OH)2的Ksp=4.0×10-12 ,求饱和溶液中的c(H+)___________ 。
(2)把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是_______________________ 。
(3)830 K时,已知可逆反应CO(g)+H2O(g) CO2(g)+H2(g)。若起始时c(CO)=2 mol/L,c(H2O)= 3 mol/L,平衡时CO的转化率为60%,则平衡时K值为
CO2(g)+H2(g)。若起始时c(CO)=2 mol/L,c(H2O)= 3 mol/L,平衡时CO的转化率为60%,则平衡时K值为_____________ 。
(2)把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是
(3)830 K时,已知可逆反应CO(g)+H2O(g)
 CO2(g)+H2(g)。若起始时c(CO)=2 mol/L,c(H2O)= 3 mol/L,平衡时CO的转化率为60%,则平衡时K值为
CO2(g)+H2(g)。若起始时c(CO)=2 mol/L,c(H2O)= 3 mol/L,平衡时CO的转化率为60%,则平衡时K值为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知常温时Ksp[Fe(OH)3]=8.0×10-38,若Fe3+离子在溶液中的浓度小于1×10-5mol·L-1时就可以认为Fe3+离子已经沉淀完全。若此溶液中c(Fe3+)=0.01mol·L-1:(已知Ksp[Mg(OH)2]=4×10-12,lg5=0.7)
(1)Fe3+开始沉淀时溶液中c(OH-)约为_______ mol·L-1。
(2)当Fe3+沉淀完全时溶液中pH约为_______ 。
(3)若此溶液中还含有Mg2+,其浓度为1mol·L-1,则Fe3+完全沉淀时Mg2+_______ 。
A.尚未开始沉淀 B.已经开始沉淀 C.已经沉淀完全
(4)在含有少量Fe3+的Mg2+溶液中_______ (填“可以”或“不可以”)用调节pH的方法来除去Fe3+。
(1)Fe3+开始沉淀时溶液中c(OH-)约为
(2)当Fe3+沉淀完全时溶液中pH约为
(3)若此溶液中还含有Mg2+,其浓度为1mol·L-1,则Fe3+完全沉淀时Mg2+
A.尚未开始沉淀 B.已经开始沉淀 C.已经沉淀完全
(4)在含有少量Fe3+的Mg2+溶液中
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按题目要求填空
(1)CH3COONa和CH3COOH的混合溶液中c(Na+)=c(CH3COO-),则该溶液呈___________ 性。(填“酸”“碱”或“中”)
(2)常温下,0.1mol·L-1NH4Cl溶液呈___________ 性,原因是___________ (用离子方程式表示)
(3)常温时,部分物质的电离平衡常数如表所示:
请回答下列问题:
①CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为___________
②向NaClO溶液中通入少量CO2,离子方程式为___________
(4)AlCl3溶液蒸干并灼烧的产物是___________
(5)已知,常温下Ksp[Cu(OH)2]=2.0×10-20,Cu2++4NH3 [Cu(NH3)4]2+,K=1.0×1013。
[Cu(NH3)4]2+,K=1.0×1013。
向硫酸铜溶液中逐渐加入浓氨水,先产生蓝色沉淀,后沉淀溶解得到[Cu(NH3)4]2+,且沉淀开始溶解时pH=10。则产生蓝色沉淀的离子反应方程式为___________ ,沉淀溶解时, =
=___________ 。
(1)CH3COONa和CH3COOH的混合溶液中c(Na+)=c(CH3COO-),则该溶液呈
(2)常温下,0.1mol·L-1NH4Cl溶液呈
(3)常温时,部分物质的电离平衡常数如表所示:
| 化学式 |  |  |  |
| 电离平衡常数 |  | 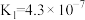 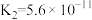 |  |
①CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为
②向NaClO溶液中通入少量CO2,离子方程式为
(4)AlCl3溶液蒸干并灼烧的产物是
(5)已知,常温下Ksp[Cu(OH)2]=2.0×10-20,Cu2++4NH3
 [Cu(NH3)4]2+,K=1.0×1013。
[Cu(NH3)4]2+,K=1.0×1013。向硫酸铜溶液中逐渐加入浓氨水,先产生蓝色沉淀,后沉淀溶解得到[Cu(NH3)4]2+,且沉淀开始溶解时pH=10。则产生蓝色沉淀的离子反应方程式为
 =
=
您最近一年使用:0次



