钛和锆为同族的元素,它们形成的化合物用途广泛。
(1)锆为第五周期元素,基态原子的价层电子排布式为_______ 。
(2)钛与EDTA(乙二胺四乙酸根离子,结构如图1)形成的配位离子如图2所示。
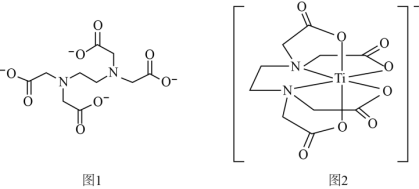
①EDTA中所含元素的电负性从大到小的顺序为_______ ;
②EDTA中键角∠NCC_______ (填“>”、“<”或“=”)∠CNC;
③钛与EDTA形成的配位离子中配位数为_______ 。
(3)常温下TiCl4为液体,ZrCl4为易升华的固体。两者熔点不同的原因是_______ 。
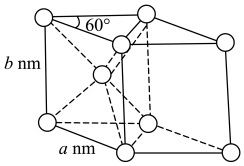
(4)ZrO2是制作全瓷牙的主要原料。ZrO2的晶体有立方晶相(如图3)、单斜晶相(如图4,微粒未画出,微粒分布与立方晶相相似,晶胞参数α=γ=900≠β,apm、bpm、cpm)等。
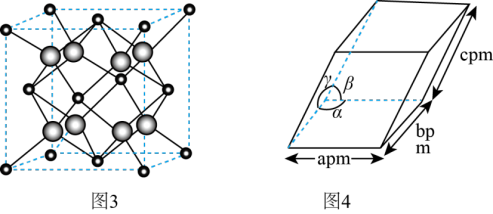
①ZrO2立方晶相中,与Zr等距离且最近的O围成的几何图形是_______ 。
②设阿伏加德罗常数的值为NA,则单斜晶相ZrO2的密度为_______ g·cm-3(列出含字母的计算表达式)。
(1)锆为第五周期元素,基态原子的价层电子排布式为
(2)钛与EDTA(乙二胺四乙酸根离子,结构如图1)形成的配位离子如图2所示。

①EDTA中所含元素的电负性从大到小的顺序为
②EDTA中键角∠NCC
③钛与EDTA形成的配位离子中配位数为
(3)常温下TiCl4为液体,ZrCl4为易升华的固体。两者熔点不同的原因是
(4)ZrO2是制作全瓷牙的主要原料。ZrO2的晶体有立方晶相(如图3)、单斜晶相(如图4,微粒未画出,微粒分布与立方晶相相似,晶胞参数α=γ=900≠β,apm、bpm、cpm)等。

①ZrO2立方晶相中,与Zr等距离且最近的O围成的几何图形是
②设阿伏加德罗常数的值为NA,则单斜晶相ZrO2的密度为
更新时间:2022-11-09 17:48:06
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】当下新能源汽车电池的发展加大了对金属钻(Co)的需求。回答下列问题:
(1)基态Co原子价电子排布式为__________ ,Co2+有___ 个未成对电子。
(2)Co的第四电离能比Fe的第四电离能要小很多,原因是________________ 。
(3)Na3[Co(NO2)6]中的 中N原子为
中N原子为_______ 杂化,空间构型名称为_________ 形。
(4)一种Co(Ⅱ)的配合物结构如图所示,下列说法错误的是______(填序号)。
(5)金属钴晶胞结构及参数如图所示,该晶胞中Co的配位数为________ 。已知金属Co晶体密度为ρ g/cm3,则阿伏加德罗常数NA=___________ mol-1。
(1)基态Co原子价电子排布式为
(2)Co的第四电离能比Fe的第四电离能要小很多,原因是
(3)Na3[Co(NO2)6]中的
 中N原子为
中N原子为(4)一种Co(Ⅱ)的配合物结构如图所示,下列说法错误的是______(填序号)。
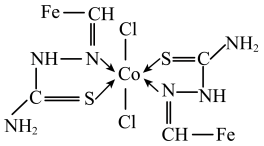
| A.配合物中的氯元素是Cl- |
| B.配合物中Co2+配位数为4 |
| C.结构中所有N原子有sp2、sp3杂化 |
D.结构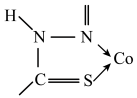 中所有原子共平面 中所有原子共平面 |
(5)金属钴晶胞结构及参数如图所示,该晶胞中Co的配位数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】高纯硫酸锰在电池材料领域具有重要的用途。一种以软锰矿(主要成分是 ,含有
,含有 、
、 、
、 、
、 等杂质)和硫铁矿(主要成分是
等杂质)和硫铁矿(主要成分是 ,含有FeO、NiO、
,含有FeO、NiO、 等杂质)为原料制备
等杂质)为原料制备 流程如下图所示。
流程如下图所示。

相关金属离子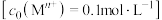 形成氢氧化物沉淀的pH范围如下:
形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)基态Mn原子的价电子排布式为_______ 。
(2)“滤渣1”的成分是 。“酸浸”过程中,
。“酸浸”过程中, 转化为
转化为 的化学反应方程式为
的化学反应方程式为_______ 。
(3)“氧化”目的是将浸出液中 氧化为
氧化为 ,为检测溶液中
,为检测溶液中 是否被氧化完全,可选用的化学试剂为
是否被氧化完全,可选用的化学试剂为_______ 。
(4)已知加入 调节溶液pH为5~6,则“滤渣2”的主要成分是
调节溶液pH为5~6,则“滤渣2”的主要成分是_______ 。
(5)已知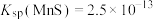 ,
, ,请用沉淀溶解平衡原理计算说明“除杂1”中选择MnS的原因
,请用沉淀溶解平衡原理计算说明“除杂1”中选择MnS的原因_______ 。
(6)“除杂2”中加入 的作用是
的作用是_______ 。
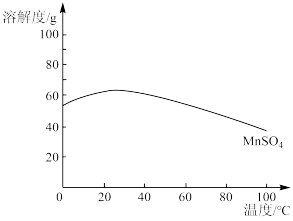
(7)下图为 溶解度曲线。则“结晶”的具体操作为
溶解度曲线。则“结晶”的具体操作为_______ 、_______ 、洗涤、干燥。
 ,含有
,含有 、
、 、
、 、
、 等杂质)和硫铁矿(主要成分是
等杂质)和硫铁矿(主要成分是 ,含有FeO、NiO、
,含有FeO、NiO、 等杂质)为原料制备
等杂质)为原料制备 流程如下图所示。
流程如下图所示。
相关金属离子
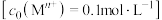 形成氢氧化物沉淀的pH范围如下:
形成氢氧化物沉淀的pH范围如下:| 金属离子 |  |  |  |  |  |  |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.9 |
回答下列问题:
(1)基态Mn原子的价电子排布式为
(2)“滤渣1”的成分是
 。“酸浸”过程中,
。“酸浸”过程中, 转化为
转化为 的化学反应方程式为
的化学反应方程式为(3)“氧化”目的是将浸出液中
 氧化为
氧化为 ,为检测溶液中
,为检测溶液中 是否被氧化完全,可选用的化学试剂为
是否被氧化完全,可选用的化学试剂为(4)已知加入
 调节溶液pH为5~6,则“滤渣2”的主要成分是
调节溶液pH为5~6,则“滤渣2”的主要成分是(5)已知
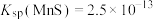 ,
, ,请用沉淀溶解平衡原理计算说明“除杂1”中选择MnS的原因
,请用沉淀溶解平衡原理计算说明“除杂1”中选择MnS的原因(6)“除杂2”中加入
 的作用是
的作用是(7)下图为
 溶解度曲线。则“结晶”的具体操作为
溶解度曲线。则“结晶”的具体操作为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
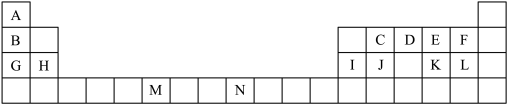
试回答下列问题:
(1)表中元素,电负性最强的是_______ (填元素符号),J的元素名称为_______ 。N基态原子核外能级上有_______ 未成对电子。
(2)D元素原子的价电子排布图为_______ ,核外有_______ 种不同运动状态的电子。该元素形成的常见单质分子中σ键和π键个数比为_______
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是_______ (填“极性”或“非极性”)分子。
(4)C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是_______ (填字母)。
a. b.CH4 c.CH2=CHCH3 d.CH3CH2C≡CH
b.CH4 c.CH2=CHCH3 d.CH3CH2C≡CH

试回答下列问题:
(1)表中元素,电负性最强的是
(2)D元素原子的价电子排布图为
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是
(4)C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是
a.
 b.CH4 c.CH2=CHCH3 d.CH3CH2C≡CH
b.CH4 c.CH2=CHCH3 d.CH3CH2C≡CH
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】已知A,B,C,D,E,F均为周期表中前36号元素,且原子序数依次增大.A,B,C为同一周期的主族元素,B原子p能级电子总数与s能级电子总数相等.A,F原子未成对电子是同周期中最多的,且F基态原子中电子占据三种不同形状的原子轨道.D和E原子的第一至第四电离能如下表所示:
(1)A,B,C三种元素的电负性最大的是__ (填写元素符号),D,E两元素中D的第一电离能较大的原因是__ .
(2)F基态原子的核外电子排布式是__ ;在一定条件下,F原子的核外电子从基态跃迁到激发态产生的光谱属于__ 光谱(填“吸收”或“发射”).
(3)根据等电子原理,写出AB+的电子式:__ .
(4)已知:F3+可形成配位数为6的配合物.组成为FCl3•6H2O的配合物有3种,分别呈紫色、蓝绿色、绿色,为确定这3种配合物的成键情况,分别取等质量的紫色、蓝绿色、绿色3种物质的样品配成溶液,分别向其中滴入过量的AgNO3溶液,均产生白色沉淀且质量比为3:2:1.则绿色配合物的化学式为__ .
A [CrCl(H2O)5]Cl2•H2O B [CrCl2(H2O)4]Cl•2H2O
C [Cr(H2O)6]Cl3 D [CrCl3(H2O)3]•3H2O
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| D | 738 | 1451 | 7733 | 10540 |
| E | 578 | 1817 | 2745 | 11578 |
(2)F基态原子的核外电子排布式是
(3)根据等电子原理,写出AB+的电子式:
(4)已知:F3+可形成配位数为6的配合物.组成为FCl3•6H2O的配合物有3种,分别呈紫色、蓝绿色、绿色,为确定这3种配合物的成键情况,分别取等质量的紫色、蓝绿色、绿色3种物质的样品配成溶液,分别向其中滴入过量的AgNO3溶液,均产生白色沉淀且质量比为3:2:1.则绿色配合物的化学式为
A [CrCl(H2O)5]Cl2•H2O B [CrCl2(H2O)4]Cl•2H2O
C [Cr(H2O)6]Cl3 D [CrCl3(H2O)3]•3H2O
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】依据原子结构知识回答下列问题。
(1)基态Cr原子的电子排布式是____________ ;基态 的价电子排布图为
的价电子排布图为____________ 。
(2)Cu、K、O、F四种元素中第一电离能最小的是______ ,电负性最大的是____________ 。
(3)下列有关微粒性质的排列顺序错误的是______。
(4)下列硼原子电子排布图表示的状态中,能量最高的为______(填选项字母)。
(5)O的基态原子核外电子空间运动状态有______ 种,其原子半径______  (填“大于”或“小于”)。
(填“大于”或“小于”)。
(1)基态Cr原子的电子排布式是
 的价电子排布图为
的价电子排布图为(2)Cu、K、O、F四种元素中第一电离能最小的是
(3)下列有关微粒性质的排列顺序错误的是______。
| A.元素的电负性:P<O<F | B.元素的第一电离能:C<N<O |
C.离子半径: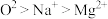 | D.原子的未成对电子数:Mn>Si>Cl |
A. | B.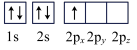 |
C. | D.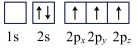 |
 (填“大于”或“小于”)。
(填“大于”或“小于”)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】铁、钴、铜是重要的过渡元素,其化合物具有广泛的用途。
(1)钴位于元素周期表中第____ 族,基态Cu的核外电子排布式是_________ 。元素铁与铜的第二电离能分别为:ICu=1958kJ/mol、IFe=1561kJ/mol,ICu>IFe的原因是______________ 。
(2)有机铁肥三硝酸六尿素合铁(Ⅲ),化学式为:[Fe(H2NCONH2)6](NO3)3.
①尿素分子中C原子的杂化方式是_______ ,所含非金属元素的电负性由大到小的顺序是_____ 。
②[Fe(H2NCONH2)6](NO3)3中“H2NCONH2”与Fe(Ⅲ)之间的作用力是_______ 。根据价层电子对互斥理论推测NO3-的空间构型为_________ 。
(3)Fe3+可用SCN-检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是________________ ,原因是________________ 。
(4)FeCl3晶体易溶于水喝乙醇,用酒精灯加热即可气化,由此可知FeCl3的晶体类型为_____ ;S和Fe形成的某化合物,其晶胞如图一所示,则该物质的化学式为_______ 。
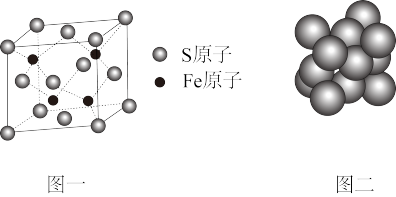
(5)Cu晶体的堆积方式如图二所示,晶体中Cu原子的配位数为_______ ;设Cu原子半径为a,晶体空间利用率为_______ (用含a的式子表达,不化简)。
(1)钴位于元素周期表中第
(2)有机铁肥三硝酸六尿素合铁(Ⅲ),化学式为:[Fe(H2NCONH2)6](NO3)3.
①尿素分子中C原子的杂化方式是
②[Fe(H2NCONH2)6](NO3)3中“H2NCONH2”与Fe(Ⅲ)之间的作用力是
(3)Fe3+可用SCN-检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是
(4)FeCl3晶体易溶于水喝乙醇,用酒精灯加热即可气化,由此可知FeCl3的晶体类型为

(5)Cu晶体的堆积方式如图二所示,晶体中Cu原子的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铁、钴、镍并称铁系元素,性质具有相似性。
(1)基态钴原子的核外电子排布式为___________ ,Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是___________ 。
(2)铁氰化钾K3[Fe(CN)6]溶液可以检验Fe2+。1 mol CN-中含有π键的数目为___________ ,与CN-互为等电子体(化学通式相同且价电子总数相等)的分子有___________ ,铁氰化钾晶体中各种微粒间的相互作用不包括___________ 。
a.离子键 b.共价键 c.配位键 d.金属键 e.氢键 f.范德华力
(3)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化。甲醛分子的空间结构为___________ ,碳原子的杂化类型为___________ 。
(4)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO___________ FeO(填“<”或“>”),判断依据是___________ 。
(5)Si与P形成的某化合物晶体的晶胞如图。该晶体类型是___________ ,该化合物的化学式为___________ 。

(1)基态钴原子的核外电子排布式为
(2)铁氰化钾K3[Fe(CN)6]溶液可以检验Fe2+。1 mol CN-中含有π键的数目为
a.离子键 b.共价键 c.配位键 d.金属键 e.氢键 f.范德华力
(3)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化。甲醛分子的空间结构为
(4)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO
(5)Si与P形成的某化合物晶体的晶胞如图。该晶体类型是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】齐家坪遗址是一处新石器时代晚期文化遗址,出土的铜镜是迄今为止我国发现最早的铜镜。铜及其化合物在工农业生产中有广泛的应用。
I.金属铜的晶胞结构模型如图1所示。 原子周围距离最近的
原子周围距离最近的 原子数目为
原子数目为___________ 。
(2)设晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞密度为
,则该晶胞密度为___________ 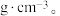
II. 能与
能与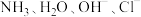 等形成配位数为4的配合物。
等形成配位数为4的配合物。
将 投入
投入 的混合溶液中进行“氨浸”,控制温度为
的混合溶液中进行“氨浸”,控制温度为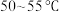 ,
, 约为9.5,
约为9.5, 转化为
转化为 溶液。
溶液。
(3) 中基态铜离子核外电子排布式为
中基态铜离子核外电子排布式为___________ 。
(4) 结构中,若用两个
结构中,若用两个 代替两个
代替两个 ,可以得到两种不同结构的化合物,由此推测
,可以得到两种不同结构的化合物,由此推测 的空间结构为
的空间结构为___________ 。
(5) 可以与乙二胺
可以与乙二胺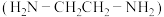 形成配离子,如图2所示:
形成配离子,如图2所示: 原子成键时采取的杂化方式是
原子成键时采取的杂化方式是___________ 杂化。
②乙二胺和三甲胺 均属于胺,但乙二胺比三甲胺的溶解度大很多,原因是
均属于胺,但乙二胺比三甲胺的溶解度大很多,原因是___________ 。
III.将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。
(6)下列物质中,属于顺磁性物质的是___________ (填字母)。
A.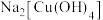 B.
B. C.
C.
I.金属铜的晶胞结构模型如图1所示。
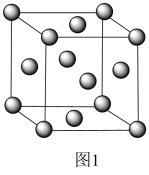
 原子周围距离最近的
原子周围距离最近的 原子数目为
原子数目为(2)设晶胞参数为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞密度为
,则该晶胞密度为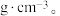
II.
 能与
能与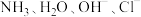 等形成配位数为4的配合物。
等形成配位数为4的配合物。将
 投入
投入 的混合溶液中进行“氨浸”,控制温度为
的混合溶液中进行“氨浸”,控制温度为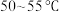 ,
, 约为9.5,
约为9.5, 转化为
转化为 溶液。
溶液。(3)
 中基态铜离子核外电子排布式为
中基态铜离子核外电子排布式为(4)
 结构中,若用两个
结构中,若用两个 代替两个
代替两个 ,可以得到两种不同结构的化合物,由此推测
,可以得到两种不同结构的化合物,由此推测 的空间结构为
的空间结构为(5)
 可以与乙二胺
可以与乙二胺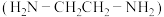 形成配离子,如图2所示:
形成配离子,如图2所示: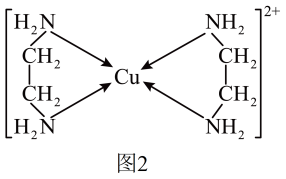
 原子成键时采取的杂化方式是
原子成键时采取的杂化方式是②乙二胺和三甲胺
 均属于胺,但乙二胺比三甲胺的溶解度大很多,原因是
均属于胺,但乙二胺比三甲胺的溶解度大很多,原因是III.将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。
(6)下列物质中,属于顺磁性物质的是
A.
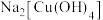 B.
B. C.
C.
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】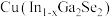 (简称
(简称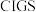 )可作多晶膜太阳能电池材料,具有非常好的发展前景。
)可作多晶膜太阳能电池材料,具有非常好的发展前景。
回答下列问题:
(1)已知铟的原子序数为49,基态铟原子的电子排布式为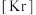
___________ ; 、
、 、
、 ,第一电离能从大到小顺序为
,第一电离能从大到小顺序为___________ 。
(2)硅与碳位于同主族,碳的化合物中往往有碳碳双键、碳碳三键,但是硅的化合物中只存在硅硅单键,其主要原因是___________ 。常温常压下, 呈气态,而
呈气态,而 呈液态,其主要原因是
呈液态,其主要原因是___________ 。
(3)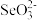 的立体构型为
的立体构型为___________ ; 中硒原子采取杂化类型是
中硒原子采取杂化类型是___________ 。
(4)常见的铜的硫化物有 和
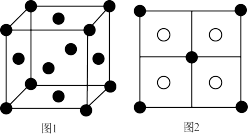
和 两种。已知:晶胞中
两种。已知:晶胞中 的位置如图1所示,铜离子位于硫离子所构成的四面体中心,它们晶胞具有相同的侧视图如图2所示。已知
的位置如图1所示,铜离子位于硫离子所构成的四面体中心,它们晶胞具有相同的侧视图如图2所示。已知 和
和 的晶胞参数分别为
的晶胞参数分别为 和
和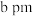 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。
① 晶体中,相邻的两个铜离子间的距离为
晶体中,相邻的两个铜离子间的距离为___________  。
。
② 晶体中,
晶体中, 的配位数为
的配位数为___________ 。
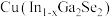 (简称
(简称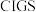 )可作多晶膜太阳能电池材料,具有非常好的发展前景。
)可作多晶膜太阳能电池材料,具有非常好的发展前景。回答下列问题:
(1)已知铟的原子序数为49,基态铟原子的电子排布式为
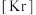
 、
、 、
、 ,第一电离能从大到小顺序为
,第一电离能从大到小顺序为(2)硅与碳位于同主族,碳的化合物中往往有碳碳双键、碳碳三键,但是硅的化合物中只存在硅硅单键,其主要原因是
 呈气态,而
呈气态,而 呈液态,其主要原因是
呈液态,其主要原因是(3)
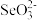 的立体构型为
的立体构型为 中硒原子采取杂化类型是
中硒原子采取杂化类型是(4)常见的铜的硫化物有
 和
和 两种。已知:晶胞中
两种。已知:晶胞中 的位置如图1所示,铜离子位于硫离子所构成的四面体中心,它们晶胞具有相同的侧视图如图2所示。已知
的位置如图1所示,铜离子位于硫离子所构成的四面体中心,它们晶胞具有相同的侧视图如图2所示。已知 和
和 的晶胞参数分别为
的晶胞参数分别为 和
和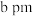 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为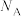 。
。①
 晶体中,相邻的两个铜离子间的距离为
晶体中,相邻的两个铜离子间的距离为 。
。②
 晶体中,
晶体中, 的配位数为
的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】电石(CaC2)是一种用于生产乙炔的浅色固体。它是由氧化钙与焦炭反应形成的:CaO+3C CaC2+CO。德国化学家维勒发现,电石与水反应释放出乙炔气体(C2H2)和氢氧化钙,也含有H2S、PH3等杂质气体。
CaC2+CO。德国化学家维勒发现,电石与水反应释放出乙炔气体(C2H2)和氢氧化钙,也含有H2S、PH3等杂质气体。
回答下列问题:
(1)上述六种元素中,电负性最大的是___________ (填写元素名称),原子半径最大者在基态时核外电子占据的轨道数目为___________ 个。
(2)H2S、PH3分子中心原子的价层电子对数目___________ (填“相同”或“不同”)。根据等电子原理,画出C 离子的电子式
离子的电子式___________ ,乙炔分子中C原子的杂化方式为___________ 。
(3)已知键能数据如下表:
请解释CO比N2容易发生反应:___________ 。
(4)如图为电石的四方晶胞(长方体),钙离子位于___________ ,它填入C 离子围成的八面体空隙。计算一个晶胞内含有化学式的数量为
离子围成的八面体空隙。计算一个晶胞内含有化学式的数量为___________ 。
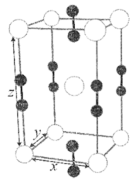
(5)已知电石密度为2.13 g·cm-3,阿伏加德罗常数为6.02×1023 mol-1,x、y值均为a (1
(1 =10-10m),则z=
=10-10m),则z=___________ nm(用含a的式子表示,且数字保留整数)。已知a<4.0,则距离钙最近的C 中心有
中心有___________ 个。
 CaC2+CO。德国化学家维勒发现,电石与水反应释放出乙炔气体(C2H2)和氢氧化钙,也含有H2S、PH3等杂质气体。
CaC2+CO。德国化学家维勒发现,电石与水反应释放出乙炔气体(C2H2)和氢氧化钙,也含有H2S、PH3等杂质气体。回答下列问题:
(1)上述六种元素中,电负性最大的是
(2)H2S、PH3分子中心原子的价层电子对数目
 离子的电子式
离子的电子式(3)已知键能数据如下表:
| 化学键 | N-N | N= N | N=N |
| 键能/kJ.mol-1 | 247 | 418 | 942 |
| 化学键 | C-O | C=O | C=O |
| 键能/kJ. mol-1 | 351 | 745 | 1072 |
(4)如图为电石的四方晶胞(长方体),钙离子位于
 离子围成的八面体空隙。计算一个晶胞内含有化学式的数量为
离子围成的八面体空隙。计算一个晶胞内含有化学式的数量为
(5)已知电石密度为2.13 g·cm-3,阿伏加德罗常数为6.02×1023 mol-1,x、y值均为a
 (1
(1 =10-10m),则z=
=10-10m),则z= 中心有
中心有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】已知X、Y和Z三种元素的原子序数之和等于48。X的一种1∶1型氢化物分子中既有σ键又有π键。Z是金属元素,Z的单质和化合物有广泛的用途。已知Z的核电荷数小于28,且次外层有2个未成对电子。工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐)。M有显著的“压电性能”,应用于超声波的发生装置。经X射线分析,M晶体的最小重复单元为正方体(如图),边长为4.03×10-10 m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占。
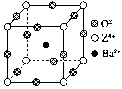
(1)Y在周期表中位于________________ ;
(2)与钡同族的镁钙锶的碳酸盐受热分解的温度从上至下逐渐_______ 填“升高”或“降低”),原因是______________________________ 。
(3)①制备M的化学方程式是__________________________________ 。
②在M晶体中,若将Z4+置于正方体的体心,Ba2+置于正方体的顶点,则O2-处于正方体的________ 。
③在M晶体中,Z4+的氧配位数为________ 。
④已知O2-半径为1.40×10-10 m,则Z4+半径为____________________ m。

(1)Y在周期表中位于
(2)与钡同族的镁钙锶的碳酸盐受热分解的温度从上至下逐渐
(3)①制备M的化学方程式是
②在M晶体中,若将Z4+置于正方体的体心,Ba2+置于正方体的顶点,则O2-处于正方体的
③在M晶体中,Z4+的氧配位数为
④已知O2-半径为1.40×10-10 m,则Z4+半径为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】已知X、Y、Z、R都是周期表中前四周期的元素,它们的核电荷数依次增大。X是空气中含量最高的元素,Z基态原子核外K、L、M三层电子数之比为1:4:2,R基态原子的3d原子轨道上的电子数是4s原子轨道上的4倍,Y基态原子的最外层电子数等于Z、R基态原子的最外层电子数之和。(提示:答题时,X、Y、Z、R用所对应的元素符号表示)
(1)X元素在周期表中的位置_______________ (周期和族),Y元素属于_______________ 区元素;
(2)基态Z原子所占的最高能级的轨道是_______________ 形,基态R原子含有_______________ 种运动状态不同的电子;
(3)化合物Z3X4熔点高达1900℃以上,硬度很大。该物质的晶体类型是_______________ ;
(4)Y、Z形成的某晶体其晶胞结构如下图所示,则该化合物的化学式为_______________ ;
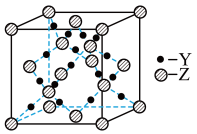
(5)R元素能形成化学式为[R(NH3)4(H2O)2]Cl2的配合物,该配合物所含的化学键种类有_______________ ,
a.离子键b.非极性共价键c氢键d.配位键
该配合物的配位体是_______________ ,1mol[R(NH3)4(H2O)2]Cl2中含有σ建的数目为_______________ ;
(6)R元素通常形成面心立方最密堆积的晶体,其模型结构如下图,该晶体的空间利用率为_______________ (用含计π算式表示)。

(1)X元素在周期表中的位置
(2)基态Z原子所占的最高能级的轨道是
(3)化合物Z3X4熔点高达1900℃以上,硬度很大。该物质的晶体类型是
(4)Y、Z形成的某晶体其晶胞结构如下图所示,则该化合物的化学式为

(5)R元素能形成化学式为[R(NH3)4(H2O)2]Cl2的配合物,该配合物所含的化学键种类有
a.离子键b.非极性共价键c氢键d.配位键
该配合物的配位体是
(6)R元素通常形成面心立方最密堆积的晶体,其模型结构如下图,该晶体的空间利用率为

您最近一年使用:0次



