对于反应N2(g)+3H2(g) 2NH3(g) △H< 0 ,下列说法正确的是
2NH3(g) △H< 0 ,下列说法正确的是
 2NH3(g) △H< 0 ,下列说法正确的是
2NH3(g) △H< 0 ,下列说法正确的是| A.缩小容器体积,N2的浓度比压缩前大 |
| B.及时将产生的氨气液化分离,可加快正反应速率 |
| C.升高温度,该反应的正反应速率减小,逆反应速率增大 |
| D.选用优质催化剂,能够降低合成氨反应的焓变 |
更新时间:2022-11-30 15:00:09
|
相似题推荐
单选题
|
较易
(0.85)
名校
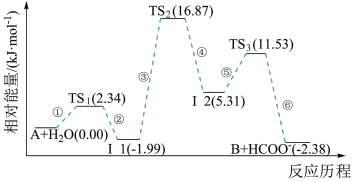
【推荐1】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。
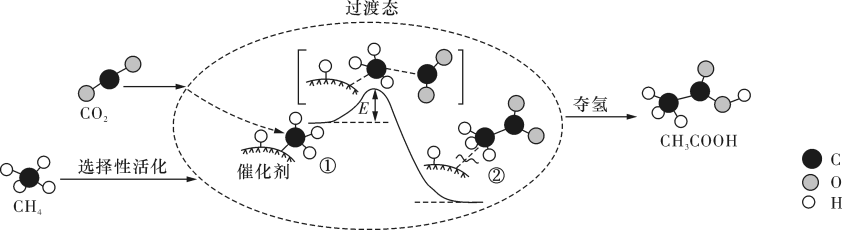
下列说法不正确的是

下列说法不正确的是
| A.生成CH3COOH总反应的原子利用率为100% | B.CH4→CH3COOH过程中,有C―H键发生断裂 |
| C.①→②放出能量并形成了C―C键 | D.该催化剂可有效降低该反应的反应热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列各组物质进行反应(表内物质均为反应物),反应刚开始时,放出H2的速率最快的是
| 选项 | 金属(粉末状) | 酸及其浓度 | 酸的体积/mL | 反应起始温度/℃ |
| A | 0.1 mol Zn | 3 mol·L-1硝酸 | 10 | 30 |
| B | 0.1 mol Zn | 3 mol·L-1硫酸 | 20 | 15 |
| C | 0.1 mol Zn | 3 mol·L-1硫酸 | 10 | 30 |
| D | 0.1 mol Zn | 3 mol·L-1盐酸 | 40 | 30 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】汽车尾气含氮氧化物(NOx)、碳氢化合物(CxHy)、碳等,直接排放容易造成“雾霾”。因此,不少汽车都安装尾气净化装置(净化处理过程如图)。下列有关叙述错误的是
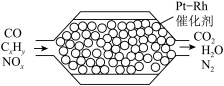

| A.Pt−Rh催化剂可提高尾气净化反应的平衡转化率 |
| B.使用氢氧燃料电池作汽车动力能有效控制雾霾 |
| C.尾气造成“雾霾”与汽油未充分燃烧有关 |
| D.尾气处理过程,氮氧化物(NOx)被还原 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】汽车尾气无害化处理的反应为2NO(g)+2CO(g)⇌N2(g)+2CO2(g) ΔH<0。下列说法不正确的是
| A.升高温度,活化分子百分数增大,正、逆反应速率都加快 |
| B.使用催化剂,活化分子百分数增大,正、逆反应速率都加快 |
| C.使用催化剂可以降低反应的活化能 |
| D.升高温度,上述反应的平衡常数会增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是| A.达到化学平衡时,4v正(O2)=5v逆(NO) |
| B.加入合适的催化剂,可使平衡正向移动 |
| C.达到化学平衡时,若增大容器体积,则正反应速率减小,逆反应速率增大 |
| D.若单位时间内生成n mol NO,同时消耗n mol NH3,则反应达到平衡状态 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】Fe氧簇MOF催化 与
与 反应的机理如图所示。下列说法错误的是
反应的机理如图所示。下列说法错误的是

 与
与 反应的机理如图所示。下列说法错误的是
反应的机理如图所示。下列说法错误的是
A.总反应方程式为 |
B. 为该反应的催化剂 为该反应的催化剂 |
| C.该反应中存在极性键的断裂和非极性键的形成 |
D.根据 分子的结构推测其电子式为: 分子的结构推测其电子式为: |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】在接触法制硫酸的工业生产中,下列生产操作及其原因解释二者都正确的是
| A.硫铁矿燃烧前需要粉碎,因为块状硫铁矿不能燃烧 |
| B.SO2氧化为SO3时需要高压,这样可以提高SO2的转化率 |
| C.SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率 |
| D.用98.3%的浓H2SO4吸收SO3,可以防止形成酸雾阻碍SO3的吸收 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】在一定的条件下,反应CO+NO2 CO2+NO达到平衡后,降低温度,混合气体的颜色变浅,下列判断正确的是
CO2+NO达到平衡后,降低温度,混合气体的颜色变浅,下列判断正确的是
 CO2+NO达到平衡后,降低温度,混合气体的颜色变浅,下列判断正确的是
CO2+NO达到平衡后,降低温度,混合气体的颜色变浅,下列判断正确的是| A.正反应为吸热反应 | B.正反应为放热反应 |
| C.CO的浓度增大 | D.各物质的浓度不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在K2Cr2O7溶液中存在下列平衡: (黄色)+2H+
(黄色)+2H+ (
(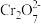 橙色)+H2O中,溶液颜色介于黄色和橙色之间,今欲使
橙色)+H2O中,溶液颜色介于黄色和橙色之间,今欲使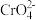 的物质的量增大,可以在溶液中加入①H+ ②OH- ③K+ ④
的物质的量增大,可以在溶液中加入①H+ ②OH- ③K+ ④ ( )
( )
 (黄色)+2H+
(黄色)+2H+ (
(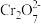 橙色)+H2O中,溶液颜色介于黄色和橙色之间,今欲使
橙色)+H2O中,溶液颜色介于黄色和橙色之间,今欲使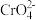 的物质的量增大,可以在溶液中加入①H+ ②OH- ③K+ ④
的物质的量增大,可以在溶液中加入①H+ ②OH- ③K+ ④ ( )
( )| A.①③ | B.②④ | C.①④ | D.②③ |
您最近一年使用:0次
【推荐3】煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) △H 1=+218.4 kJ/mol(反应Ⅰ)
CaO(s)+SO2(g)+CO2(g) △H 1=+218.4 kJ/mol(反应Ⅰ)
CaSO4(s)+4CO(g) CaS(s)+4CO2(g) △H 2=-175.6 kJ/mol (反应Ⅱ)
CaS(s)+4CO2(g) △H 2=-175.6 kJ/mol (反应Ⅱ)
下列有关说法正确的是
CaSO4(s)+CO(g)
 CaO(s)+SO2(g)+CO2(g) △H 1=+218.4 kJ/mol(反应Ⅰ)
CaO(s)+SO2(g)+CO2(g) △H 1=+218.4 kJ/mol(反应Ⅰ)CaSO4(s)+4CO(g)
 CaS(s)+4CO2(g) △H 2=-175.6 kJ/mol (反应Ⅱ)
CaS(s)+4CO2(g) △H 2=-175.6 kJ/mol (反应Ⅱ)下列有关说法正确的是
| A.提高反应体系的温度,能提高该反应体系中SO2生成量 |
| B.反应Ⅱ在较高的温度下可自发进行 |
C.用生石灰固硫的反应为:4CaO(s)+4SO2(g)  3CaSO4(s)+CaS(s) △H3,则△H3>△H2 3CaSO4(s)+CaS(s) △H3,则△H3>△H2 |
D.由反应Ⅰ和反应Ⅱ可计算出反应CaSO4(s)  CaO(s)+SO3(g)的焓变 CaO(s)+SO3(g)的焓变 |
您最近一年使用:0次

 2SO3(g)的反应速率没有影响的是
2SO3(g)的反应速率没有影响的是

