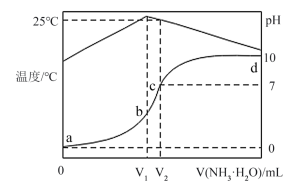
完成下列填空
(1)氯化铝水溶液呈_______ 性,(填“酸”、“中”、“碱”)原因是:_______ (用离子方程式表示)。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是_______
(2)硫化钠溶于水时发生水解,其水解的离子方程为:_______ ,在配制硫化钠溶液时可以加入少量的_______ 以抑制其水解。
(3)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈_______ (填“酸性”、“中性”或“碱性”,下同),溶液中c(Na+)_______ c(CH3COO-)(填“>”、“=”或“<”,下同)。
(4)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈_______ ,溶液中c(Na+)_______ c(CH3COO-)。
(1)氯化铝水溶液呈
(2)硫化钠溶于水时发生水解,其水解的离子方程为:
(3)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈
(4)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈
更新时间:2022-12-27 20:15:28
|
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】请根据要求填空。
(1)在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
①当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是________ 。
②同体积、同PH的三种酸,中和NaOH的能力由大到小的顺序是________ 。
③将PH相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是________ 。
(2)已知:Ksp(AgBr)=7.7×10-13,Ksp(AgSCN)=1×10-12;AgBr(s)+SCN-(aq) AgSCN(s)+Br-(aq)的平衡常数
AgSCN(s)+Br-(aq)的平衡常数____________ 。
(3)已知NH4A溶液为中性,又知将HA溶液加入Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH________ 7(填“<”、“>”或“=”);相同温度下,等物质的量浓度的下列四种盐溶液按pH由大到小的排列顺序是________________ (填序号)。
a.NH4HCO3 b.NH4A c.(NH4)2CO3 d.NH4Cl
(4)在室温下,有下列四种溶液:①NH4Cl②CH3COONH4③NH4HSO4④NH3·H2O,若c(NH4+)相等,则四种溶液的浓度由大到小的排列顺序是__________ (填序号)。
(5)某二元弱酸H2A,已知:Ka1=1.54×10-2,Ka2=1.02×10-7;NaHA溶液显________ 性,原因是_________ 。
(1)在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
①当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是
②同体积、同PH的三种酸,中和NaOH的能力由大到小的顺序是
③将PH相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是
(2)已知:Ksp(AgBr)=7.7×10-13,Ksp(AgSCN)=1×10-12;AgBr(s)+SCN-(aq)
 AgSCN(s)+Br-(aq)的平衡常数
AgSCN(s)+Br-(aq)的平衡常数(3)已知NH4A溶液为中性,又知将HA溶液加入Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH
a.NH4HCO3 b.NH4A c.(NH4)2CO3 d.NH4Cl
(4)在室温下,有下列四种溶液:①NH4Cl②CH3COONH4③NH4HSO4④NH3·H2O,若c(NH4+)相等,则四种溶液的浓度由大到小的排列顺序是
(5)某二元弱酸H2A,已知:Ka1=1.54×10-2,Ka2=1.02×10-7;NaHA溶液显
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】下列各实验中需用浓HCl而不能用稀HCl溶液,写出反应方程式并阐明理由。
(1)配制SnCl2溶液时,将SnCl2(s)溶于浓HCl后再加水冲稀_______ 。
(2)加热MnO2的浓HCl溶液制取氯气_______ 。
(3)需用浓HCl溶液配制王水才能溶解金_______ 。
(1)配制SnCl2溶液时,将SnCl2(s)溶于浓HCl后再加水冲稀
(2)加热MnO2的浓HCl溶液制取氯气
(3)需用浓HCl溶液配制王水才能溶解金
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】软锰矿(主要成分MnO2,含Fe,Al2O3,MgO杂质)的水悬浊液与烟气中的SO2反应可制备MnSO4·H2O,MnO2与SO2反应的化学方程式为MnO2 +SO2=MnSO4。已知下列信息:
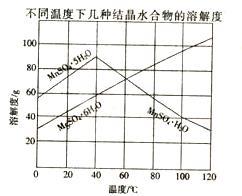
室温下几种氢氧化物的溶度积
回答下列问题:
(1)质量为17.40 g纯净MnO2最多能氧化____ L(标准状况) SO2。
(2)悬浊液吸收烟气后,Fe首先转化为Fe2+进入溶液,然后被_____ 氧化为Fe3+;要证明溶液中存在Fe3+,可选择的试剂是_____ (填标号)。
a.KMnO4溶液 b.KCl溶液 c.KSCN溶液 d.KNO3溶液
(3)室温下,将吸收液过滤,在滤液中加入CaCO3,可除去MnSO4溶液中的Fe3+、Al3+,原因是________ 。
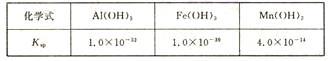
(4)从MnSO4和MgSO4混合溶液中结晶MnSO4·H2O晶体,需控制结晶温度范围为__________ 。

室温下几种氢氧化物的溶度积

回答下列问题:
(1)质量为17.40 g纯净MnO2最多能氧化
(2)悬浊液吸收烟气后,Fe首先转化为Fe2+进入溶液,然后被
a.KMnO4溶液 b.KCl溶液 c.KSCN溶液 d.KNO3溶液
(3)室温下,将吸收液过滤,在滤液中加入CaCO3,可除去MnSO4溶液中的Fe3+、Al3+,原因是
(4)从MnSO4和MgSO4混合溶液中结晶MnSO4·H2O晶体,需控制结晶温度范围为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】硫代硫酸钠(Na2S2O3)是一种常用的化工原料,常用作除氯剂等。回答下列问题:
(1)硫代硫酸钠中所含的化学键类型为_______________________ 。
(2)硫代硫酸钠在中性或碱性溶液中稳定,在酸性溶液中不稳定。向pH=2的硫酸中滴加Na2S2O3溶液,可观察到的现象是________________ 。
(3)实验测定Na2S2O3溶液呈弱碱性,用离子方程式解释其主要原因:__________ ,25℃时该离子反应的平衡常数值约为__________________
【已知:25℃时K1(H2S2O3)=2.52×10-1mol/L,K2(H2S2O3)=1.02xl0-2mol/L】
(4)实际生产中,一般将Na2S和Na2CO3以物质的量比2∶1配成溶液后加热,将SO2缓缓通入溶液中,即可得到硫代硫酸钠。反应的化学方程式为_______________________ 。
(5)在水产养殖上,硫代硫酸钠常用于除去自来水中的氯气,理论上,去除1g的氯需要0.56g硫代硫酸钠。硫代硫酸钠作除氯剂的主要原因是其具有_________ 性,反应的离子方程式为___________________ 。
(1)硫代硫酸钠中所含的化学键类型为
(2)硫代硫酸钠在中性或碱性溶液中稳定,在酸性溶液中不稳定。向pH=2的硫酸中滴加Na2S2O3溶液,可观察到的现象是
(3)实验测定Na2S2O3溶液呈弱碱性,用离子方程式解释其主要原因:
【已知:25℃时K1(H2S2O3)=2.52×10-1mol/L,K2(H2S2O3)=1.02xl0-2mol/L】
(4)实际生产中,一般将Na2S和Na2CO3以物质的量比2∶1配成溶液后加热,将SO2缓缓通入溶液中,即可得到硫代硫酸钠。反应的化学方程式为
(5)在水产养殖上,硫代硫酸钠常用于除去自来水中的氯气,理论上,去除1g的氯需要0.56g硫代硫酸钠。硫代硫酸钠作除氯剂的主要原因是其具有
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】25℃时,如果取0.1 mol·L-1HA溶液与0.1 mol·L-1NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因_______ (用离子方程式表示);
(2)混合溶液中由水电离出的c(H+)_______ 0.1 mol·L-1 NaOH溶液中由水电离出的c(H+);(填>、<、=)
(3)将混合溶液从25 ℃升温至30 ℃,溶液中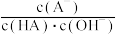 将
将 _______ (填增大或减小)
(4)求出混合液中下列算式的计算结果(填具体数字):c (HA)+c (A-)=_______ mol·L-1;
(5)若向0.1 mol·L-1HA溶液中加入少量水,溶液中 将
将_______ (填增大或减小)
(6)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,将相同温度下相同浓度的四种盐溶液:A.NH4HCO3;B.NH4A;C.(NH4)2SO4;D.NH4Cl,按pH由大到小的顺序排列_______ (填序号)
(1)混合溶液的pH=8的原因
(2)混合溶液中由水电离出的c(H+)
(3)将混合溶液从25 ℃升温至30 ℃,溶液中
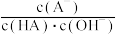 将
将 (4)求出混合液中下列算式的计算结果(填具体数字):c (HA)+c (A-)=
(5)若向0.1 mol·L-1HA溶液中加入少量水,溶液中
 将
将(6)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,将相同温度下相同浓度的四种盐溶液:A.NH4HCO3;B.NH4A;C.(NH4)2SO4;D.NH4Cl,按pH由大到小的顺序排列
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】水是生命的源泉、工业的血液、城市的命脉。要保护好河流,河水是主要的饮用水源,污染物通过饮用水可直接毒害人体,也可通过食物链和灌溉农田间接危及健康。
请回答下列问题:
(1)25℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为___ ,由水电离出的c(OH-)=____ mol·L-1。
(2)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
①25℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三溶液的pH由大到小的顺序为___ (用化学式表示)。
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为____ 。
(3)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=___ mol·L-1(填精确值),c(CH3COO-)/c(CH3COOH)=___ 。
请回答下列问题:
(1)25℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为
(2)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三溶液的pH由大到小的顺序为
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为
(3)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】25℃时,有浓度均为0.1mol•L-1的下列4种溶液:
①NaCN溶液 ②NaOH溶液 ③CH3COONa溶液 ④Na2CO3溶液
(1)H3PO2是一元中强酸,具有较强的还原性。写出其电离方程式______ 。
(2)上述4种溶液pH最小的是______ (填序号),其中②由水电离的H+浓度为_____ mol•L-1。
(3)①中各离子浓度由大到小的顺序是______ 。
(4)现有浓度为0.02mol/L的HCN与0.01moL/LNaOH等体积混合后(忽略体积变化),测得c(Na+)>c(CN-),下列关系正确的是______ 。(填标号)
(5)25℃时,测得HCN和NaCN的混合溶液的pH=11,则 约为
约为_____ (计算结果保留两位小数)。向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:_____ 。
(6)已知t℃时,Kw=1×10-13,则t℃_____ 25℃(填“>”、“<”或“=”)。在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则 =
=_____ 。
(7)25℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH值pH1与强碱的pH值pH2之间应满足的关系是_____ 。
①NaCN溶液 ②NaOH溶液 ③CH3COONa溶液 ④Na2CO3溶液
| HCN | H2CO3 | CH3COOH |
| Ka=4.9×10-10 | Ka1=4.4×10-7 Ka2=4.7×10-11 | Ka=1.75×10-5 |
(2)上述4种溶液pH最小的是
(3)①中各离子浓度由大到小的顺序是
(4)现有浓度为0.02mol/L的HCN与0.01moL/LNaOH等体积混合后(忽略体积变化),测得c(Na+)>c(CN-),下列关系正确的是
| A.c(H+)>c(OH-) | B.c(H+)<c(OH-) |
| C.c(H+)+c(HCN)=c(OH-) | D.c(HCN)+c(CN-)=0.01mol/L |
 约为
约为(6)已知t℃时,Kw=1×10-13,则t℃
 =
=(7)25℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH值pH1与强碱的pH值pH2之间应满足的关系是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】钠碱法的启动吸收剂为NaOH溶液,捕捉SO2后生成Na2SO3和NaHSO3的混合液。
(1)常温下进行“钠碱法”的模拟实验。用12gNaOH固体配成一定浓度的溶液,这些NaOH理论上最多可吸收SO2的体积约为______ L(折算成标准状况)。若实验时只吸收了0.10molSO2,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为______ 。
(2)当钠碱法的吸收液pH达到4~6时,混合液中含较多量NaHSO3.加热该溶液可回收得到较高纯度的SO2,剩余溶液可循环使用,进一步吸收SO2,剩余溶液的主要溶质是______ (填写化学式)。
(3)将SO2通入NaOH溶液时,得到一组c(H2SO3)+c(HSO )+c(SO
)+c(SO )=0.100mol·L-1的混合溶液,溶液中部分微粒的物质的量浓度随pH的关系曲线如下图所示。
)=0.100mol·L-1的混合溶液,溶液中部分微粒的物质的量浓度随pH的关系曲线如下图所示。
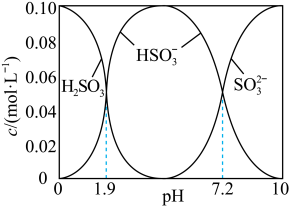
若溶液的pH=7,溶液中c(Na+)=c( )+
)+______ ,此时溶液中c(Na+)______ 0.100mol·L-1.(选填“>”、“<”或“=”)
(4)上述混合液中存在多个水解平衡,与化学平衡一样,水解平衡也有自己的平衡常数(Kh)。以醋酸钠(CH3COONa)为例,其水解平衡常数存在以下定量关系:Kh=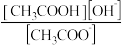
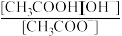 =
=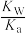 (Kw为水的离子积常数,Ka为CH3COOH的电离常数)亚硫酸为二元弱酸,25℃时,其电离常数Ka1=1.54×10-2,Ka2=1.02×10-7。请结合相关数据说明NaHSO3溶液呈酸性的理由。
(Kw为水的离子积常数,Ka为CH3COOH的电离常数)亚硫酸为二元弱酸,25℃时,其电离常数Ka1=1.54×10-2,Ka2=1.02×10-7。请结合相关数据说明NaHSO3溶液呈酸性的理由。______ 。
(5)“钙碱法”的工作原理与“钠碱法”相似,一般选择消石灰的悬浊液为SO2吸收剂。请对照“钠碱法”,尝试通过比较反应物和生成物的不同性质,从生产成本和设备维护两方面对“钙碱法”做出评价______ 。
(1)常温下进行“钠碱法”的模拟实验。用12gNaOH固体配成一定浓度的溶液,这些NaOH理论上最多可吸收SO2的体积约为
(2)当钠碱法的吸收液pH达到4~6时,混合液中含较多量NaHSO3.加热该溶液可回收得到较高纯度的SO2,剩余溶液可循环使用,进一步吸收SO2,剩余溶液的主要溶质是
(3)将SO2通入NaOH溶液时,得到一组c(H2SO3)+c(HSO
 )+c(SO
)+c(SO )=0.100mol·L-1的混合溶液,溶液中部分微粒的物质的量浓度随pH的关系曲线如下图所示。
)=0.100mol·L-1的混合溶液,溶液中部分微粒的物质的量浓度随pH的关系曲线如下图所示。
若溶液的pH=7,溶液中c(Na+)=c(
 )+
)+(4)上述混合液中存在多个水解平衡,与化学平衡一样,水解平衡也有自己的平衡常数(Kh)。以醋酸钠(CH3COONa)为例,其水解平衡常数存在以下定量关系:Kh=
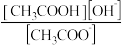
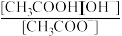 =
=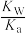 (Kw为水的离子积常数,Ka为CH3COOH的电离常数)亚硫酸为二元弱酸,25℃时,其电离常数Ka1=1.54×10-2,Ka2=1.02×10-7。请结合相关数据说明NaHSO3溶液呈酸性的理由。
(Kw为水的离子积常数,Ka为CH3COOH的电离常数)亚硫酸为二元弱酸,25℃时,其电离常数Ka1=1.54×10-2,Ka2=1.02×10-7。请结合相关数据说明NaHSO3溶液呈酸性的理由。(5)“钙碱法”的工作原理与“钠碱法”相似,一般选择消石灰的悬浊液为SO2吸收剂。请对照“钠碱法”,尝试通过比较反应物和生成物的不同性质,从生产成本和设备维护两方面对“钙碱法”做出评价
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为: H2SO4= H++HSO , HSO
, HSO
 H++SO
H++SO 。
。
请回答下列有关问题:
(1)Na2SO4溶液呈_______ (填“弱酸性”、“中性”或“弱碱性”),其理由是_______ (用离子方程式表示);
(2)NaHSO4溶液与BaCl2溶液反应的离子方程式为_______ ;
(3)在0.10mol・L-1的Na2SO4溶液中,下列离子浓度关系正确的是_______(填写编号);
(4)写出NaHSO4溶液中溶质电离常数(Ka)的表达式_______ ;
(5)若25℃时,0.10mol・L-1的NaHSO4溶液中c(SO )=0.029mol・L-1,则0.10mol・L-1的H2SO4溶液中c(SO
)=0.029mol・L-1,则0.10mol・L-1的H2SO4溶液中c(SO )
)_______ 0.029mol・L-1(填“<”、“>”或“=”),其理由是_______ ;
(6)如果25℃时,0.10mol・L-1H2SO4溶液的pH=-1g0.11,则0.10mol・L-1的H2SO4溶液中c(SO )=
)=_______ mol・L-1。
 , HSO
, HSO
 H++SO
H++SO 。
。请回答下列有关问题:
(1)Na2SO4溶液呈
(2)NaHSO4溶液与BaCl2溶液反应的离子方程式为
(3)在0.10mol・L-1的Na2SO4溶液中,下列离子浓度关系正确的是_______(填写编号);
A.c(Na+)=c(SO )+c(HSO )+c(HSO )+c(H2SO4) )+c(H2SO4) |
B.c(OH-)=c(HSO )+c(H+) )+c(H+) |
C.c(Na+)+c(H+)=c(OH-)+c(HSO )+2c(SO )+2c(SO ) ) |
D.c(Na+)=2c(SO )+2c(HSO )+2c(HSO ) ) |
(5)若25℃时,0.10mol・L-1的NaHSO4溶液中c(SO
 )=0.029mol・L-1,则0.10mol・L-1的H2SO4溶液中c(SO
)=0.029mol・L-1,则0.10mol・L-1的H2SO4溶液中c(SO )
)(6)如果25℃时,0.10mol・L-1H2SO4溶液的pH=-1g0.11,则0.10mol・L-1的H2SO4溶液中c(SO
 )=
)=
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】将0.4mol·L-1HA溶液与0.2mol·L-1NaOH溶液等体积混合,测得混合溶液中c(Na+)﹥c(A-),则:
(1)混合溶液中c(A-)_________ c(HA)(填“﹥”“﹤”或“=”)
(2)混合溶液中c(HA)+ c(A-)__________ 0.2mol·L-1(填“﹥”“﹤”或“=”)
(3)25℃时,如果取0.4 mol·L-1HA溶液与0.2mol·L-1NaOH溶液等体积混合,若测得混合溶液的pH=8,则c(Na+)-c(A-)=___________ 。(填准确数值)
(1)混合溶液中c(A-)
(2)混合溶液中c(HA)+ c(A-)
(3)25℃时,如果取0.4 mol·L-1HA溶液与0.2mol·L-1NaOH溶液等体积混合,若测得混合溶液的pH=8,则c(Na+)-c(A-)=
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看作化学平衡的一种.请根据所学化学知识回答下列问题:
(1)草酸是二元弱酸,草酸氢钾溶液呈酸性.在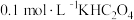 溶液中,下列关系正确的是
溶液中,下列关系正确的是________ (填字母).
A.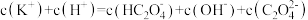
B.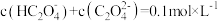
C.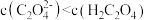
D.
(2)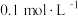 的
的 溶液中存在的平衡有(用离子方程式表示)
溶液中存在的平衡有(用离子方程式表示)__________________ 、____________________ 、____________________ .
(3)MOH和ROH两种一元碱的溶液分别加水稀释时的pH变化如图所示.下列叙述中不正确的是________ (填字母)
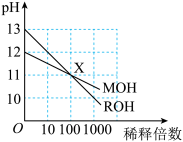
A.ROH是一种强碱
B.在X点,MOH未完全电离
C.在X点,
D.稀释前,
(4)AgCl在溶液中存在如下平衡: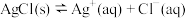 AgCl,在25 ℃时,AgCl的
AgCl,在25 ℃时,AgCl的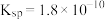 .现将足量的AgCl分别加入下列液体中:①100 mL蒸馏水,②100mL
.现将足量的AgCl分别加入下列液体中:①100 mL蒸馏水,②100mL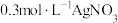 溶液,③100 mL
溶液,③100 mL 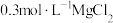 溶液,充分搅拌后冷却到相同温度,
溶液,充分搅拌后冷却到相同温度, 浓度由大到小的顺序为
浓度由大到小的顺序为________ (填序号),向50 mL 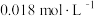 的
的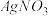 溶液中加入50 mL
溶液中加入50 mL  的盐酸,沉淀生成后溶液中
的盐酸,沉淀生成后溶液中 是
是________ 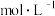 .如果向生成沉淀后的溶液中再加入50 mL
.如果向生成沉淀后的溶液中再加入50 mL 的盐酸,
的盐酸,________ (填“能”或“不能”)产生沉淀.
(1)草酸是二元弱酸,草酸氢钾溶液呈酸性.在
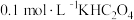 溶液中,下列关系正确的是
溶液中,下列关系正确的是A.
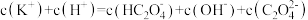
B.
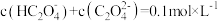
C.
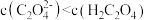
D.

(2)
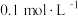 的
的 溶液中存在的平衡有(用离子方程式表示)
溶液中存在的平衡有(用离子方程式表示)(3)MOH和ROH两种一元碱的溶液分别加水稀释时的pH变化如图所示.下列叙述中不正确的是

A.ROH是一种强碱
B.在X点,MOH未完全电离
C.在X点,

D.稀释前,

(4)AgCl在溶液中存在如下平衡:
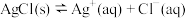 AgCl,在25 ℃时,AgCl的
AgCl,在25 ℃时,AgCl的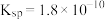 .现将足量的AgCl分别加入下列液体中:①100 mL蒸馏水,②100mL
.现将足量的AgCl分别加入下列液体中:①100 mL蒸馏水,②100mL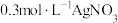 溶液,③100 mL
溶液,③100 mL 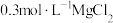 溶液,充分搅拌后冷却到相同温度,
溶液,充分搅拌后冷却到相同温度, 浓度由大到小的顺序为
浓度由大到小的顺序为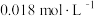 的
的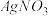 溶液中加入50 mL
溶液中加入50 mL  的盐酸,沉淀生成后溶液中
的盐酸,沉淀生成后溶液中 是
是 .如果向生成沉淀后的溶液中再加入50 mL
.如果向生成沉淀后的溶液中再加入50 mL 的盐酸,
的盐酸,
您最近一年使用:0次