 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.1L 溴化铵水溶液中 溴化铵水溶液中 与 与 的数目之和大于 的数目之和大于 |
B.标准状况下,22.4L 中含有 中含有 键的数目为 键的数目为 |
C.14g聚丙烯中含有的原子总数为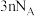 |
D.3mol 与 与 完全反应时转移的电子数为 完全反应时转移的电子数为 |
更新时间:2023-01-05 22:21:19
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列叙述正确的是
| A.O2的摩尔体积约为22.4L |
| B.1molCO2的质量为44g/mol |
| C.80g NaOH溶解在水中配成1L溶液,所得溶液中溶质的物质的量浓度为2mol/L |
| D.18g H2O在标准状况下的体积约为22.4L |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列叙述正确的是
A.1mol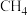 的质量为16 的质量为16 |
B.标准状况下,1mol 体积约为22.4L 体积约为22.4L |
C.1L1 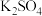 溶液中 溶液中 的物质的量为2mol 的物质的量为2mol |
D.从1L0.5 NaCl溶液中取出100mL,剩余溶液中 NaCl溶液中取出100mL,剩余溶液中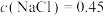  |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】用 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是A.标准状况下,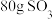 体积约为 体积约为 |
B.常温常压下,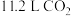 含有的原子数为 含有的原子数为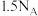 |
C.标准状况下,含有 个氦原子的氦气体积约为11.2L 个氦原子的氦气体积约为11.2L |
D.标准状况下,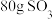 中含有的原子数为 中含有的原子数为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】已知常温下,在溶液中可发生以下两个反应:①Cl2 + 2Br- = Br2 + 2Cl-;②Br2 + 2Fe2+ = 2Fe3+ + 2Br-。现将标准状况下 1.12L 的氯气通入 1L 0.05mol/L 的 FeBr2溶液中,由此判断下列说法正确的是
| A.氧化性强弱:Cl2 > Fe3+ > Br2 | B.还原性强弱:Br- >Fe2+ >Cl- |
| C.反应后溶液中 c(Fe3+):c(Br- ) =1:1 | D.反应后溶液中 c(Fe2+):c(Cl-) =1:2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温下,39g Na2O2中含有的共用电子对数目为NA |
B.0.1mol•L﹣1NaHSO3溶液中的HSO 数目小于NA 数目小于NA |
| C.标准状况下,22.4L Cl2与足量CH4反应时转移的电子数目为2NA |
| D.1mol C2H4O2中含有的C﹣H键数目一定为4NA |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】除去下列杂质的操作方法错误的是
A.除去 中混有的 中混有的 :用加热法 :用加热法 |
B.除去 中混有的HCl气体:用饱和 中混有的HCl气体:用饱和 溶液洗气 溶液洗气 |
C.除去 中混有的HCl气体:用饱和食盐水洗气 中混有的HCl气体:用饱和食盐水洗气 |
D.除去NO中混有的少量 气体:用水洗气 气体:用水洗气 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列有关NO2性质的叙述不正确的是
| A.常温下是红棕色气体,易溶于水 |
| B.能与水反应生成硝酸并放出一氧化氮 |
| C.密度大于空气,可用向下排空气法收集 |
| D.是形成光化学烟雾的一种有毒气体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】20℃时,向20mL0.1 mol∙L−1醋酸溶液中不断滴入0.1 mol∙L−1NaOH(aq),溶液pH变化如图所示,则下列离子浓度关系错误的是


| A.a点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| B.b点:c(Na+)=c(CH3COO-)>c(H+)=c(OH-) |
| C.c点:c(H+)=c(CH3COOH)+c(OH-) |
| D.d点:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】室温下,向20.0 mL 0.100 mol∙L−1的某弱酸HA的溶液中滴加同浓度的NaOH溶液,过程中 随pH的变化关系如下图所示。下列说法不正确的是
随pH的变化关系如下图所示。下列说法不正确的是

 随pH的变化关系如下图所示。下列说法不正确的是
随pH的变化关系如下图所示。下列说法不正确的是
A.a到c的过程中, 为定值 为定值 |
| B.a到c的过程中,水的电离程度不断减小 |
C.b点时,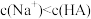 |
| D.c点时加入碱的体积小于20 mL |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列说法中正确的是
A.常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c( )、c(H+)均下降 )、c(H+)均下降 |
B.pH=8.3的NaHCO3溶液:c(Na+)>c( )>c( )>c( )>c(H2CO3) )>c(H2CO3) |
C.常温下,c( )相等的①(NH4)2SO4 ②(NH4)2Fe(SO4)2 ③NH4Cl ④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③ )相等的①(NH4)2SO4 ②(NH4)2Fe(SO4)2 ③NH4Cl ④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③ |
D.当溶液中存在的离子只有Cl-、OH-、 、H+时,该溶液中离子浓度大小关系可能为c(Cl-)>c( 、H+时,该溶液中离子浓度大小关系可能为c(Cl-)>c( )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
您最近一年使用:0次



