钒的化合物能有效调节血糖,化合物丁有望成为抗糖尿病的新型药物,其制备流程如下:
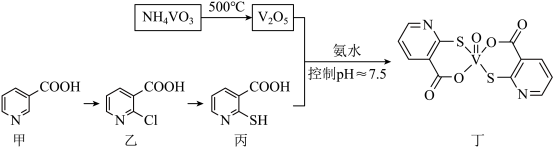
(1)钒在元素周期表中的位置为_______ ,基态V的原子结构示意图为_______ 。
(2) 转化为
转化为 的化学方程式是
的化学方程式是_______ 。
(3)下列说法正确的是_______(填字母)
(4)分析丙的分子结构与性质
①比较丙中 键角和
键角和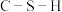 键角的大小并解释原因:
键角的大小并解释原因:_______
②丙为有机弱酸,请写出1mol丙与2mol一水合氨反应的离子方程式_______ 。
(5)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域 键”,下列物质中存在“离域
键”,下列物质中存在“离域 键”的是_______。
键”的是_______。
(6)丁是一种配合物含有化合物丁的样品中,含钒量的测定方法是:先把样品中的钒元素经处理转化为 溶液,再用硫酸酸化的
溶液,再用硫酸酸化的 标准溶液进行滴定,生成
标准溶液进行滴定,生成 。取样品10.2g,用上述方法测定其中钒的含量,消耗
。取样品10.2g,用上述方法测定其中钒的含量,消耗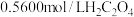 标准溶液25.00mL,则样品中钒元素的质量分数为
标准溶液25.00mL,则样品中钒元素的质量分数为_______ (写出计算结果)。

(1)钒在元素周期表中的位置为
(2)
 转化为
转化为 的化学方程式是
的化学方程式是(3)下列说法正确的是_______(填字母)
A.元素的第一电离能: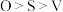 |
B.共价键的极性:丙中 乙中 乙中 |
| C.甲分子中所有原子可能在同一平面内 |
D.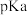 :乙>甲 :乙>甲 |
①比较丙中
 键角和
键角和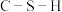 键角的大小并解释原因:
键角的大小并解释原因:②丙为有机弱酸,请写出1mol丙与2mol一水合氨反应的离子方程式
(5)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域
 键”,下列物质中存在“离域
键”,下列物质中存在“离域 键”的是_______。
键”的是_______。A. | B. | C. | D. |
 溶液,再用硫酸酸化的
溶液,再用硫酸酸化的 标准溶液进行滴定,生成
标准溶液进行滴定,生成 。取样品10.2g,用上述方法测定其中钒的含量,消耗
。取样品10.2g,用上述方法测定其中钒的含量,消耗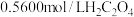 标准溶液25.00mL,则样品中钒元素的质量分数为
标准溶液25.00mL,则样品中钒元素的质量分数为
更新时间:2023-01-10 20:34:59
|
相似题推荐
【推荐1】用含铬不锈钢废渣(含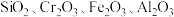 等)制取
等)制取 (铬绿)的工艺流程如图所示:
(铬绿)的工艺流程如图所示:
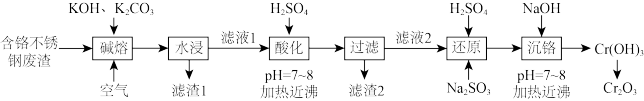
已知:滤液1:含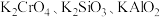 滤液2:含
滤液2:含 等
等
回答下列问题:
(1)“碱熔”时,为使废渣充分氧化可采取的措施是_______ (任写一条)。
(2) 反应生成
反应生成 的化学方程式为
的化学方程式为_______ 。
(3)“水浸”时,碱熔渣中的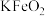 强烈水解生成的难溶物为
强烈水解生成的难溶物为_______ (填化学式);为检验“水浸”后的滤液中是否含有 的操作是
的操作是_______ 。
(4)“还原”时发生反应的离子方程式为_______ 。
(5)工业上可用含铬矿石制得 后,通过铝热反应制备金属铬。氧铬酸钙是一种常见含铬矿石,其立方晶胞如图所示。
后,通过铝热反应制备金属铬。氧铬酸钙是一种常见含铬矿石,其立方晶胞如图所示。

①已知A、B的原子坐标分别为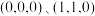 ,则C的原子坐标为
,则C的原子坐标为_______ 。
②1个钙原子与_______ 个氧原子等距离且最近。
③该晶体密度为_______  (列出计算式即可可。已知钙和氧的最近距离为
(列出计算式即可可。已知钙和氧的最近距离为 ,
, 代表阿伏加德罗常数。
代表阿伏加德罗常数。
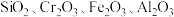 等)制取
等)制取 (铬绿)的工艺流程如图所示:
(铬绿)的工艺流程如图所示:
已知:滤液1:含
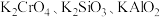 滤液2:含
滤液2:含 等
等回答下列问题:
(1)“碱熔”时,为使废渣充分氧化可采取的措施是
(2)
 反应生成
反应生成 的化学方程式为
的化学方程式为(3)“水浸”时,碱熔渣中的
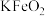 强烈水解生成的难溶物为
强烈水解生成的难溶物为 的操作是
的操作是(4)“还原”时发生反应的离子方程式为
(5)工业上可用含铬矿石制得
 后,通过铝热反应制备金属铬。氧铬酸钙是一种常见含铬矿石,其立方晶胞如图所示。
后,通过铝热反应制备金属铬。氧铬酸钙是一种常见含铬矿石,其立方晶胞如图所示。
①已知A、B的原子坐标分别为
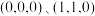 ,则C的原子坐标为
,则C的原子坐标为②1个钙原子与
③该晶体密度为
 (列出计算式即可可。已知钙和氧的最近距离为
(列出计算式即可可。已知钙和氧的最近距离为 ,
, 代表阿伏加德罗常数。
代表阿伏加德罗常数。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】为了探究Fe3+、Fe2+、Cu2+、Ag+的氧化性强弱,设计实验如图所示。请回答:
(1)写出AgNO3的电离方程式:___________ 。
(2)实验Ⅰ、Ⅱ的现象和结论如表:

①实验Ⅰ的现象___________ 。②实验Ⅱ的结论___________ 。
③写出实验Ⅱ中发生反应的离子方程式:___________ 。
④写出实验Ⅲ中发生反应的离子方程式:___________ 。
(3)Fe、Cu、CuSO4溶液、AgNO3溶液均能导电,CuSO4溶液、AgNO3溶液能导电的原因是___________ 。
(4)实验Ⅱ中的AgNO3完全反应后,抽出铜丝,洗净后干燥,称重,发现铜丝比反应前增重0.152g,则反应生成的Ag的质量为___________ g。
(1)写出AgNO3的电离方程式:
(2)实验Ⅰ、Ⅱ的现象和结论如表:

| 实验编号 | 实验现象 | 实验结论 |
| Ⅰ | ① | 氧化性:Cu2+>Fe2+ |
| Ⅱ | 溶液变蓝色 | ② |
| Ⅲ | 铜丝溶解,溶液颜色变浅 | 氧化性:Fe3+>Cu2+ |
③写出实验Ⅱ中发生反应的离子方程式:
④写出实验Ⅲ中发生反应的离子方程式:
(3)Fe、Cu、CuSO4溶液、AgNO3溶液均能导电,CuSO4溶液、AgNO3溶液能导电的原因是
(4)实验Ⅱ中的AgNO3完全反应后,抽出铜丝,洗净后干燥,称重,发现铜丝比反应前增重0.152g,则反应生成的Ag的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
(1)在周期表中,与元素b的化学性质最相似的邻族元素是________ (填写以上表中字母对应的元素符号),该元素基态原子核外M层电子的自旋状态________ (填“相同”或“相反”)。
(2)元素As与________ 同族(填写以上表中字母对应的元素符号),其简单气态氢化物的稳定性由大到小的顺序是________ 。
(3)基态ρ原子成为阳离子时首先失去________ 轨道电子,基态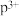 的最外层电子排布式
的最外层电子排布式________ 。
(4)i的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式为________________ 。
(5)下列关于上图表中元素说法正确的是________ (填序号)。
①未成对电子数最多的元素是O
②元素的电负性强弱;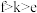
③元素的第一电离能:
④简单离子半径: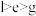
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o | p |
(2)元素As与
(3)基态ρ原子成为阳离子时首先失去
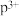 的最外层电子排布式
的最外层电子排布式(4)i的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式为
(5)下列关于上图表中元素说法正确的是
①未成对电子数最多的元素是O
②元素的电负性强弱;
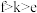
③元素的第一电离能:

④简单离子半径:
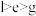
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
(1)请用元素符号完成下列空白:
①元素:A_______ 、B_______ 、C_______ 、D______ 、E______
②B、C、D、E四种元素的第一电离能大小顺序是:___________ 。
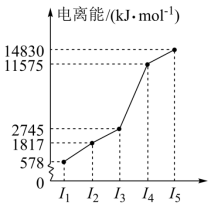
(2)如图是A~F元素中某种元素的部分电离能,由此可判断该元素是___________ 。F元素位于周期表的___________ 区,此区元素的价电子层结构特点是___________ 。
 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。(1)请用元素符号完成下列空白:
①元素:A
②B、C、D、E四种元素的第一电离能大小顺序是:
(2)如图是A~F元素中某种元素的部分电离能,由此可判断该元素是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E为前四周期元素,且原子序数依次增大。气体AB遇空气变红棕色,C原子内层电子数是最外层电子数的5倍,D在同周期元素中电负性最大,E的硫酸盐溶液呈蓝色。回答下列问题:
(1)A原子有________ 种能量不同的电子;D原子的M能层电子的运动状态有________ 种。
(2)元素A的第一电离能________ (填“大于”“小于”或“等于”)元素B的第一电离能;AB2-的立体构型是________ ;气体AB中含有的σ键和π键个数之比为________ 。
(3)元素C与D所形成的化合物的某种晶胞结构如图所示,则晶胞中阴离子与阳离子的个数比是________ .

(4)E基态原子的核外电子排布式为________ ,将E单质的粉末加入A的简单气态氢化物的浓溶液中,并不断鼓入空气充分反应,得到深蓝色的溶液,该反应的离子方程式是________ 。
(1)A原子有
(2)元素A的第一电离能
(3)元素C与D所形成的化合物的某种晶胞结构如图所示,则晶胞中阴离子与阳离子的个数比是

(4)E基态原子的核外电子排布式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】硫铝酸钙化学式为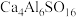 ,可写成
,可写成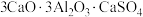 ,是一种常用的混凝土膨胀剂。回答下列问题:
,是一种常用的混凝土膨胀剂。回答下列问题:
(1)基态氧原子的价电子排布图为 ,而不是
,而不是 ,因为核外电子排布应遵循
,因为核外电子排布应遵循_____ (填“泡利原理”或“洪特规则”)。基态Ca原子核外电子占据的最高能层符号是_____ 。
(2) 的中心原子杂化方式为
的中心原子杂化方式为_____ , 可看成是
可看成是 中的一个氧原子被硫原子所替代,则
中的一个氧原子被硫原子所替代,则 -的VSEPR模型名称为
-的VSEPR模型名称为_____ 。
(3)Al的性质与Be的性质相似,可知熔点:
_____  (填“>”或“<”),理由是
(填“>”或“<”),理由是_____ 。
(4) 中存在的作用力有
中存在的作用力有_____ 。
A.离子键 B.共价键 C.范德华力 D.金属键 E.配位键
(5)在空气中灼烧 生成Ag和
生成Ag和 ,
, 分子空间构型为
分子空间构型为_____ ;与 相比,
相比, 的键角更
的键角更_____ (“大”、“小”、“相等”)。
(6)如图是金属氢化物储氢材料,其晶胞如图所示,其化学式为_____ ,已知该晶体的密度为 ,则该晶胞的体积为
,则该晶胞的体积为_____  (用含
(用含 、
、 的代数式表示)
的代数式表示)
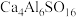 ,可写成
,可写成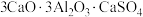 ,是一种常用的混凝土膨胀剂。回答下列问题:
,是一种常用的混凝土膨胀剂。回答下列问题:(1)基态氧原子的价电子排布图为
 ,而不是
,而不是 ,因为核外电子排布应遵循
,因为核外电子排布应遵循(2)
 的中心原子杂化方式为
的中心原子杂化方式为 可看成是
可看成是 中的一个氧原子被硫原子所替代,则
中的一个氧原子被硫原子所替代,则 -的VSEPR模型名称为
-的VSEPR模型名称为(3)Al的性质与Be的性质相似,可知熔点:

 (填“>”或“<”),理由是
(填“>”或“<”),理由是(4)
 中存在的作用力有
中存在的作用力有A.离子键 B.共价键 C.范德华力 D.金属键 E.配位键
(5)在空气中灼烧
 生成Ag和
生成Ag和 ,
, 分子空间构型为
分子空间构型为 相比,
相比, 的键角更
的键角更(6)如图是金属氢化物储氢材料,其晶胞如图所示,其化学式为
 ,则该晶胞的体积为
,则该晶胞的体积为 (用含
(用含 、
、 的代数式表示)
的代数式表示)
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】丹皮酚(G)可用于缓解骨关节炎引起的疼痛,过敏性鼻炎以及感冒。一种合成丹皮酚及其衍生物H的合成路线如下:
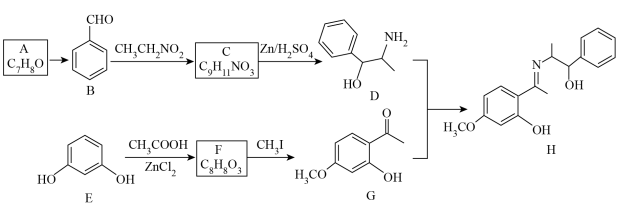
回答下列问题:
(1)E的化学名称为_______ 。
(2)A生成B的反应类型为_______ 。
(3)C的结构简式为_______ 。
(4)D中官能团的名称为_______ 。
(5)H中氮原子的杂化轨道类型为_______ ,手性碳个数为_______ 。
(6)E转变为F的化学方程式为_______ 。
(7)在G的同分异构体中,同时满足下列条件的共有_______ 种(不考虑立体异构);
①与 溶液反应放出
溶液反应放出 ;②与
;②与 溶液显色;③苯环上有两个取代基。其中核磁共振氢谱显示为6组峰,且峰面积比为
溶液显色;③苯环上有两个取代基。其中核磁共振氢谱显示为6组峰,且峰面积比为 的同分异构体的结构简式为
的同分异构体的结构简式为_______ 。

回答下列问题:
(1)E的化学名称为
(2)A生成B的反应类型为
(3)C的结构简式为
(4)D中官能团的名称为
(5)H中氮原子的杂化轨道类型为
(6)E转变为F的化学方程式为
(7)在G的同分异构体中,同时满足下列条件的共有
①与
 溶液反应放出
溶液反应放出 ;②与
;②与 溶液显色;③苯环上有两个取代基。其中核磁共振氢谱显示为6组峰,且峰面积比为
溶液显色;③苯环上有两个取代基。其中核磁共振氢谱显示为6组峰,且峰面积比为 的同分异构体的结构简式为
的同分异构体的结构简式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】金属钛被誉为“二十一世纪金属”,有“生物金属,海洋金属,太空金属”的美称,具有广泛的应用前景。回答下列问题:
(1)钛在周期表中的位置________ ,Ti2+电子占据的最高能层的电子排布式为_________ 。
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO 的空间构型是
的空间构型是___________ ,第一电离能介于Al、P之间的第三周期元素为___________ (填元素符号)。
(3)Ti(BH4)2是一种储氢材料,其中所含元素的电负性由小到大排列顺序为___________ ,B原子的杂化方式是___________ ,其中的BH 可由BH3和H-结合而成。BH
可由BH3和H-结合而成。BH 含有
含有___________ (填序号)
①σ键②π键③氢键④配位键⑤离子键
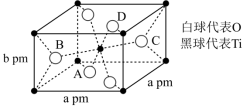
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为___________ g·cm-3(设阿伏加德罗常数的值为NA,用含a、b、NA的代数式表示)。
(1)钛在周期表中的位置
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO
 的空间构型是
的空间构型是(3)Ti(BH4)2是一种储氢材料,其中所含元素的电负性由小到大排列顺序为
 可由BH3和H-结合而成。BH
可由BH3和H-结合而成。BH 含有
含有①σ键②π键③氢键④配位键⑤离子键
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】某小组利用工厂度弃物(主要含MgCO3、MgSiO3、Al2O3和Fe2O3 等)设计回收镁的工艺流程如下:
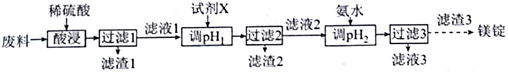
(1)酸浸过程中采用“粉碎废料、加热、搅拌、适当提高稀硫酸的浓度等”措施的目的是____________ 。为了提高产品的纯度,试剂X宜选择_______ (填选项字母)。
A.CuO B.MgO C.MgCO3 D.氨水
(2)滤渣2的主要成分是__________ (填化学式)。
(3)写出生成滤渣3的离子方程式:_______________________ 。
(4)已知:298K时,Ksp[Al(OH)3]=3.0×10-34、Ksp[Fe(OH)3]=4.0×10-38。
①加入试剂X,当Al3+ 开始沉淀时,滤液1中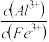 =
=____________ 。
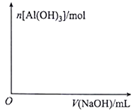
②向浓度均为0.1mol·L-1 的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液。在图中面出生成Al(OH)3的物质的量与滴加NaOH溶液体积的关系图(大致图)。______
(5)若废料中镁元素的质量分数为a%,取mkg废料按上述流程生产,最终回收到20kg纯度为6%的镁锭,则镁的产率为__________ (用含a、b、m 的代数式表示)。
(6)参照上述流程图,设计经三步,由滤渣3得到镁锭的路线:_________________________ 。

(1)酸浸过程中采用“粉碎废料、加热、搅拌、适当提高稀硫酸的浓度等”措施的目的是
A.CuO B.MgO C.MgCO3 D.氨水
(2)滤渣2的主要成分是
(3)写出生成滤渣3的离子方程式:
(4)已知:298K时,Ksp[Al(OH)3]=3.0×10-34、Ksp[Fe(OH)3]=4.0×10-38。
①加入试剂X,当Al3+ 开始沉淀时,滤液1中
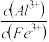 =
=②向浓度均为0.1mol·L-1 的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液。在图中面出生成Al(OH)3的物质的量与滴加NaOH溶液体积的关系图(大致图)。

(5)若废料中镁元素的质量分数为a%,取mkg废料按上述流程生产,最终回收到20kg纯度为6%的镁锭,则镁的产率为
(6)参照上述流程图,设计经三步,由滤渣3得到镁锭的路线:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】硫代硫酸钠(Na2S2O3)是中学阶段常见的化学试剂。
I.它在酸性条件下不稳定,可与稀硫酸发生反应: 。现利用该反应探究外界条件对反应速率的影响。
。现利用该反应探究外界条件对反应速率的影响。
(1)完成此实验设计,其中:V1=_______ ,V2=_______
(2)对比实验1、2可探究_______ 对反应速率的影响。
II.硫代硫酸钠易与空气中的CO2、O2等反应而变质,现有研究性学习小组同学,测定实验室储存的Na2S2O3样品的纯度。方法如下:准确称取10.00g样品,用蒸馏水溶解并定容至250mL,准确移取该溶液25.00mL于锥形瓶中,加入2滴淀粉溶液,用0.1000mol/L碘的标准溶液滴定。反应原理为 。
。
(3)滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):检漏→蒸馏水洗涤→_______ →开始滴定。
a.烘干 b.装入滴定液至零刻度以上 c.调整滴定液液面至零刻度或零刻度以下 d.用洗耳球吹出润洗液 e.排除气泡 f.用滴定液润洗滴定管2至3次 g.记录起始读数
(4)本实验滴定过程中操作滴定管的图示正确的是_______(填字母)
(5)在接近终点时,使用“半滴操作”可提高测量的准确度。其方法是:将旋塞稍稍转动,使半滴溶液悬于管口,用锥形瓶内壁将半滴溶液沾落,_______ 继续摇动锥形瓶,观察颜色变化。(请在横线上补全操作)
(6)滴定终点的判断方法:_______ 。
(7)本实验消耗碘的标准溶液20.00mL,则该样品的纯度为_______ (保留四位有效数字)。
(8)下列操作会使测得的样品纯度偏高的是_______(填字母)。
I.它在酸性条件下不稳定,可与稀硫酸发生反应:
 。现利用该反应探究外界条件对反应速率的影响。
。现利用该反应探究外界条件对反应速率的影响。| 实验编号 | 0.1mol/L Na2S2O3溶液体积/mL | 0.1mol/L H2SO4溶液体积/mL | 水的体积/mL | 温度/℃ | 出现浑浊所用时间/s |
| 1 | 4.0 | 3.0 | 1.0 | 20 |  |
| 2 | 2.0 | 3.0 | V1 | 20 |  |
| 3 | V2 | 3.0 | 3.0 | 30 |  |
(2)对比实验1、2可探究
II.硫代硫酸钠易与空气中的CO2、O2等反应而变质,现有研究性学习小组同学,测定实验室储存的Na2S2O3样品的纯度。方法如下:准确称取10.00g样品,用蒸馏水溶解并定容至250mL,准确移取该溶液25.00mL于锥形瓶中,加入2滴淀粉溶液,用0.1000mol/L碘的标准溶液滴定。反应原理为
 。
。(3)滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):检漏→蒸馏水洗涤→
a.烘干 b.装入滴定液至零刻度以上 c.调整滴定液液面至零刻度或零刻度以下 d.用洗耳球吹出润洗液 e.排除气泡 f.用滴定液润洗滴定管2至3次 g.记录起始读数
(4)本实验滴定过程中操作滴定管的图示正确的是_______(填字母)
A.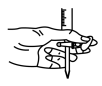 | B.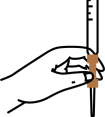 |
C.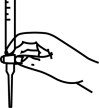 | D.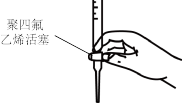 |
(6)滴定终点的判断方法:
(7)本实验消耗碘的标准溶液20.00mL,则该样品的纯度为
(8)下列操作会使测得的样品纯度偏高的是_______(填字母)。
| A.滴定前有气泡,滴定结束时气泡消失 |
| B.滴定管未用标准溶液润洗 |
| C.滴定前仰视读数,结束时俯视读数 |
| D.锥形瓶未润洗 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】亚硝酰硫酸(NOSO4H)在重氮化反应中可以代替亚硝酸钠。实验室用如图装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。

已知:i.亚硝酰硫酸是白色片状、多孔或粒状晶体,遇水分解为硫酸、硝酸和NO,溶于浓硫酸而不分解。
ii.实验室制备亚硝酰硫酸的原理为SO2+HNO3=SO3+HNO2,SO3+HNO2=NOSO4H。
回答下列问题:
(1)仪器I的名称为______ ,按照气流从左到右的顺序,上述仪器的连接顺序为_______ (填仪器接口的字母,部分仪器可以重复使用)。
(2)C装置的作用为______ 。
(3)反应需将温度控制在25~40℃,采用水浴加热的优点是_____ ,开始时反应缓慢,但某时刻反应速率明显加快,其原因可能是______ 。
(4)测定亚硝酰硫酸的纯度。
步骤①:准确称取14.00g产品,在特定条件下配制成250mL溶液。
步骤②:取25.00mL①中溶液于250mL烧瓶中,加入60.00mL未知浓度KMnO4溶液(过量)和10.00mL25%H2SO4溶液,摇匀,发生反应:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4。
步骤③:向②反应后溶液中加0.2500mol•L-1Na2C2O4标准溶液进行滴定,消耗Na2C2O4溶液20.00mL。
步骤④:把②中亚硝酰硫酸溶液换为蒸馏水(空白实验),重复上述步骤,消耗Na2C2O4溶液的体积为60.00mL。滴定终点时的现象为______ ,亚硝酰硫酸的纯度为______ %(精确到0.1)。

已知:i.亚硝酰硫酸是白色片状、多孔或粒状晶体,遇水分解为硫酸、硝酸和NO,溶于浓硫酸而不分解。
ii.实验室制备亚硝酰硫酸的原理为SO2+HNO3=SO3+HNO2,SO3+HNO2=NOSO4H。
回答下列问题:
(1)仪器I的名称为
(2)C装置的作用为
(3)反应需将温度控制在25~40℃,采用水浴加热的优点是
(4)测定亚硝酰硫酸的纯度。
步骤①:准确称取14.00g产品,在特定条件下配制成250mL溶液。
步骤②:取25.00mL①中溶液于250mL烧瓶中,加入60.00mL未知浓度KMnO4溶液(过量)和10.00mL25%H2SO4溶液,摇匀,发生反应:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4。
步骤③:向②反应后溶液中加0.2500mol•L-1Na2C2O4标准溶液进行滴定,消耗Na2C2O4溶液20.00mL。
步骤④:把②中亚硝酰硫酸溶液换为蒸馏水(空白实验),重复上述步骤,消耗Na2C2O4溶液的体积为60.00mL。滴定终点时的现象为
您最近一年使用:0次

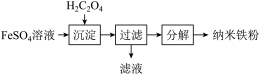
 。写出沉淀反应的离子方程式为
。写出沉淀反应的离子方程式为 时分解:
时分解: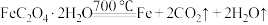 。由于生成
。由于生成 :酸性条件下,纳米铁粉与废水中
:酸性条件下,纳米铁粉与废水中 与
与 ,其反应的离子方程式是
,其反应的离子方程式是

