 是阿伏加德罗常数的值。下列说法正确的是
是阿伏加德罗常数的值。下列说法正确的是A.120g 和 和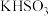 的固体混合物中含有的阳离子数为 的固体混合物中含有的阳离子数为 |
B.1L NaCl溶液含有 NaCl溶液含有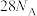 个电子 个电子 |
C.常温下, 的 的 溶液中,水电离出的 溶液中,水电离出的 数为 数为 |
D.1L 的 的 溶液中,阴离子数等于 溶液中,阴离子数等于 |
更新时间:2023-01-13 16:44:37
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】在100mL 0.1 mol·L-1 HA的溶液中,c(H+)=0.05mol·L-1,往该溶液中加入等体积等浓度的NaOH溶液(忽略溶液混合体积变化),下列离子浓度关系正确的是
| A.c(Na+)> c(A-)> c(H+)> c(OH-) |
| B.c(A-)+ c(HA)="0.05" mol·L-1 |
| C.c(Na+)> c(A-)> c(HA)>c(OH-) |
| D.c(HA)+ c(H+)= c(A-)+ c(OH-) |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下,通过下列实验探究 溶液的性质。下列有关说法正确的是
溶液的性质。下列有关说法正确的是
 溶液的性质。下列有关说法正确的是
溶液的性质。下列有关说法正确的是| 实验 | 实验操作和现象 |
| 1 | 用pH计测定0.05mol/L  溶液的pH,测得pH约为6.4 溶液的pH,测得pH约为6.4 |
| 2 | 向0.05 mol/L  溶液中滴加过量0.1 mol/L 溶液中滴加过量0.1 mol/L  溶液,产生白色沉淀 溶液,产生白色沉淀 |
| 3 | 向10mL 0.05 mol/L  溶液中滴加10mL 0.05 mol/L盐酸,反应结束,测得pH约为3.2 溶液中滴加10mL 0.05 mol/L盐酸,反应结束,测得pH约为3.2 |
| 4 | 向10mL 0.05 mol/L  溶液中滴加l0 mL 0.05 mol/L NaOH溶液,反应结束,测得pH约为9.3 溶液中滴加l0 mL 0.05 mol/L NaOH溶液,反应结束,测得pH约为9.3 |
A.实验1中: 溶液中 溶液中 的水解程度大于电离程度 的水解程度大于电离程度 |
B.实验2反应静置后的上层清液中: |
C.实验3滴加过程中: |
D.实验4滴加过程中: 逐渐减小 逐渐减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】25℃时,下列说法不正确的是
| A.0.10mol·L-1、0.010mol·L-1的醋酸溶液的电离度分别为a1、a2,则a1<a2 |
| B.pH相等的盐酸、CH3COOH溶液,c(Cl—)=c(CH3COO—) |
| C.1LpH=7的CH3COONH4溶液中水电离出H+的物质的量为1.0×10-7mol |
| D.中和pH和体积均相等的醋酸、盐酸溶液,所需NaOH的物质的量前者多 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】短周期主族元素W、X、Y、Z的原子序数依次增大,W是短周期中非金属性最强的元素,X是所在周期中原子半径最大的元素,Y的最外层电子数是最内层电子数的3倍,下列说法正确的是
| A.简单离子半径:Y>Z>W>X |
| B.简单氢化物稳定性:Y>Z>W |
| C.X与氧元素形成的化合物中阴阳离子个数比均为2:1 |
| D.X和Y两种元素形成的化合物水溶液呈中性 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】NA为阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,11.2LH2O2含有的非极性共价键数目为0.5NA |
| B.在1L0.1mol∙L-1CH3COONa溶液中,阴离子的总数等于0.1NA |
| C.5.6gFe与足量的S反应转移的电子数为0.2NA |
| D.1molHOOCCH2COOH与足量乙醇在一定条件下反应,生成的酯基的数目为2NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
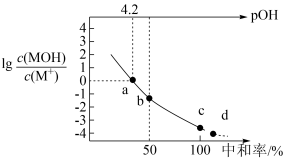
【推荐1】常温下,向 某一元碱
某一元碱 溶液中逐滴加入
溶液中逐滴加入 的
的 溶液,溶液中
溶液,溶液中 、
、 、中和率的变化如图所示。
、中和率的变化如图所示。 为
为 的电离常数,
的电离常数,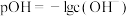 ,中和率
,中和率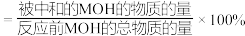 。下列说法正确的是
。下列说法正确的是
 某一元碱
某一元碱 溶液中逐滴加入
溶液中逐滴加入 的
的 溶液,溶液中
溶液,溶液中 、
、 、中和率的变化如图所示。
、中和率的变化如图所示。 为
为 的电离常数,
的电离常数,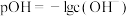 ,中和率
,中和率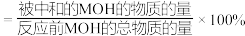 。下列说法正确的是
。下列说法正确的是
| A.根据a点数据计算,常温下MOH的电离平衡常数的数量级为10-4 |
| B.溶液中水的电离程度从a点到d点逐渐增大 |
C.b点时, |
D.c点溶液中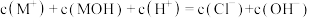 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,二元弱酸H2Y溶液中滴加KOH溶液,所得混合溶液的pH与离子浓度变化的关系如图所示,下列有关说法不正确的是
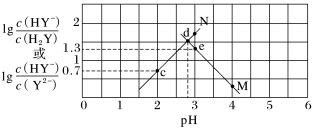
A.曲线M表示pH与lg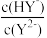 的变化关系 的变化关系 |
| B.NaHY溶液显酸性 |
| C.交点d对应的pH=2.8 |
| D.e点溶液中:c(HY-)>c(H2Y)>c(Y2-)>c(H+)>c(OH-) |
您最近半年使用:0次




