下列实验操作、现象和解释结论都正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 室温下,用 试纸分别测定浓度为 试纸分别测定浓度为 溶液和 溶液和 溶液的 溶液的 | 前者 大于后者 大于后者 |  的酸性小于 的酸性小于 |
| B | 向浓度均为 的 的 和 和 的混合溶液中滴加少量 的混合溶液中滴加少量 的 的 溶液 溶液 | 产生黄色沉淀 |  |
| C | 向2支盛有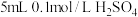 溶液的试管中分别加入 溶液的试管中分别加入 溶液,分别放入20℃和40℃的水浴中,并开始计时 溶液,分别放入20℃和40℃的水浴中,并开始计时 | 40℃下出现浑浊的时间短 | 温度越高反应速率越快 |
| D | 在两个烧杯中分别盛有等体积、等浓度的烧碱溶液和氨水,插入电极,连接灯泡,接通电源,分别进行导电实验 | 盛有烧碱溶液的灯泡亮度大 | 强电解质导电能力大于弱电解质 |
| A.A | B.B | C.C | D.D |
更新时间:2023-02-02 16:34:11
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】把0.05mol的NaOH固体分别加入到100 mL下列溶液中,溶液的导电能力变化不大 的是( )
| A.自来水 | B.0.5mol/L盐酸 | C.0.5mol/L醋酸 | D.0.5mol/L NH4Cl溶液 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】在一定温度下,冰醋酸稀释过程中溶液的导电能力变化如图所示,下列判断正确的是


| A.加水前导电能力约为零 |
B.A、B、C三点对应的溶液中, 由小到大的顺序是A>B>C 由小到大的顺序是A>B>C |
C.A、B、C三点对应的溶液中, 电离程度最大的B 电离程度最大的B |
D.若使B点对应的溶液中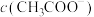 增大、 增大、 增大,可行的方法是加热溶液 增大,可行的方法是加热溶液 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
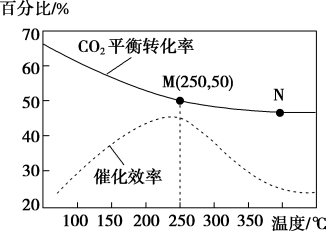
【推荐1】一定条件下合成乙烯:6H2(g)+2CO2(g)  CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是
CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是
 CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是
CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是
| A.平衡常数:KN>KM |
| B.该反应的逆反应为吸热反应 |
| C.生成乙烯的速率:v(N)一定大于v(M) |
| D.当温度高于250 ℃,升高温度,催化剂的催化效率降低 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】在一定温度下,以 为催化剂,氯苯和
为催化剂,氯苯和 在
在 中发生平行反应,生成邻二氯苯和对二氯苯,其反应式为:反应①
中发生平行反应,生成邻二氯苯和对二氯苯,其反应式为:反应①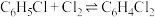 (邻二氯苯)
(邻二氯苯)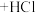

反应②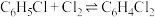 (对二氯苯)
(对二氯苯)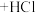

反应①和②的速率方程式分别为:① ;②
;② ,
, 为速率常数且只与温度有关。图为反应①和②的
为速率常数且只与温度有关。图为反应①和②的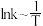 曲线。下列说法错误的是
曲线。下列说法错误的是

 为催化剂,氯苯和
为催化剂,氯苯和 在
在 中发生平行反应,生成邻二氯苯和对二氯苯,其反应式为:反应①
中发生平行反应,生成邻二氯苯和对二氯苯,其反应式为:反应①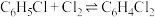 (邻二氯苯)
(邻二氯苯)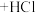

反应②
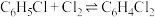 (对二氯苯)
(对二氯苯)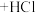

反应①和②的速率方程式分别为:①
 ;②
;② ,
, 为速率常数且只与温度有关。图为反应①和②的
为速率常数且只与温度有关。图为反应①和②的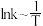 曲线。下列说法错误的是
曲线。下列说法错误的是
A.对二氯苯比邻二氯苯稳定,则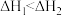 |
| B.相同温度下,平衡后,体系中两种有机产物的浓度之比保持不变 |
| C.提高产物中对二氯苯的比例,适当降低反应温度和改变催化剂 |
D. (对二氯苯) (对二氯苯) (邻二氯苯) (邻二氯苯) |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】298K,发生反应H2O2+2HI=I2+2H2O,反应速率与浓度关系式为v=k c(HI) m·c(H2O2)n,k为速率常数,实验测定数据如下:
下列说法错误的是
| 实验编号 | 1 | 2 | 3 | 4 | 5 |
| c(HI)/mol·L﹣1 | 0.100 | 0.200 | 0.300 | 0.100 | 0.100 |
| c(H2O2)/mol·L﹣1 | 0.100 | 0.100 | 0.100 | 0.200 | 0.300 |
| 溶液出现棕黄色的时间t/s | 13 | 6.5 | t1 | 6.5 | t2 |
| v/mol·L﹣1·s﹣1 | 0.0076 | 0.0153 | v1 | 0.0151 | v2 |
| A.m=1,n=1 |
| B.反应速率常数k只与温度有关 |
| C.v1=v2,由表中数据可得出结论,该反应只要增大反应物浓度,化学反应速率加快 |
| D.化学反应速率与反应物浓度的关系与化学方程式系数有定量关系 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】下列选项中的实验操作、现象与结论完全一致的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用玻璃棒蘸取次氯酸钠溶液,点在pH试纸上 | 试纸最终显蓝色 | 次氯酸钠溶液显碱性 |
| B | 用pH试纸分别测定0.1 mol·L-1的Na2CO3溶液和0.1 mol·L-1的NaHCO3溶液的pH | Na2CO3溶液的pH约为10,NaHCO3 溶液的pH约为8 | 结合H+能力:CO >HCO >HCO |
| C | 用坩埚钳夹住一小块用砂纸打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点低 |
| D | 将NaAlO2溶液加入NaHCO3溶液中 | 有白色沉淀生成 | A1O 结合H+能力比CO 结合H+能力比CO 强 强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】已知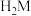 是二元弱酸其电离常数
是二元弱酸其电离常数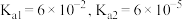 ,CaM为难溶物,其
,CaM为难溶物,其 ,现进行两组实验:
,现进行两组实验:
实验1:往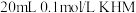 溶液中滴加
溶液中滴加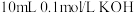 溶液。
溶液。
实验Ⅱ:往 溶液中滴加
溶液中滴加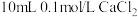 溶液。
溶液。
[溶液混合后的体积变化忽略不计],下列说法正确的是
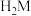 是二元弱酸其电离常数
是二元弱酸其电离常数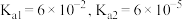 ,CaM为难溶物,其
,CaM为难溶物,其 ,现进行两组实验:
,现进行两组实验:实验1:往
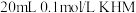 溶液中滴加
溶液中滴加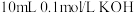 溶液。
溶液。实验Ⅱ:往
 溶液中滴加
溶液中滴加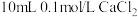 溶液。
溶液。[溶液混合后的体积变化忽略不计],下列说法正确的是
| A.实验1可选用甲基橙作指示剂,指示反应终点 |
B.实验I中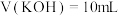 时,存在 时,存在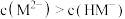 |
| C.实验II中无CaM沉淀生成 |
D.若实验II中将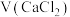 改为 改为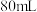 ,则溶液中 ,则溶液中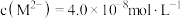 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列实验操作、现象与结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向盛有2mL0.5mol/LNaOH溶液中先滴加2滴0.1mol/LMgCl2溶液,再滴加2滴0.1mol/LFeCl3溶液 | 先出现白色沉淀,后沉淀变为红褐色 | 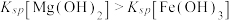 |
| B | 向盛有少量Mg(OH)2沉淀的试管中加入适量饱和CH3COONH4溶液,振荡 | 白色沉淀溶解 |  结合了OH-,促使Mg(OH)2溶解平衡正移 结合了OH-,促使Mg(OH)2溶解平衡正移 |
| C | 用玻璃棒蘸取NaHCO3溶液点在pH试纸上 | 试纸变红 |  的电离程度大于水解程度 的电离程度大于水解程度 |
| D | 比较电负性:室温下,用pH计测定0.1mol·L-1的CF3COOH、CCl3COOH两种溶液的pH | CF3COOH溶液的pH较小 | F元素的电负性大于Cl元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】下列实验方案设计、现象和结论都正确的是
| 编号 | 目的 | 方案设计 | 现象和结论 |
| A | 探究NaClO 溶液的酸碱性 | 把NaClO溶液滴到pH试纸上 | pH=10,则NaClO溶液水解显碱性 |
| B | 验证牺牲阳极的阴极保护法 | 往铁电极区滴加铁氰化钾溶液 | 未出现特征蓝色的沉淀,说明锌、铁与酸化的氯化钠溶液构成原电池后,锌能够有效保护铁制品 |
| C | 探究反应速率与温度的关系 | 向2支盛有5mL0.1mol•L-1H2SO4溶液的试管中分别加入5mL0.1mol•L-1Na2S2O3溶液,分别放入20℃、40℃的水浴中,并开始计时 | 若40℃下出现浑浊的时间短,则温度越高反应速率越快 |
| D | 探究AgCl和AgI的溶度积大小 | 向2支盛有2mL相同浓度硝酸银溶液的试管中分别加入相同滴数同浓度的NaCl和NaI溶液 | 一支试管中产生黄色沉淀,一支试管中无明显现象,说明 Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】常温下,CaSO4、CaCO3、MnCO3三种物质的pM与pR的关系如图所示,已知:pM为阳离子浓度的负对数,pR为阴离子浓度的负对数;离子浓度≤10-5mol·L-1时认为其沉淀完全。下列说法错误的是
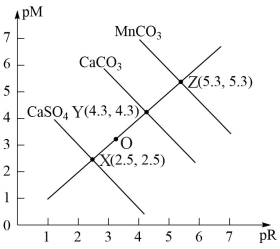

| A.常温下,溶度积:CaSO4>CaCO3>MnCO3 |
| B.O点对应CaCO3的不饱和溶液 |
C.常温下,向物质的量浓度均为0.5mol·L-1Na2SO4和Na2CO3的混合溶液中逐滴加入CaC12溶液,当CO 恰好完全沉淀时,溶液中c(SO 恰好完全沉淀时,溶液中c(SO )=10-1.4mol·L-1 )=10-1.4mol·L-1 |
D.常温时,CaCO3(s)+Mn2+(aq) MnCO3(s)+Ca2+(aq)的平衡常数K=0.01 MnCO3(s)+Ca2+(aq)的平衡常数K=0.01 |
您最近一年使用:0次


 和
和 溶液的pH
溶液的pH NaCN溶液和
NaCN溶液和 溶液pH
溶液pH
 、
、 的混合溶液
的混合溶液

