 是一种易溶有机碱,与足量盐酸反应生成MCl。常温下,将
是一种易溶有机碱,与足量盐酸反应生成MCl。常温下,将

 稀释体积为
稀释体积为 ,
,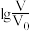 与pH的关系如图所示。下列说法正确的是
与pH的关系如图所示。下列说法正确的是
A.将1mL1mol/L的MOH溶液稀释至 ,溶液 ,溶液 |
B.MOH是弱碱,电离常数 |
C.MOH溶液稀释过程中, 和 和 均逐渐增大 均逐渐增大 |
D.MCl溶液中存在 |
更新时间:2023-02-13 14:44:14
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在室温下,将pH=3的酸和pH=11的碱等体积混合,混合后溶液的pH>7,则该酸和碱的组合可以是
| A.醋酸和氢氧化钾 | B.硝酸和氢氧化钠 |
| C.硫酸和氢氧化钡 | D.盐酸和氨水 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,在 某一元碱
某一元碱 的溶液中滴加
的溶液中滴加 的盐酸,其中pH水(水电离出的
的盐酸,其中pH水(水电离出的 浓度的负对数)与加入盐酸体积的变化曲线如图所示。下列说法中正确的是(已知
浓度的负对数)与加入盐酸体积的变化曲线如图所示。下列说法中正确的是(已知 )
)

 某一元碱
某一元碱 的溶液中滴加
的溶液中滴加 的盐酸,其中pH水(水电离出的
的盐酸,其中pH水(水电离出的 浓度的负对数)与加入盐酸体积的变化曲线如图所示。下列说法中正确的是(已知
浓度的负对数)与加入盐酸体积的变化曲线如图所示。下列说法中正确的是(已知 )
)
A.一元碱 为弱碱,原溶液的浓度大于 为弱碱,原溶液的浓度大于 |
B.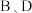 点溶液的 点溶液的 均是7 均是7 |
C.C点溶液中存在 |
D.E点溶液的 近似为1.3 近似为1.3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】25°C时,下列说法正确的是
A.向0.1mol/LCH3COOH溶液中加入少量水,溶液中 减小 减小 |
B.向盐酸中加入氨水至中性,溶液中 >l >l |
| C.pH为2的盐酸与等体积pH=l2的氨水混合后所得溶液呈酸性 |
D.Na2SO3溶液中:c(Na+)=2[c( )+c( )+c( )+c(H2SO3)] )+c(H2SO3)] |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】缓冲溶液可以抗御少量酸碱对溶液pH的影响。人体血液里存在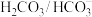 缓冲体系,可使血液的pH稳定在7.4左右,当血液pH低于7.2或高于7.5时,会发生酸中毒或碱中毒。
缓冲体系,可使血液的pH稳定在7.4左右,当血液pH低于7.2或高于7.5时,会发生酸中毒或碱中毒。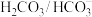 缓冲体系的缓冲作用可用下列平衡表示:
缓冲体系的缓冲作用可用下列平衡表示: ,已知
,已知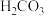 的
的 ,
, 。下列说法正确的是
。下列说法正确的是
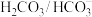 缓冲体系,可使血液的pH稳定在7.4左右,当血液pH低于7.2或高于7.5时,会发生酸中毒或碱中毒。
缓冲体系,可使血液的pH稳定在7.4左右,当血液pH低于7.2或高于7.5时,会发生酸中毒或碱中毒。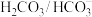 缓冲体系的缓冲作用可用下列平衡表示:
缓冲体系的缓冲作用可用下列平衡表示: ,已知
,已知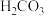 的
的 ,
, 。下列说法正确的是
。下列说法正确的是A.人体发生碱中毒时注射 溶液可以缓解症状 溶液可以缓解症状 |
B.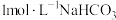 溶液中 溶液中 的个数约为 的个数约为 |
C. 的血液中, 的血液中, |
D.人体血液中的 在血液酸碱平衡中起着主要的缓冲调节作用 在血液酸碱平衡中起着主要的缓冲调节作用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】常温下,分别取未知浓度的MOH和HA溶液,加水稀释至原体积的n倍。稀释过程中,两溶液pH的变化如图所示。下列叙述正确的是


| A.MOH为弱碱,HA为强酸 |
| B.水的电离程度:X=Z>Y |
| C.若升高温度,Y、Z点对应溶液的pH均不变 |
| D.将X点溶液与Z点溶液等体积混合,所得溶液呈中性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述错误的是
A.向 的 的 溶液中加入少量 溶液中加入少量 固体,溶液的pH会减小 固体,溶液的pH会减小 |
B.在 的 的 ,溶液中一定存在: ,溶液中一定存在: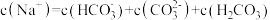 |
C.把 的 的 溶液与 溶液与 的KOH溶液混合,所得溶液中一定存在: 的KOH溶液混合,所得溶液中一定存在: |
D.常温下,在 的稀盐酸和 的稀盐酸和 的 的 溶液等体积混合后,溶液显碱性 溶液等体积混合后,溶液显碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下,通过下列实验探究NaHSO3溶液的性质。
实验1:用pH试纸测定0.1 mol/L NaHSO3溶液的pH,测得pH约为5
实验2:向0.1 mol/L NaHSO3,溶液中滴加稀盐酸至pH=3
实验3:向0.1 mol/L NaHSO3溶液滴加NaOH溶液至pH=7
实验4:向0.1 mol/L NaHSO3溶液中滴加HNO3酸化的Ba(NO3)2溶液,产生白色沉淀
下列有关说法正确的是
实验1:用pH试纸测定0.1 mol/L NaHSO3溶液的pH,测得pH约为5
实验2:向0.1 mol/L NaHSO3,溶液中滴加稀盐酸至pH=3
实验3:向0.1 mol/L NaHSO3溶液滴加NaOH溶液至pH=7
实验4:向0.1 mol/L NaHSO3溶液中滴加HNO3酸化的Ba(NO3)2溶液,产生白色沉淀
下列有关说法正确的是
A.由实验1可以得出: |
B.实验2中,滴加稀盐酸时反应的离子方程式为: |
C.实验3所得pH=7的溶液中存在: |
D.实验4反应后静置所得上层清液中一定有: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】室温下,通过下列实验探究NaHS溶液的性质:
下列有关说法正确的是
| 实验 | 实验操作和现象 |
| 1 | 测定0.1mol·L-1NaHS溶液的pH值,其pH值大于7 |
| 2 | 向0.1mol·L-1NaHS溶液中滴加少量CuCl2溶液,产生黑色沉淀 |
| 3 | 向0.1mol·L-1NaHS溶液中加入等体积0.1mol·L-1NaHCO3溶液充分混合,无气泡产生 |
| 4 | 向0.1mol·L-1NaHS溶液中通入一定量Cl2,溶液变浑浊 |
| A.实验1可知0.1mol·L-1溶液中:c(H+)·c(S2-)>c(H2S)·c(OH-) |
| B.实验2说明Ka(HS-)>Ksp(CuS) |
C.实验3所得溶液中:c(S2-)+c(HS-)+c(H2S)>c(CO )+c(HCO )+c(HCO )+c(H2CO3) )+c(H2CO3) |
| D.实验4在Cl2通入过程中,水的电离程度先增大后减小 |
您最近一年使用:0次



