氮及其化合物在工农业生产和生命活动中起着重要的作用。同时,氮氧化物(NOx)是常见的大气污染物,能引起雾霾、光化学烟雾、酸雨等环境问题。因此,研究氮氧化物(NOx)的无害化处理对治理大气污染、建设生态文明具有重要意义。请按要求回答下列问题:
(1)“中国制造2025”是中国政府实施制造强国战略第一个十年行动纲领。氮化铬在现代工业中发挥着重要的作用。基态铬、氮原子的未成对电子数之比为__________ 。
(2)联氨(又称肼,N2H4,无色液体)也是氮的一种重要的化合物,是一种应用广泛的化工原料,可用作火箭燃料。联氨为二元弱碱,在水中的电离方程式与氨相似,联氨的第一步电离方程式为___________ 。
(3)研究氮氧化物(NOx)的无害化处理
I.CO还原NO2的反应原理如下:
已知:①NO2(g)+CO(g) CO2(g)+NO(g) ΔH1= -234kJ·mol-1
CO2(g)+NO(g) ΔH1= -234kJ·mol-1
②N2(g)+O2(g) 2NO(g) ΔH2= +179.5 kJ·mol-1
2NO(g) ΔH2= +179.5 kJ·mol-1
③2NO(g)+O2(g) 2NO2(g) ΔH3=-112.3 kJ·mol-1
2NO2(g) ΔH3=-112.3 kJ·mol-1
NO2与CO反应生成无污染气体的热化学方程式为__________________________ 。
II.用H2还原NO的反应为2H2(g) + 2NO(g) N2(g) + 2H2O(g) ΔH =-752 kJ·mol-1。为研究H2和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为aL的刚性密闭容器中加入一定量H2和NO发生反应,实验结果如图:
N2(g) + 2H2O(g) ΔH =-752 kJ·mol-1。为研究H2和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为aL的刚性密闭容器中加入一定量H2和NO发生反应,实验结果如图:
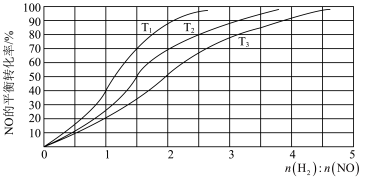
①反应温度T1、T2、T3从高到低的关系为______________________ ;
②T1温度下,充入H2、NO分别为3mol、3mol, 容器内的压强为w Pa,反应进行到10min时达平衡,0~ 10min内N2的平均反应速率为_____________ mol·L-1·s-1,该反应的平衡常数Kp=___________ (写出计算表达式,以分压表示的平衡常数为Kp,某气体分压=总压 ×某气体物质的量分数);
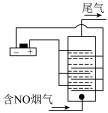
III.以铂为电极,饱和食盐水作电解液,对含有NO的烟气进行脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为 ,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的原理为
,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的原理为___________________________ (用电极反应和离子方程式表示)
(1)“中国制造2025”是中国政府实施制造强国战略第一个十年行动纲领。氮化铬在现代工业中发挥着重要的作用。基态铬、氮原子的未成对电子数之比为
(2)联氨(又称肼,N2H4,无色液体)也是氮的一种重要的化合物,是一种应用广泛的化工原料,可用作火箭燃料。联氨为二元弱碱,在水中的电离方程式与氨相似,联氨的第一步电离方程式为
(3)研究氮氧化物(NOx)的无害化处理
I.CO还原NO2的反应原理如下:
已知:①NO2(g)+CO(g)
 CO2(g)+NO(g) ΔH1= -234kJ·mol-1
CO2(g)+NO(g) ΔH1= -234kJ·mol-1②N2(g)+O2(g)
 2NO(g) ΔH2= +179.5 kJ·mol-1
2NO(g) ΔH2= +179.5 kJ·mol-1③2NO(g)+O2(g)
 2NO2(g) ΔH3=-112.3 kJ·mol-1
2NO2(g) ΔH3=-112.3 kJ·mol-1NO2与CO反应生成无污染气体的热化学方程式为
II.用H2还原NO的反应为2H2(g) + 2NO(g)
 N2(g) + 2H2O(g) ΔH =-752 kJ·mol-1。为研究H2和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为aL的刚性密闭容器中加入一定量H2和NO发生反应,实验结果如图:
N2(g) + 2H2O(g) ΔH =-752 kJ·mol-1。为研究H2和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为aL的刚性密闭容器中加入一定量H2和NO发生反应,实验结果如图: 
①反应温度T1、T2、T3从高到低的关系为
②T1温度下,充入H2、NO分别为3mol、3mol, 容器内的压强为w Pa,反应进行到10min时达平衡,0~ 10min内N2的平均反应速率为
III.以铂为电极,饱和食盐水作电解液,对含有NO的烟气进行脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为
 ,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的原理为
,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的原理为
2023·云南曲靖·一模 查看更多[2]
更新时间:2023-03-09 16:34:12
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】煤和天然气都是重要的化石资源,在工业生产中用途广泛。
(1)燃煤时往往在煤中添加石灰石,目的是_____ ,达到该目的时发生反应的化学方程式为_____ 。
(2)煤的综合利用包括____ (将煤隔绝空气加强热)、煤的气化和液化。煤的气化是将其转化为可燃性气体的过程,主要发生的反应的化学方程式为____ 。
(3)CO是煤气的主要成分,可与水蒸气反应生成氢气:CO(g)+ H2O(g)⇌CO2(g)+H2(g) △H。 查阅资料得出相关数据如下:
①该反应升高到一定温度时,反应将不能正向进行,由此判断该反应的△S_____ (填“>”或“<”")0。
②在容积为10 L的密闭容器中通入0.1 mol CO(g)和0.1 mol H2O(g)发生反应,在400℃时反应达到平衡,此时CO(g)的转化率为__ 。
(4)将2 mol CH4和4 mol H2O(g)通入容积为10 L的恒容密闭容器中,发生反应:CH4(g)+ H2O(g)⇌CO(g)+ 3H2(g)。CH4的平衡转化率与温度、压强的变化关系如图所示。

①200 °C时,该反应的平衡常数K=______ 。
②A、B、C三点的平衡常数KA、KB、KC的大小关系是________ 。
③压强:p1_____ (填“>”“<”或“=”)p2。
(1)燃煤时往往在煤中添加石灰石,目的是
(2)煤的综合利用包括
(3)CO是煤气的主要成分,可与水蒸气反应生成氢气:CO(g)+ H2O(g)⇌CO2(g)+H2(g) △H。 查阅资料得出相关数据如下:
温度/°C | 400 | 500 |
平衡常数K | 9 | 5.3 |
②在容积为10 L的密闭容器中通入0.1 mol CO(g)和0.1 mol H2O(g)发生反应,在400℃时反应达到平衡,此时CO(g)的转化率为
(4)将2 mol CH4和4 mol H2O(g)通入容积为10 L的恒容密闭容器中,发生反应:CH4(g)+ H2O(g)⇌CO(g)+ 3H2(g)。CH4的平衡转化率与温度、压强的变化关系如图所示。

①200 °C时,该反应的平衡常数K=
②A、B、C三点的平衡常数KA、KB、KC的大小关系是
③压强:p1
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】将二氧化碳加氢转化为高附加值的化学品或液体燃料是二氧化碳资源化利用的有效方法,其中转换为甲醇被认为是最可能的利用路径,主要涉及反应如下:
反应I: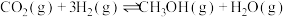
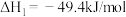
反应II:
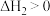
请回答下列问题:
(1)已知 的燃烧热
的燃烧热 和CO的燃烧热
和CO的燃烧热 ,水的汽化热(1mol
,水的汽化热(1mol 从液体汽化为气体所需要吸收的热量)为40.8kJ/mol,则反应II的
从液体汽化为气体所需要吸收的热量)为40.8kJ/mol,则反应II的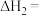
_______ 。
(2) 和
和 在某NiO支撑的
在某NiO支撑的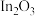 表面的反应历程如下图所示。(TS表示过渡态)
表面的反应历程如下图所示。(TS表示过渡态)
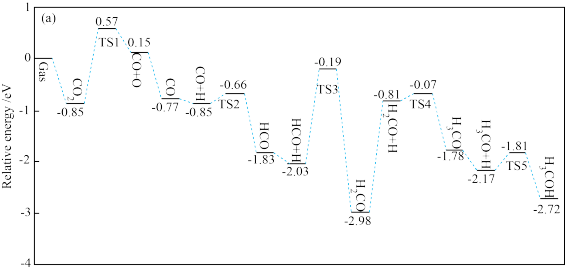
决定总反应速率的步骤的反应方程式为_______ ,该步骤的活化能
_______ eV。
(3)恒定压强P下,体积比1:3的 和
和 发生反应I、反应II,反应相同时间,测得不同温度下
发生反应I、反应II,反应相同时间,测得不同温度下 的转化率和
的转化率和 的选择性如下图中实验值所示。图中平衡值表示相同条件下平衡状态
的选择性如下图中实验值所示。图中平衡值表示相同条件下平衡状态 的转化率和
的转化率和 的选择性随温度的变化[
的选择性随温度的变化[ 的选择性
的选择性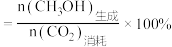 ]
]
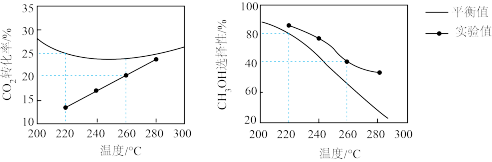
①当温度高于260℃时,二氧化碳的平衡转化率随温度升高而增大的原因是_______ 。
②260℃时,甲醇产率的实验值是_______ 。220℃-260℃甲醇的选择性随温度升高降低的原因是_______ 。
③220℃时,反应II的化学平衡常数
_______ 。
反应I:
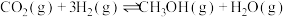
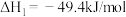
反应II:

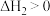
请回答下列问题:
(1)已知
 的燃烧热
的燃烧热 和CO的燃烧热
和CO的燃烧热 ,水的汽化热(1mol
,水的汽化热(1mol 从液体汽化为气体所需要吸收的热量)为40.8kJ/mol,则反应II的
从液体汽化为气体所需要吸收的热量)为40.8kJ/mol,则反应II的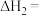
(2)
 和
和 在某NiO支撑的
在某NiO支撑的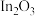 表面的反应历程如下图所示。(TS表示过渡态)
表面的反应历程如下图所示。(TS表示过渡态)
决定总反应速率的步骤的反应方程式为

(3)恒定压强P下,体积比1:3的
 和
和 发生反应I、反应II,反应相同时间,测得不同温度下
发生反应I、反应II,反应相同时间,测得不同温度下 的转化率和
的转化率和 的选择性如下图中实验值所示。图中平衡值表示相同条件下平衡状态
的选择性如下图中实验值所示。图中平衡值表示相同条件下平衡状态 的转化率和
的转化率和 的选择性随温度的变化[
的选择性随温度的变化[ 的选择性
的选择性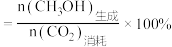 ]
]
①当温度高于260℃时,二氧化碳的平衡转化率随温度升高而增大的原因是
②260℃时,甲醇产率的实验值是
③220℃时,反应II的化学平衡常数

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】用钒钛磁铁为原料冶炼铁,产生一种固体废料,主要成分如下表。
通过下列工艺流程可以实现元素Ti、Al、 Si的回收利用,并得到纳米二氧化钛和分子筛。

请回答下列问题:
(1)步骤①②③中进行分离操作的名称是_____________________ 。
(2)下列固体废料的成分中,不属于碱性氧化物的是___________________ (填字母序号)。
a.TiO2 b.MgO c.SiO2 d.CaO
(3)熔融温度和钛的提取率关系如下图,适宜温度为500℃,理由__________________ 。
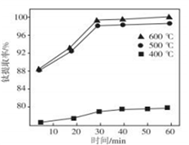
(4)滤液①中溶质的成分是_______________________ 。
(5)步骤②中发生反应的离子方程式是___________________________ 。
(6)将步骤③中制取分子筛的化学方程式补充完整:_______
□____+6Na2SiO3+8H2O=Na8Al6Si6O24(OH)2·2H2O+□
根据成分表中数据,计算10kg固体废料,理论上应再加入Na2SiO3物质的量的计算式是n(Na2SiO3)=______ mol (摩尔质量/g/mol:SiO2 60 Al2O3 102)。
| 物质 | TiO2 | MgO | SiO2 | CaO | Al2O3 |
| 质量百分含量/% | 51.00 | 12.52 | 5.39 | 4.00 | 19.34 |
通过下列工艺流程可以实现元素Ti、Al、 Si的回收利用,并得到纳米二氧化钛和分子筛。

请回答下列问题:
(1)步骤①②③中进行分离操作的名称是
(2)下列固体废料的成分中,不属于碱性氧化物的是
a.TiO2 b.MgO c.SiO2 d.CaO
(3)熔融温度和钛的提取率关系如下图,适宜温度为500℃,理由

(4)滤液①中溶质的成分是
(5)步骤②中发生反应的离子方程式是
(6)将步骤③中制取分子筛的化学方程式补充完整:
□____+6Na2SiO3+8H2O=Na8Al6Si6O24(OH)2·2H2O+□
根据成分表中数据,计算10kg固体废料,理论上应再加入Na2SiO3物质的量的计算式是n(Na2SiO3)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】CO2的绿色减排、捕捉、转化是人类可持续发展的重要战略之一。
(1)CO2来源之一是汽车尾气
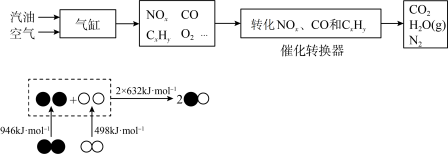
①根据上图,写出气缸内产生NO的热化学方程式________ 。
②写出转换器中在催化剂作用下NOx和CO反应的化学方程式________ 。
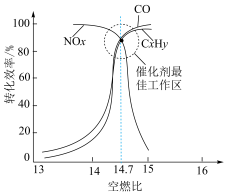
③在催化转换器中机动车尾气转化效率与空燃比(空气与燃油气的体积比)的关系如右图。若空燃比小于14.7,氧气不足,CxHy和CO不能被完全氧化,导致其转化效率降低;若空燃比大于14.7,则NOx的转化效率降低,原因是________ 。
(2)利用NaOH溶液可以“捕捉” CO2
已知:0.448L CO2(已折算标准状况)被NaOH溶液充分吸收,得到100mL含有Na2CO3和NaHCO3的吸收液。
①向吸收液中加入足量BaCl2溶液得到沉淀,经过滤、洗涤、干燥后,称重为1.97g,则吸收液中c(Na2CO3) =________ 。(该条件下NaHCO3与BaCl2不反应)
②对该吸收液,下列判断正确的是________ 。
a . c (CO32- ) > c (HCO3- )
b. 2c (CO32- ) + c (HCO3- ) + c (OH- ) = c (H+ ) + c (Na+ )
c. c (H2CO3) + c (HCO3- ) + c (CO32- ) =0.2mol•L-1
(3)工业上可用CO2来制甲醇
①CO2 (g) + 3H2(g)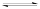 CH3OH(g) + H2O(g) ΔH < 0
CH3OH(g) + H2O(g) ΔH < 0
根据图1分析,实际工业生产中,反应温度选择250℃的理由________ 。
②利用光电催化原理,由CO2和H2O制备CH3OH的装置如图2。写出右侧的电极反应式________ 。
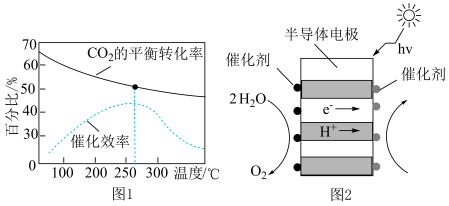
(1)CO2来源之一是汽车尾气

①根据上图,写出气缸内产生NO的热化学方程式
②写出转换器中在催化剂作用下NOx和CO反应的化学方程式

③在催化转换器中机动车尾气转化效率与空燃比(空气与燃油气的体积比)的关系如右图。若空燃比小于14.7,氧气不足,CxHy和CO不能被完全氧化,导致其转化效率降低;若空燃比大于14.7,则NOx的转化效率降低,原因是
(2)利用NaOH溶液可以“捕捉” CO2
已知:0.448L CO2(已折算标准状况)被NaOH溶液充分吸收,得到100mL含有Na2CO3和NaHCO3的吸收液。
①向吸收液中加入足量BaCl2溶液得到沉淀,经过滤、洗涤、干燥后,称重为1.97g,则吸收液中c(Na2CO3) =
②对该吸收液,下列判断正确的是
a . c (CO32- ) > c (HCO3- )
b. 2c (CO32- ) + c (HCO3- ) + c (OH- ) = c (H+ ) + c (Na+ )
c. c (H2CO3) + c (HCO3- ) + c (CO32- ) =0.2mol•L-1
(3)工业上可用CO2来制甲醇
①CO2 (g) + 3H2(g)
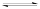 CH3OH(g) + H2O(g) ΔH < 0
CH3OH(g) + H2O(g) ΔH < 0根据图1分析,实际工业生产中,反应温度选择250℃的理由
②利用光电催化原理,由CO2和H2O制备CH3OH的装置如图2。写出右侧的电极反应式

您最近一年使用:0次
【推荐2】煤气中主要的含硫杂质有 以及COS(有机硫),煤气燃烧后含硫杂质会转化成
以及COS(有机硫),煤气燃烧后含硫杂质会转化成 从而引起大气污染,因此煤气中
从而引起大气污染,因此煤气中 的脱出程度已成为煤气洁净度的一个重要指标。请回答下列问题:
的脱出程度已成为煤气洁净度的一个重要指标。请回答下列问题:
(1)脱除煤气中CoS的方法有 的KOH溶液氧化法,
的KOH溶液氧化法, 还原法、水解法等。已知:
还原法、水解法等。已知: 、COS、
、COS、 、CO的燃烧热依次为285kJ/mol,299kJ/mol,586kJ/mol、283kJ/mol;
、CO的燃烧热依次为285kJ/mol,299kJ/mol,586kJ/mol、283kJ/mol; 还原COS发生的反应为
还原COS发生的反应为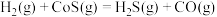 ,该反应的
,该反应的
___________  。
。
(2)较普遍采用的 处理方法是克劳斯工艺即高温热分解
处理方法是克劳斯工艺即高温热分解 ,原理为:
,原理为: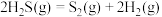 。在1470K、l00kPa反应条件下,将
。在1470K、l00kPa反应条件下,将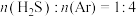 的混合气进行
的混合气进行 热分解反应。平衡时混合气中
热分解反应。平衡时混合气中 与
与 的分压相等,
的分压相等, 平衡转化率为
平衡转化率为___________ ,平衡常
___________  。
。
(3)在1373K、100kPa反应条件下,对于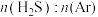 分别为4:1、1:1、1:4、1:9、1:19的
分别为4:1、1:1、1:4、1:9、1:19的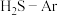 混合气,热分解反应过程中
混合气,热分解反应过程中 转化率随时间的变化如图所示。
转化率随时间的变化如图所示。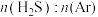 越大,
越大, 平衡转化率
平衡转化率___________ ,理由是___________ 。
②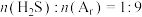 对应图中曲线
对应图中曲线___________ ,计算其在0-0.1s之间, 分压的平均变化率为
分压的平均变化率为___________  。
。
(4)我国科研团队近期开发了一种新型铠甲催化剂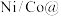 石墨烯,可以高效去除合成气中的
石墨烯,可以高效去除合成气中的 杂质并耦合产氢,其工作原理如图所示。
杂质并耦合产氢,其工作原理如图所示。___________ 。
 以及COS(有机硫),煤气燃烧后含硫杂质会转化成
以及COS(有机硫),煤气燃烧后含硫杂质会转化成 从而引起大气污染,因此煤气中
从而引起大气污染,因此煤气中 的脱出程度已成为煤气洁净度的一个重要指标。请回答下列问题:
的脱出程度已成为煤气洁净度的一个重要指标。请回答下列问题:(1)脱除煤气中CoS的方法有
 的KOH溶液氧化法,
的KOH溶液氧化法, 还原法、水解法等。已知:
还原法、水解法等。已知: 、COS、
、COS、 、CO的燃烧热依次为285kJ/mol,299kJ/mol,586kJ/mol、283kJ/mol;
、CO的燃烧热依次为285kJ/mol,299kJ/mol,586kJ/mol、283kJ/mol; 还原COS发生的反应为
还原COS发生的反应为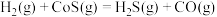 ,该反应的
,该反应的
 。
。(2)较普遍采用的
 处理方法是克劳斯工艺即高温热分解
处理方法是克劳斯工艺即高温热分解 ,原理为:
,原理为: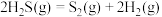 。在1470K、l00kPa反应条件下,将
。在1470K、l00kPa反应条件下,将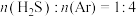 的混合气进行
的混合气进行 热分解反应。平衡时混合气中
热分解反应。平衡时混合气中 与
与 的分压相等,
的分压相等, 平衡转化率为
平衡转化率为
 。
。(3)在1373K、100kPa反应条件下,对于
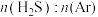 分别为4:1、1:1、1:4、1:9、1:19的
分别为4:1、1:1、1:4、1:9、1:19的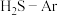 混合气,热分解反应过程中
混合气,热分解反应过程中 转化率随时间的变化如图所示。
转化率随时间的变化如图所示。
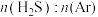 越大,
越大, 平衡转化率
平衡转化率②
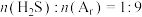 对应图中曲线
对应图中曲线 分压的平均变化率为
分压的平均变化率为 。
。(4)我国科研团队近期开发了一种新型铠甲催化剂
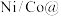 石墨烯,可以高效去除合成气中的
石墨烯,可以高效去除合成气中的 杂质并耦合产氢,其工作原理如图所示。
杂质并耦合产氢,其工作原理如图所示。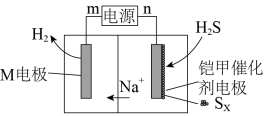
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】将二氧化碳加氢转化为高附加值的化学品或液体燃料是二氧化碳资源化利用的有效方法,其中转换为甲醇被认为是最可能的利用路径,主要涉及反应如下:
反应I: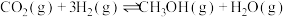
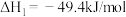
反应II:
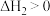
请回答下列问题:
(1)已知 的燃烧热
的燃烧热 和CO的燃烧热
和CO的燃烧热 ,水的汽化热(1mol
,水的汽化热(1mol 从液体汽化为气体所需要吸收的热量)为40.8kJ/mol,则反应II的
从液体汽化为气体所需要吸收的热量)为40.8kJ/mol,则反应II的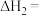
_______ 。
(2) 和
和 在某NiO支撑的
在某NiO支撑的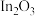 表面的反应历程如下图所示。(TS表示过渡态)
表面的反应历程如下图所示。(TS表示过渡态)

决定总反应速率的步骤的反应方程式为_______ ,该步骤的活化能
_______ eV。
(3)恒定压强P下,体积比1:3的 和
和 发生反应I、反应II,反应相同时间,测得不同温度下
发生反应I、反应II,反应相同时间,测得不同温度下 的转化率和
的转化率和 的选择性如下图中实验值所示。图中平衡值表示相同条件下平衡状态
的选择性如下图中实验值所示。图中平衡值表示相同条件下平衡状态 的转化率和
的转化率和 的选择性随温度的变化[
的选择性随温度的变化[ 的选择性
的选择性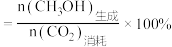 ]
]

①当温度高于260℃时,二氧化碳的平衡转化率随温度升高而增大的原因是_______ 。
②260℃时,甲醇产率的实验值是_______ 。220℃-260℃甲醇的选择性随温度升高降低的原因是_______ 。
③220℃时,反应II的化学平衡常数
_______ 。
反应I:
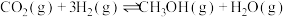
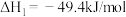
反应II:

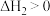
请回答下列问题:
(1)已知
 的燃烧热
的燃烧热 和CO的燃烧热
和CO的燃烧热 ,水的汽化热(1mol
,水的汽化热(1mol 从液体汽化为气体所需要吸收的热量)为40.8kJ/mol,则反应II的
从液体汽化为气体所需要吸收的热量)为40.8kJ/mol,则反应II的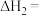
(2)
 和
和 在某NiO支撑的
在某NiO支撑的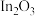 表面的反应历程如下图所示。(TS表示过渡态)
表面的反应历程如下图所示。(TS表示过渡态)
决定总反应速率的步骤的反应方程式为

(3)恒定压强P下,体积比1:3的
 和
和 发生反应I、反应II,反应相同时间,测得不同温度下
发生反应I、反应II,反应相同时间,测得不同温度下 的转化率和
的转化率和 的选择性如下图中实验值所示。图中平衡值表示相同条件下平衡状态
的选择性如下图中实验值所示。图中平衡值表示相同条件下平衡状态 的转化率和
的转化率和 的选择性随温度的变化[
的选择性随温度的变化[ 的选择性
的选择性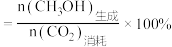 ]
]
①当温度高于260℃时,二氧化碳的平衡转化率随温度升高而增大的原因是
②260℃时,甲醇产率的实验值是
③220℃时,反应II的化学平衡常数

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】甲酸是基本有机化工原料之一,广泛用于农药、皮革、染料、医药和橡胶等工业。
(1)工业上利用甲酸的能量关系转换图如下:
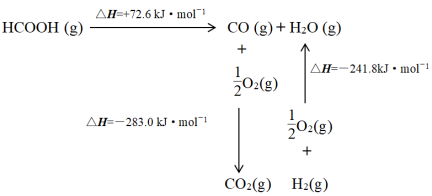
反应HCOOH(g) CO2 (g) + H2(g) 的焓变△H =
CO2 (g) + H2(g) 的焓变△H =__________________ kJ·mol-1。
(2)某科学小组研究不同压强条件对反应CO2(g) + H2(g) HCOOH(g) 的影响。t℃下,在一个容积可变的密闭容器中,充入一定量的CO2和H2,测得不同压强下,平衡时容器内气体的浓度如下表:
HCOOH(g) 的影响。t℃下,在一个容积可变的密闭容器中,充入一定量的CO2和H2,测得不同压强下,平衡时容器内气体的浓度如下表:
试回答以下问题:
①平衡时,实验1的正反应速率______ (填“>”、“<”或“=”)实验3的逆反应速率。
②由实验1的数据可计算t℃时,该反应的平衡常数K=________________ 。
③ a=___________ mol·L-1
(3)经研究发现采用电还原法也可将CO2转化为甲酸根,同时还能提高CO2的转换效率。其电解原理如图所示,下列叙述正确的是__________ 。

A.Sn极的电极方程式为CO2 + 2e﹣+ HCO3﹣=HCOO﹣+ CO32﹣
B.电解过程中K+向Pt极移动
C.Pt极发生还原反应并有气体逸出
D.电解过程中HCO3﹣浓度逐渐减小
(4)甲酸的用途之一是用于配制“缓冲溶液”,在这种溶液中加入少量的强酸或强碱,溶液的pH变化不大,能保持溶液pH相对稳定。(已知甲酸的电离平衡常数Ka=1.8×10-4)
①现将等浓度甲酸与甲酸钠溶液混合,配成0.1 mol·L-1的HCOOH-HCOONa溶液。用离子方程式表示将少量强碱加入HCOOH-HCOONa缓冲溶液中,pH变化不大的原因_______________ 。
②若用100mL 0.2mol·L-1HCOOH溶液配制pH为4的缓冲溶液,需加入_________ (答案保留一位小数)mL 0.2mol· L-1NaOH溶液。
(1)工业上利用甲酸的能量关系转换图如下:

反应HCOOH(g)
 CO2 (g) + H2(g) 的焓变△H =
CO2 (g) + H2(g) 的焓变△H =(2)某科学小组研究不同压强条件对反应CO2(g) + H2(g)
 HCOOH(g) 的影响。t℃下,在一个容积可变的密闭容器中,充入一定量的CO2和H2,测得不同压强下,平衡时容器内气体的浓度如下表:
HCOOH(g) 的影响。t℃下,在一个容积可变的密闭容器中,充入一定量的CO2和H2,测得不同压强下,平衡时容器内气体的浓度如下表:| 实验编号 | 反应压强 | 物质浓度(mol·L-1) | ||
| CO2 | H2 | HCOOH | ||
| 1 | p1 | 0.3 | 0.3 | 0.9 |
| 2 | p2 | a | a | 0.4 |
| 3 | p3 | 0.4 | 0.4 | b |
试回答以下问题:
①平衡时,实验1的正反应速率
②由实验1的数据可计算t℃时,该反应的平衡常数K=
③ a=
(3)经研究发现采用电还原法也可将CO2转化为甲酸根,同时还能提高CO2的转换效率。其电解原理如图所示,下列叙述正确的是

A.Sn极的电极方程式为CO2 + 2e﹣+ HCO3﹣=HCOO﹣+ CO32﹣
B.电解过程中K+向Pt极移动
C.Pt极发生还原反应并有气体逸出
D.电解过程中HCO3﹣浓度逐渐减小
(4)甲酸的用途之一是用于配制“缓冲溶液”,在这种溶液中加入少量的强酸或强碱,溶液的pH变化不大,能保持溶液pH相对稳定。(已知甲酸的电离平衡常数Ka=1.8×10-4)
①现将等浓度甲酸与甲酸钠溶液混合,配成0.1 mol·L-1的HCOOH-HCOONa溶液。用离子方程式表示将少量强碱加入HCOOH-HCOONa缓冲溶液中,pH变化不大的原因
②若用100mL 0.2mol·L-1HCOOH溶液配制pH为4的缓冲溶液,需加入
您最近一年使用:0次
【推荐2】直接排放含SO2的烟气会形成酸雨,危害环境。工业上常采用催化还原法和碱吸收法处理SO2气体。
(1)如图所示:1molCH4完全燃烧生成气态水的能量变化和1molS(g)燃烧的能量变化。
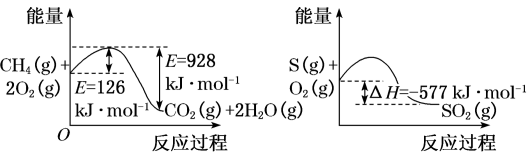
在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式___ 。
(2)焦炭催化还原二氧化硫的化学方程式为2C(s)+2SO2(g) S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率和S2(g)的生成速率随温度变化的关系如图所示:
S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率和S2(g)的生成速率随温度变化的关系如图所示:

①A、B、C、D四点对应的状态中,达到平衡状态的有___ (填字母)。
②该反应的ΔH___ 0(填“>”“<”或“=”)
③下列措施能够增大SO2平衡转化率的是___ 。
A.降低温度 B.增加C的量 C.减小容器体积 D.添加高效催化剂
(3)用氨水吸收SO2。25℃时2.0mol·L-1的氨水中,NH3·H2O的电离度α=___ (α= ×100%)。。将含SO2的烟气通入该氨水中,当溶液显中性时,溶液中的
×100%)。。将含SO2的烟气通入该氨水中,当溶液显中性时,溶液中的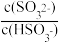 =
=___ 。(已知25℃,Kb(NH3·H2O)=1.8×10-5;Ka1(H2SO3)=1.3×10-2,Ka2(H2SO3)=6.2×10-8)
(4)当吸收液失去吸收能力后通入O2可得到NH4HSO4溶液,用如图所示装置电解所得NH4HSO4溶液可制得强氧化剂(NH4)2S2O8。

写出电解NH4HSO4溶液的化学方程式___ 。
(1)如图所示:1molCH4完全燃烧生成气态水的能量变化和1molS(g)燃烧的能量变化。

在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式
(2)焦炭催化还原二氧化硫的化学方程式为2C(s)+2SO2(g)
 S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率和S2(g)的生成速率随温度变化的关系如图所示:
S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率和S2(g)的生成速率随温度变化的关系如图所示:
①A、B、C、D四点对应的状态中,达到平衡状态的有
②该反应的ΔH
③下列措施能够增大SO2平衡转化率的是
A.降低温度 B.增加C的量 C.减小容器体积 D.添加高效催化剂
(3)用氨水吸收SO2。25℃时2.0mol·L-1的氨水中,NH3·H2O的电离度α=
 ×100%)。。将含SO2的烟气通入该氨水中,当溶液显中性时,溶液中的
×100%)。。将含SO2的烟气通入该氨水中,当溶液显中性时,溶液中的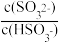 =
=(4)当吸收液失去吸收能力后通入O2可得到NH4HSO4溶液,用如图所示装置电解所得NH4HSO4溶液可制得强氧化剂(NH4)2S2O8。

写出电解NH4HSO4溶液的化学方程式
您最近一年使用:0次
【推荐3】氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。
(1)甲烷水蒸气催化重整是制高纯氢的方法之一
①反应器中初始反应的生成物为 和
和 ,其物质的量之比为4:1,甲烷和水蒸气反应的方程式是
,其物质的量之比为4:1,甲烷和水蒸气反应的方程式是_______ 。
②已知反应器中还存在如下反应:
i.

ii.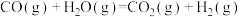

iii.

……
iii为积炭反应,利用 和
和 计算
计算 时,还需要利用
时,还需要利用_______ 反应的△H。
③反应物投料比采用 ,大于初始反应的化学计量数之比,目的是
,大于初始反应的化学计量数之比,目的是_______ (选填字母序号)。
a.促进 转化 b.促进CO转化为
转化 b.促进CO转化为 c.减少积炭生成
c.减少积炭生成
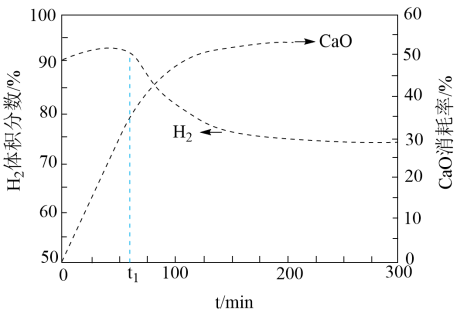
④用CaO可以去除 。
。 体积分数和CaO消耗率随时间变化关系如下图所示。从
体积分数和CaO消耗率随时间变化关系如下图所示。从 时开始,
时开始, 体积分数显著降低,单位时间CaO消耗率
体积分数显著降低,单位时间CaO消耗率_______ (填“升高”“降低”或“不变”)。此时CaO消耗率约为35%,但已失效结合化学方程式解释原因:_______ 。
(2)可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接 或
或 ,可交替得到
,可交替得到 和
和 。
。
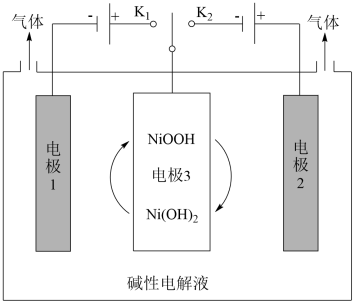
①制 时,连接
时,连接_______ 。
②改变开关连接方式,可得 ,产生
,产生 的电极反应式是
的电极反应式是_______
③结合①和②中电极3的电极反应式,说明电极3的作用:_______ 。
(1)甲烷水蒸气催化重整是制高纯氢的方法之一
①反应器中初始反应的生成物为
 和
和 ,其物质的量之比为4:1,甲烷和水蒸气反应的方程式是
,其物质的量之比为4:1,甲烷和水蒸气反应的方程式是②已知反应器中还存在如下反应:
i.


ii.
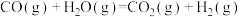

iii.


……
iii为积炭反应,利用
 和
和 计算
计算 时,还需要利用
时,还需要利用③反应物投料比采用
 ,大于初始反应的化学计量数之比,目的是
,大于初始反应的化学计量数之比,目的是a.促进
 转化 b.促进CO转化为
转化 b.促进CO转化为 c.减少积炭生成
c.减少积炭生成④用CaO可以去除
 。
。 体积分数和CaO消耗率随时间变化关系如下图所示。从
体积分数和CaO消耗率随时间变化关系如下图所示。从 时开始,
时开始, 体积分数显著降低,单位时间CaO消耗率
体积分数显著降低,单位时间CaO消耗率
(2)可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接
 或
或 ,可交替得到
,可交替得到 和
和 。
。
①制
 时,连接
时,连接②改变开关连接方式,可得
 ,产生
,产生 的电极反应式是
的电极反应式是③结合①和②中电极3的电极反应式,说明电极3的作用:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有部分前36号元素的性质或原子结构信息如下表:
(1) 元素的第一电离能要大于其同周期相邻的元素,原因是
元素的第一电离能要大于其同周期相邻的元素,原因是______ 。
(2) 元素的常见化合价为
元素的常见化合价为______ ,原因是______ 。
(3) 元素的原子
元素的原子 能层上电子数为
能层上电子数为______ 。
(4) 的电子排布图违背了
的电子排布图违背了______ 。用 的单质、碱金属盐等可以制作焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:
的单质、碱金属盐等可以制作焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:______ 。
| 元素 | 元素的性质或原子结构 |
 | 基态原子的最外层有3个未成对电子,次外层有2个电子 |
 | 单质能与水剧烈反应,所得溶液呈弱酸性 |
 | 基态原子 轨道上有1个电子 轨道上有1个电子 |
 | 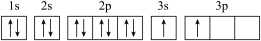 |
 元素的第一电离能要大于其同周期相邻的元素,原因是
元素的第一电离能要大于其同周期相邻的元素,原因是(2)
 元素的常见化合价为
元素的常见化合价为(3)
 元素的原子
元素的原子 能层上电子数为
能层上电子数为(4)
 的电子排布图违背了
的电子排布图违背了 的单质、碱金属盐等可以制作焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:
的单质、碱金属盐等可以制作焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知X、Y、Z、W、Q是原子序数依次增大的前四周期元素。X原子核外有6种不同运动状态的电子;Y基态原子中s电子总数与p电子总数相等;Z最高价氧化物对应水化物的碱性在同周期元素中最强;W基态原子的最外层p轨道有2个电子的自旋状态与其他电子的自旋状态相反。
(1)基态X原子中电子占据的最高能级的原子轨道形状为_______ 。原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为_______ 。
(2)Y、Z、W的简单离子半径由大到小的顺序为_______ 。(用离子符号表示)
(3)Q是生活中使用最广泛的一种金属。
①Q的原子结构示意图为_______ 。
②检验溶液中是否含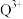 离子的试剂是
离子的试剂是_______ (填化学式),现象为_______ 。
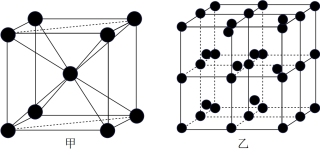
③Q的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的截面图是_______ (填字母序号)。
A.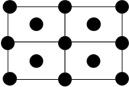 B.
B.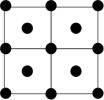 C.
C.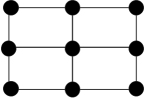 D.
D.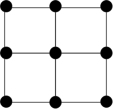
(1)基态X原子中电子占据的最高能级的原子轨道形状为
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为(2)Y、Z、W的简单离子半径由大到小的顺序为
(3)Q是生活中使用最广泛的一种金属。
①Q的原子结构示意图为
②检验溶液中是否含
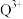 离子的试剂是
离子的试剂是③Q的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的截面图是

A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】白磷(P4)在化工、军事等领域有着广泛应用。工业上采用Ca3(PO4)2、SiO2及C为原料制备,产物除P4外,还有CaSiO3、CO等。
回答下列问题:
(1)下列状态的钙中,电离最外层第一个电子所需能量最小的是________ (填选项字母)。
A.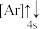 B.
B.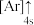 C.
C.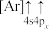 D.
D.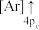
(2)SiO2硬而脆,其原因是_____________________________________________________ 。
(3) 的空间构型为
的空间构型为____________________________ ,酸性条件下,可与Fe3+形成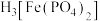 从而掩蔽溶液中的Fe3+,基态Fe3+核外M层有
从而掩蔽溶液中的Fe3+,基态Fe3+核外M层有________ 种空间运动状态不同的电子。
(4)P4分子中P原子的杂化形式为_______________________________ ,P4难溶于水而易溶于CS2,原因是____________________________________ 。
(5)CO可与第四周期过渡元素形成羰基配合物,形成配合物时,每个CO提供一对电子与金属原子形成配位键,研究发现金属原子的价电子和CO提供的电子总和等于18。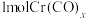 中所含
中所含 键的物质的量为
键的物质的量为________ mol(填数值)
(6)天然硅酸盐组成复杂,其复杂性在其阴离子,而阴离子的基本结构单元是硅氧四面体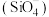 。硅、氧原子通过共用氧原子形成各种不同的硅酸根负离子,无限长链的硅酸根离子(如图a所示)的化学式可用通式表示为
。硅、氧原子通过共用氧原子形成各种不同的硅酸根负离子,无限长链的硅酸根离子(如图a所示)的化学式可用通式表示为_____________________________ (用n代表Si原子数,不考虑边界氧原子)。
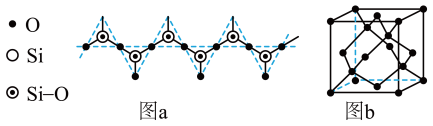
(7)单晶硅的晶体结构与金刚石的一种晶体结构相似(如图b所示),则晶胞中Si原子的体积占晶胞体积的百分率为________ (列出计算式即可)。
回答下列问题:
(1)下列状态的钙中,电离最外层第一个电子所需能量最小的是
A.
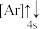 B.
B.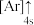 C.
C.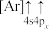 D.
D.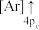
(2)SiO2硬而脆,其原因是
(3)
 的空间构型为
的空间构型为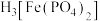 从而掩蔽溶液中的Fe3+,基态Fe3+核外M层有
从而掩蔽溶液中的Fe3+,基态Fe3+核外M层有(4)P4分子中P原子的杂化形式为
(5)CO可与第四周期过渡元素形成羰基配合物,形成配合物时,每个CO提供一对电子与金属原子形成配位键,研究发现金属原子的价电子和CO提供的电子总和等于18。
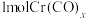 中所含
中所含 键的物质的量为
键的物质的量为(6)天然硅酸盐组成复杂,其复杂性在其阴离子,而阴离子的基本结构单元是硅氧四面体
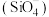 。硅、氧原子通过共用氧原子形成各种不同的硅酸根负离子,无限长链的硅酸根离子(如图a所示)的化学式可用通式表示为
。硅、氧原子通过共用氧原子形成各种不同的硅酸根负离子,无限长链的硅酸根离子(如图a所示)的化学式可用通式表示为
(7)单晶硅的晶体结构与金刚石的一种晶体结构相似(如图b所示),则晶胞中Si原子的体积占晶胞体积的百分率为
您最近一年使用:0次



