将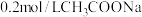 溶液与0.1mol/LHCl溶液等体积混合(忽略温度变化),下列说法正确的是
溶液与0.1mol/LHCl溶液等体积混合(忽略温度变化),下列说法正确的是
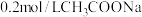 溶液与0.1mol/LHCl溶液等体积混合(忽略温度变化),下列说法正确的是
溶液与0.1mol/LHCl溶液等体积混合(忽略温度变化),下列说法正确的是A.混合溶液中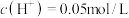 |
B.混合后 的水解常数增大 的水解常数增大 |
C.混合溶液中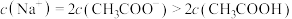 |
D.混合后加入适量 固体, 固体, 的电离平衡向右移动 的电离平衡向右移动 |
2023·重庆·模拟预测 查看更多[2]
更新时间:2023-03-31 16:59:38
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】欲使0.1mol/L的稀氨水中,C(NH3·H2O)/C(OH-)逐渐减小,可采取的措施是:
| A.加入少量Al(OH)3固体 | B.加入少量NaOH晶体 |
| C.加入少量NH4Cl晶体 | D.继续加0.1mol/L的稀氨水 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】向0.1 mol·L-1 CH3COOH溶液中加入少量的CH3COONa晶体时,会引起
| A.溶液中的c(H+)减小 | B.溶液中的c(H+)增大 |
| C.溶液的导电能力减弱 | D.溶液中的c(OH-)减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列叙述正确的是
| A.不能用红外光谱区分C2H5OH和CH3OCH3 |
| B.铁管镀锌层局部破损后,铁管仍不易生锈 |
| C.某温度下,一元弱酸HA的Ka越小,则NaA的Kh(水解常数)越小 |
| D.25℃时,pH=2的硫酸与pH =12的NaOH溶液等体积混合溶液显酸性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】25℃时,向100mL
 溶液中滴加
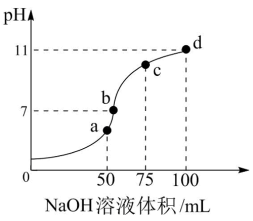
溶液中滴加 的NaOH溶液,所得溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
的NaOH溶液,所得溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是

 溶液中滴加
溶液中滴加 的NaOH溶液,所得溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
的NaOH溶液,所得溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
A.由a到b发生反应的离子方程式为 |
B.d点处存在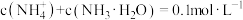 |
| C.图中a、b、c、d四个点,水的电离程度最大的是b点 |
D.25℃时,K(NH3·H2O)约为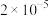 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某课外活动小组对采集的酸雨样品进行化验,测得数据如下:c(Na+)=5.0×10-6 mol/L、c(NH4+)=2.0×10-5 mol/L、c(NO )=2.0×10-4 mol/L、c(SO
)=2.0×10-4 mol/L、c(SO )=4.0×10-4 mol/L,H+和OH-浓度未测定,则此酸雨的pH约为
)=4.0×10-4 mol/L,H+和OH-浓度未测定,则此酸雨的pH约为
 )=2.0×10-4 mol/L、c(SO
)=2.0×10-4 mol/L、c(SO )=4.0×10-4 mol/L,H+和OH-浓度未测定,则此酸雨的pH约为
)=4.0×10-4 mol/L,H+和OH-浓度未测定,则此酸雨的pH约为| A.3 | B.4 | C.5 | D.6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】25℃时,用NaOH调节0.1mol∙L-1 H2C2O4溶液的pH,假设不同pH下均有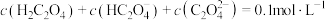 ,使用数字传感器测得溶液中各含碳微粒的物质的量浓度随pH的变化曲线如图。下列有关分析正确的是
,使用数字传感器测得溶液中各含碳微粒的物质的量浓度随pH的变化曲线如图。下列有关分析正确的是
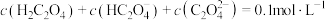 ,使用数字传感器测得溶液中各含碳微粒的物质的量浓度随pH的变化曲线如图。下列有关分析正确的是
,使用数字传感器测得溶液中各含碳微粒的物质的量浓度随pH的变化曲线如图。下列有关分析正确的是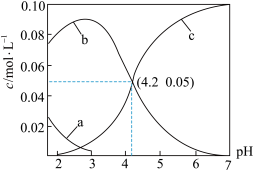
| A.曲线b代表H2C2O4浓度随pH的变化 |
B.HC2O4- C2O42-+ H+ K = 1×10-4.2 C2O42-+ H+ K = 1×10-4.2 |
| C.pH从4到6时主要发生反应的离子方程式为2OH- + H2C2O4 = 2H2O + C2O42- |
D.当溶液pH = 7 时: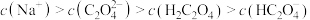 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对于常温下
 溶液,叙述正确的是
溶液,叙述正确的是

 溶液,叙述正确的是
溶液,叙述正确的是A.温度升高,溶液的pH升高,但溶液中的 与 与 乘积不变 乘积不变 |
B.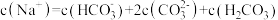 |
| C.加入适量的NaOH固体,溶液的pH减小 |
D.与等体积等浓度的 溶液反应后,溶液中 溶液反应后,溶液中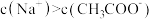 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列溶液中微粒的物质的量浓度关系正确的是
A.室温下,向0.01 mol·L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)+c(H+)+c(NH )=c(SO )=c(SO )+c(OH-) )+c(OH-) |
B.0.1 mol·L-1NaHCO3溶液: c(Na+)>c(OH-)>c(HCO )>c(H+) )>c(H+) |
C.Na2CO3溶液:c(OH-)=c(HCO )+2c(H2CO3)+c(H+) )+2c(H2CO3)+c(H+) |
| D.25℃时,浓度均为0.1 mol·L-1的CH3COOH、CH3COONa等体积混合溶液呈酸性:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)> c(OH-) |
您最近一年使用:0次

 )
) )>c(H+)>c(OH-)
)>c(H+)>c(OH-)

