下列有关工业生产的叙述正确的是
| A.合成氨生产过程中升高温度可加快反应速率,缩短生产周期,故温度越高越好 |
| B.硫酸工业中,使用催化剂是为了提高SO2转化为SO3的转化率 |
| C.合成氨工业中,将NH3及时液化分离有利于氨的生产 |
| D.硫酸工业中,SO2的催化氧化不采用高压,是因为压强对SO2转化率无影响 |
更新时间:2023-04-07 16:06:30
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】工业合成氨原理反应总方程式为N2(g) + 3H2(g)⇌2NH3(g),包含多个基元反应,其反应机理如图所示,已知各物质在催化剂表面吸附放出能量。下列说法错误的是


| A.从充入反应物到A处,物质的能量降低,表示N2、H2在催化剂表面吸附过程放热,物质由气态转化为液态,该过程ΔS>0 |
| B.B→C过程决定了总反应的速率 |
| C.工业合成氨选择温度为700K,主要考虑催化剂在此温度下活性较高 |
| D.由图象可知氨气分解为吸热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在新型催化剂 作用下,
作用下, 氧化
氧化 可获得Cl2:
可获得Cl2: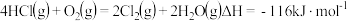 。关于反应
。关于反应 ,下列说法正确的是
,下列说法正确的是
 作用下,
作用下, 氧化
氧化 可获得Cl2:
可获得Cl2: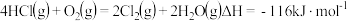 。关于反应
。关于反应 ,下列说法正确的是
,下列说法正确的是A.反应活化能: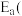 正 正 逆 逆 |
B.每生成标准状况下22.4L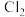 ,放出 ,放出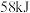 的热量 的热量 |
C.使用高效催化剂,可使平衡时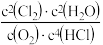 的值增大 的值增大 |
D.断裂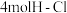 键的同时,有 键的同时,有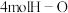 键生成,说明该反应达到平衡状态 键生成,说明该反应达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列方案设计、现象及结论都正确的是
| 方案设计 | 现象 | 结论 | |
| A | 室温下将铝片放入浓硫酸 | 未观察到气泡产生 | 铝片常温下与浓硫酸不反应 |
| B | 将2 mL 0.5mo/L CuCl2溶液置于试管中加热 | 溶液由蓝色变为绿色 | 升高温度可以使平衡 [Cu(H2O)4]2++4Cl-= [CuCl4]2-+4H2O正移 |
| C | 向K2Cr2O7溶液中滴加少量浓NaOH溶液 | 溶液由黄色变为橙色 | 改变溶液pH可以使平衡 +H2O +H2O 2 2 +2H+移动 +2H+移动 |
| D | 将钠块分别投入水和无水乙醇中 | 水中生成气泡,无水乙醇无明显现象 | 水分子中氢原子的活泼性大于乙醇分子中氢原子的活泼性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某温度下, 在固定体积的密闭容器中,可逆反应 A(g) + 3B(g) 2C(g) 达到平衡时,各物质的物质的量之比为A:B:C = 2:2:1,保持温度不变,以2:2:1的物质的量之比再次充入A、B、C,则
2C(g) 达到平衡时,各物质的物质的量之比为A:B:C = 2:2:1,保持温度不变,以2:2:1的物质的量之比再次充入A、B、C,则
 2C(g) 达到平衡时,各物质的物质的量之比为A:B:C = 2:2:1,保持温度不变,以2:2:1的物质的量之比再次充入A、B、C,则
2C(g) 达到平衡时,各物质的物质的量之比为A:B:C = 2:2:1,保持温度不变,以2:2:1的物质的量之比再次充入A、B、C,则| A.平衡逆向移动 | B.平衡时A的体积分数增大 |
| C.平衡时C的体积分数增大 | D.平衡时各气体的体积分数不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列各图中能正确表示A(g)+B(g) 2C(g) ∆H<0这个可逆反应图像的是
2C(g) ∆H<0这个可逆反应图像的是
 2C(g) ∆H<0这个可逆反应图像的是
2C(g) ∆H<0这个可逆反应图像的是A.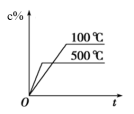 | B.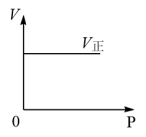 |
C. | D.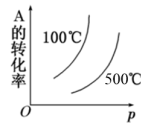 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】化学与生活、社会发展息息相关。下列有关说法正确的是
| A.工业上用金属钠制备金属钾,是因为金属钠的还原性比钾的强 |
| B.《本草纲目》中“石碱”条目下写道:“采蒿蓼之属,晒干烧灰……浣衣发面,甚获利也”,其中“浣衣”与盐类的水解有关 |
| C.牙膏中添加氟化物用于预防齲齿是利用了氧化还原反应的原理 |
| D.党的二十大报告中提到的超级计算机,其处理器芯片主要用到了二氧化硅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实中,不能用勒夏特列原理解释的是
| A.黄绿色的氯水光照后颜色变浅 |
| B.红棕色的NO2,加压后颜色先变深后变浅 |
| C.加入催化剂,有利于SO2与O2反应生成SO3 |
| D.工业合成氨使用过量氮气以提高氢气的平衡转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】合成氨反应N2+3H2=2NH3,初始时氮气、氢气的体积比为1:3,在相同催化剂条件下平衡混合物中氨的体积分数φ(NH3)与温度、压强的关系如图所示;下列说法正确的是
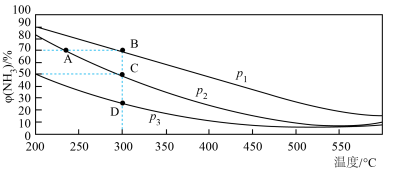

| A.图像中P1<P2<P3 |
| B.A、B、C、D的平衡常数大小关系A=B>C>D |
C.反应速率 逆(状态A)> 逆(状态A)> 逆(状态B) 逆(状态B) |
| D.在C点时,N2的转化率约为67% |
您最近一年使用:0次

 2C(g) (正反应吸热)进行如下操作(只改变该条件):
2C(g) (正反应吸热)进行如下操作(只改变该条件):

