已知常温下部分弱电解质的电离平衡常数如表:
(1)常温下,物质的量浓度相同的三种溶液①NaF溶液②NaClO溶液③Na2CO3溶液,其pH由大到小的顺序是_______ 。(填序号)
(2)25℃时,pH=4的NH4Cl溶液中各离子浓度的大小关系为_______ ,水电离出的氢离子的浓度为_______ 。
(3)NaClO溶液中的质子守恒关系为_______ 。
(4)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式_______ 。
(5)25℃下,将pH=12的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=_______ 。
| 化学式 | HF | HClO | H2CO3 | NH3·H2O |
| 电离常数 | 6.8×10-4 | 4.7×10-8 | K1=4.3×10-7 K2=5.6×10-11 | Kb=1.7×10-5 |
(2)25℃时,pH=4的NH4Cl溶液中各离子浓度的大小关系为
(3)NaClO溶液中的质子守恒关系为
(4)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式
(5)25℃下,将pH=12的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=
更新时间:2023-06-24 17:00:49
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】现有下列状态的物质①干冰②NaHCO3晶体③氨水④纯醋酸⑤FeCl3溶液⑥铜⑦熔融的KOH⑧蔗糖,其中:
(1)属于电解质的是_____ ,属于非电解质的是_____ ,能导电的电解质是_____ 。
(2)写出FeCl3的电离方程式:_____ 。
(3)写出NaHCO3与稀盐酸反应的离子方程式:_____ 。
(4)胶体是一种常见的分散系,回答下列问题。
①向煮沸的蒸馏水中逐滴加入_____ 溶液,继续煮沸至_____ ,停止加热,可制得Fe(OH)3胶体,提纯该胶体应采用_____ 方法,写出制取Fe(OH)3胶体化学反应方程式为_____ 。
②向Fe(OH)3胶体中加入Na2SO4饱和溶液,由于_____ 离子(填离子符号)的作用,使胶体形成了沉淀,这个过程叫做_____ 。
③区分胶体和溶液常用的方法叫做_____ 。
(1)属于电解质的是
(2)写出FeCl3的电离方程式:
(3)写出NaHCO3与稀盐酸反应的离子方程式:
(4)胶体是一种常见的分散系,回答下列问题。
①向煮沸的蒸馏水中逐滴加入
②向Fe(OH)3胶体中加入Na2SO4饱和溶液,由于
③区分胶体和溶液常用的方法叫做
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)实验室制取CO2的离子反应方程式:________________________________________ ;
(2)CO2与足量的NaOH溶液反应的离子方程式:________________________________ ;
(3)氢氧化铁胶体制备的离子反应:_____________________________________________ ;
(4)同温同压条件下,N2与O2的摩尔质量比为:__________ 。
(2)CO2与足量的NaOH溶液反应的离子方程式:
(3)氢氧化铁胶体制备的离子反应:
(4)同温同压条件下,N2与O2的摩尔质量比为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.现有下列10种物质:①铜 ②熔融KCl ③ ④
④ ⑤
⑤ 晶体 ⑥胆矾 ⑦碳酸钙 ⑧
晶体 ⑥胆矾 ⑦碳酸钙 ⑧ ⑨盐酸 ⑩酒精
⑨盐酸 ⑩酒精
(1)上述物质中属于电解质的有_______ ,能导电的有_______ 。(填序号)
(2)⑧在熔化状态下电离方程式为:_______ 。
(3)少量④通入③的溶液中,反应的离子方程式为:_______ 。
(4)写出⑤在水溶液中的电离方程式:_______ 。
(5)向 溶液逐滴加入
溶液逐滴加入 溶液至
溶液至 恰好完全沉淀,发生反应的离子方程式为
恰好完全沉淀,发生反应的离子方程式为_______ ,然后继续滴加 溶液时,此步发生反应的离子方程式为
溶液时,此步发生反应的离子方程式为_______ 。
Ⅱ.现有课外活动小组进行 胶体的制备并检验其性质,甲同学在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和
胶体的制备并检验其性质,甲同学在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,继续煮沸并用玻璃棒搅拌至溶液呈红褐色,停止加热,即制得
溶液,继续煮沸并用玻璃棒搅拌至溶液呈红褐色,停止加热,即制得 胶体。
胶体。
(6)①请评价该操作是否正确_______ (填“正确”或“不正确”)
②乙同学将用氯化铁溶液制得的氢氧化铁胶体放入半透膜制成的袋内,如图所示,放置2min后取少量半透膜外的液体于试管中,置于暗处用一束强光从侧面照射,观察_______ (填“有”或“无”)丁达尔现象,这个实验可以用来区别_______ 。

 ④
④ ⑤
⑤ 晶体 ⑥胆矾 ⑦碳酸钙 ⑧
晶体 ⑥胆矾 ⑦碳酸钙 ⑧ ⑨盐酸 ⑩酒精
⑨盐酸 ⑩酒精(1)上述物质中属于电解质的有
(2)⑧在熔化状态下电离方程式为:
(3)少量④通入③的溶液中,反应的离子方程式为:
(4)写出⑤在水溶液中的电离方程式:
(5)向
 溶液逐滴加入
溶液逐滴加入 溶液至
溶液至 恰好完全沉淀,发生反应的离子方程式为
恰好完全沉淀,发生反应的离子方程式为 溶液时,此步发生反应的离子方程式为
溶液时,此步发生反应的离子方程式为Ⅱ.现有课外活动小组进行
 胶体的制备并检验其性质,甲同学在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和
胶体的制备并检验其性质,甲同学在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,继续煮沸并用玻璃棒搅拌至溶液呈红褐色,停止加热,即制得
溶液,继续煮沸并用玻璃棒搅拌至溶液呈红褐色,停止加热,即制得 胶体。
胶体。(6)①请评价该操作是否正确
②乙同学将用氯化铁溶液制得的氢氧化铁胶体放入半透膜制成的袋内,如图所示,放置2min后取少量半透膜外的液体于试管中,置于暗处用一束强光从侧面照射,观察

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知水在25 ℃和100 ℃时,其电离平衡曲线如图所示:
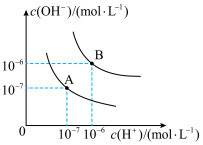
(1)B点所处曲线的温度为___________ ℃(填“25”或“100”)。
(2)25 ℃时,将pH=11的NaOH溶液稀释100倍,稀释后溶液的pH=___________ 。
(3)25 ℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,所得混合溶液的pH=7,则NaOH溶液与硫酸溶液的体积比为___________ 。
(4)100 ℃时,pH=3的HCl溶液和pH=10的NaOH溶液等体积混合后,溶液显___________ 。(填“酸性”“碱性”或“中性”)
(5)100 ℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是___________ 。
(6)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程度分别用α1、α2表示,则α1___________ α2(填“>”“<”或“=”)。
(7)曲线B对应的温度下,将0.02 mol·L-1 Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合后,混合溶液的pH=___________ 。

(1)B点所处曲线的温度为
(2)25 ℃时,将pH=11的NaOH溶液稀释100倍,稀释后溶液的pH=
(3)25 ℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,所得混合溶液的pH=7,则NaOH溶液与硫酸溶液的体积比为
(4)100 ℃时,pH=3的HCl溶液和pH=10的NaOH溶液等体积混合后,溶液显
(5)100 ℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是
(6)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程度分别用α1、α2表示,则α1
(7)曲线B对应的温度下,将0.02 mol·L-1 Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合后,混合溶液的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知水溶液中 和
和 的关系如图所示:
的关系如图所示:
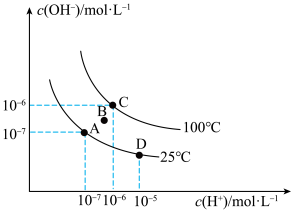
(1)图中B点水的离子积常数___________  (填>、=或<)。
(填>、=或<)。
(2)从A点到D点,可采取的措施是___________ 。
a.升温b.加入少量盐酸c.降温d.加入少量NaOH
(3)100℃时,pH=2的盐酸中水电离产生的H+浓度为___________  。
。
(4)25℃时,将pH=12的NaOH溶液与pH=3的 溶液混合,若所得混合溶液pH=7,则NaOH溶液与
溶液混合,若所得混合溶液pH=7,则NaOH溶液与 溶液的体积比为
溶液的体积比为___________ 。
 和
和 的关系如图所示:
的关系如图所示:
(1)图中B点水的离子积常数
 (填>、=或<)。
(填>、=或<)。(2)从A点到D点,可采取的措施是
a.升温b.加入少量盐酸c.降温d.加入少量NaOH
(3)100℃时,pH=2的盐酸中水电离产生的H+浓度为
 。
。(4)25℃时,将pH=12的NaOH溶液与pH=3的
 溶液混合,若所得混合溶液pH=7,则NaOH溶液与
溶液混合,若所得混合溶液pH=7,则NaOH溶液与 溶液的体积比为
溶液的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】溶液中的反应大多都是离子反应,请按要求回答下列问题:
(1)要求设计实验证明盐类水解是吸热过程,有四位学生分别做了以下实验,其中根据实验现象得出的结论正确的是___ (填字母标号)。
(2)泡沫灭火器的反应原理是盐类水解,请写出其离子方程式:___ 。
(3)将一定浓度的CH3COOH溶液和NaOH溶液等体积混合,测得所得溶液的pH=7,则该溶液中离子浓度的大小关系是___ 。
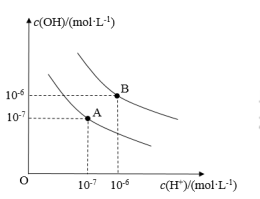
(4)已知水在25℃和95℃时的电离平衡曲线如图所示:95℃时,将pH=9的NaOH溶液与pH=4的H2SO4,溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4,溶液的体积比为___ 。
(5)在一定温度下,有以下三种酸:a.醋酸 b.硫酸 c.盐酸。
①当三种酸物质的量浓度相同时,三种溶液中水的电离程度由大到小的顺序是___ (用a、b、c表示,下同)。
②当三种酸的pH相同、体积相同时,分别加入足量的锌,产生H2的体积(相同状况)大小关系为___ 。
(1)要求设计实验证明盐类水解是吸热过程,有四位学生分别做了以下实验,其中根据实验现象得出的结论正确的是
| A.甲学生:在醋酸钠溶液中滴入酚酞试液,加热后溶液红色加深,说明盐类水解是吸热的 |
| B.乙学生:将硝酸铵晶体溶于水,水温下降,说明硝酸铵水解是吸热的 |
| C.丙学生:在盐酸中加入同温度的氨水,混合液温度下降,说明盐类水解是吸热的 |
| D.丁学生:在醋酸钠溶液中加入醋酸钠晶体,溶液温度下降,说明盐类水解是吸热的 |
(3)将一定浓度的CH3COOH溶液和NaOH溶液等体积混合,测得所得溶液的pH=7,则该溶液中离子浓度的大小关系是
(4)已知水在25℃和95℃时的电离平衡曲线如图所示:95℃时,将pH=9的NaOH溶液与pH=4的H2SO4,溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4,溶液的体积比为

(5)在一定温度下,有以下三种酸:a.醋酸 b.硫酸 c.盐酸。
①当三种酸物质的量浓度相同时,三种溶液中水的电离程度由大到小的顺序是
②当三种酸的pH相同、体积相同时,分别加入足量的锌,产生H2的体积(相同状况)大小关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】合理应用和处理氮的化合物,在生产生活中有重要意义。
Ⅰ.NO2会污染环境,可用Na2CO3溶液吸收NO2并放出CO2,反应产物还有另外两种盐。完成下列填空:
(1)写出上述化学方程式___________ 。
(2)上述反应恰好完全后,所得溶液呈弱碱性,则溶液中各离子浓度大小关系是___________ (不考虑二氧化碳的溶解)。
Ⅱ.氰化钠(NaCN)属于剧毒物质,可用双氧水或硫代硫酸钠处理。
(3)用双氧水处理,发生的反应为:NaCN+H2O2+H2O→A+NH3↑(已配平),则A的化学式为___________ 。
(4)NaCN与Na2S2O3二者等物质的量反应后的溶液中,大量存在的阴离子只有两种且都含硫元素,其中一种遇到Fe3+显血红色,该离子是___________ ,另一种离子是___________ 。
Ⅰ.NO2会污染环境,可用Na2CO3溶液吸收NO2并放出CO2,反应产物还有另外两种盐。完成下列填空:
(1)写出上述化学方程式
(2)上述反应恰好完全后,所得溶液呈弱碱性,则溶液中各离子浓度大小关系是
Ⅱ.氰化钠(NaCN)属于剧毒物质,可用双氧水或硫代硫酸钠处理。
(3)用双氧水处理,发生的反应为:NaCN+H2O2+H2O→A+NH3↑(已配平),则A的化学式为
(4)NaCN与Na2S2O3二者等物质的量反应后的溶液中,大量存在的阴离子只有两种且都含硫元素,其中一种遇到Fe3+显血红色,该离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】常温下,部分酸的电离平衡常数如下:
(1)c(H+)相同的三种酸溶液的浓度从大到小为___ 。
(2)若HCN溶液的起始浓度为0.01mol·L-1,平衡时c(H+)约为__ mol·L-1。使此溶液中HCN的电离程度增大且c(H+)也增大的方法是__ 。
(3)中和等量的NaOH,消耗等pH的氢氟酸和硫酸的体积分别为aL、bL,则a__ (填“大于”“小于”或“等于”,下同)b。中和等浓度、等体积的氢氟酸和硫酸需要NaOH的物质的量为n1、n2,则n1__ n2。
(4)向NaCN溶液中通入少量的CO2,发生反应的离子方程式为__ 。
(5)设计实验证明氢氟酸比HCl的酸性弱__ 。
| 化学式 | HF | HCN | H2CO3 |
| 电离常数 | Ka=3.5×10-4 | Ka=5.0×10-10 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
(1)c(H+)相同的三种酸溶液的浓度从大到小为
(2)若HCN溶液的起始浓度为0.01mol·L-1,平衡时c(H+)约为
(3)中和等量的NaOH,消耗等pH的氢氟酸和硫酸的体积分别为aL、bL,则a
(4)向NaCN溶液中通入少量的CO2,发生反应的离子方程式为
(5)设计实验证明氢氟酸比HCl的酸性弱
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】水是生命的源泉、工业的血液、城市的命脉。请回答下列问题:
(1)纯水在25 ℃时,pH=7,该温度下1 mol·L-1的NaOH溶液中,由水电离出的c(OH-)=________ mol·L-1。
(2)25 ℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为__________ ,由水电离出的c(OH-)=________ mol·L-1。

(3)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如右图所示,则HX的电离常数________ (填“大于”“小于”或“等于”)CH3COOH的电离常数。理由是_______ 。
(4)电离常数是衡量弱电解质电离程度强弱的物理量。已知:
25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三溶液的pH由大到小的顺序为____________________ 。
(1)纯水在25 ℃时,pH=7,该温度下1 mol·L-1的NaOH溶液中,由水电离出的c(OH-)=
(2)25 ℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为

(3)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如右图所示,则HX的电离常数
(4)电离常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 | 电离常数(25 ℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有①0.2mol/LNaOH溶液和②0.2mol/L HX溶液,两溶液等体积混合后,测得溶液中c(Na+)>c(X—)。则:
(1)①中由水电离出的c(OH)-___ ②中由水电离出的c(H+)。(填“>”、“=”或“<”)
(2)上述混合液中共存在___ 种粒子 。且:c(HX)___ c(X-)。(填“>”、“=”或“<”,下同)c(HX)+c(X-)___ 0.1mol/L(忽略体积变化)
请根据电荷守恒写出一个用离子浓度表示的等式:___ 。
(3)上述混合液显___ 性(填“酸”、“碱”或“中”),其原因用离子方程式表示___ 。
(4)已知t℃,KW=1×10-13,则t℃(填“>”或“<”或“=”)___ 25℃。在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4的溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b=___ 。
(1)①中由水电离出的c(OH)-
(2)上述混合液中共存在
请根据电荷守恒写出一个用离子浓度表示的等式:
(3)上述混合液显
(4)已知t℃,KW=1×10-13,则t℃(填“>”或“<”或“=”)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】25℃时,已知 ,对0.1mol/L氨水进行如下操作,回答下列问题:
,对0.1mol/L氨水进行如下操作,回答下列问题:
(1)该氨水的pH=_______ ;若向氨水中加入少量硫酸铵固体,则溶液中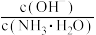 将
将_______ (填“增大”“减小”或“不变”)。
(2)若向氨水中加入稀硫酸,使氨水恰好被中和,此时溶液中离子浓度由大到小的顺序为_______ 。
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时溶液中 ,则
,则 =
=_______ 。
 ,对0.1mol/L氨水进行如下操作,回答下列问题:
,对0.1mol/L氨水进行如下操作,回答下列问题:(1)该氨水的pH=
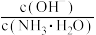 将
将(2)若向氨水中加入稀硫酸,使氨水恰好被中和,此时溶液中离子浓度由大到小的顺序为
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时溶液中
 ,则
,则 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有室温下溶质浓度均为 的几种溶液:①盐酸、②硫酸、③HCN、④硫酸氢铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
的几种溶液:①盐酸、②硫酸、③HCN、④硫酸氢铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
(1)请写出将等体积的①、⑤溶液混合后所得的溶液中的元素质量守恒式:_______ (用浓度表示)
(2)在④溶液中,各离子浓度由大到小的顺序为:_______ 。
(3)将③、⑥混合后,若溶液呈现中性,则消耗量溶液的体积为3_______ ⑥(填“>”“<”或“=”),溶液中的离子浓度由大到小的顺序为_______ 。
(4)常温下,pH均为4的 、
、 、HCl溶液中由水电离出的氢离子浓度之比为
、HCl溶液中由水电离出的氢离子浓度之比为_______ 。
(5)若将③溶液和⑥溶液按体积比2:1混合,所得溶液的质子守恒式为:_______ (用浓度表示)。
(6)在常温下,将 的
的 溶液100mL和
溶液100mL和 的
的 溶液100mL混合,若忽略溶液体积变化,则混合后的溶液的pH为
溶液100mL混合,若忽略溶液体积变化,则混合后的溶液的pH为_______ 。
 的几种溶液:①盐酸、②硫酸、③HCN、④硫酸氢铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
的几种溶液:①盐酸、②硫酸、③HCN、④硫酸氢铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:(1)请写出将等体积的①、⑤溶液混合后所得的溶液中的元素质量守恒式:
(2)在④溶液中,各离子浓度由大到小的顺序为:
(3)将③、⑥混合后,若溶液呈现中性,则消耗量溶液的体积为3
(4)常温下,pH均为4的
 、
、 、HCl溶液中由水电离出的氢离子浓度之比为
、HCl溶液中由水电离出的氢离子浓度之比为(5)若将③溶液和⑥溶液按体积比2:1混合,所得溶液的质子守恒式为:
(6)在常温下,将
 的
的 溶液100mL和
溶液100mL和 的
的 溶液100mL混合,若忽略溶液体积变化,则混合后的溶液的pH为
溶液100mL混合,若忽略溶液体积变化,则混合后的溶液的pH为
您最近一年使用:0次



