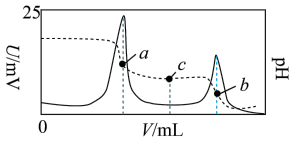
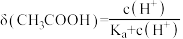某研究小组利用电位滴定法研究盐酸滴定亚磷酸钠( )溶液过程中的化学变化,得到电极电位U和溶液pH随盐酸滴加的体积变化曲线如图所示。下列说法正确的是
)溶液过程中的化学变化,得到电极电位U和溶液pH随盐酸滴加的体积变化曲线如图所示。下列说法正确的是
[已知:①电位滴定法的原理:在化学计量点附近,被测离子浓度发生突跃,指示电极j电位也发生了突跃,进而确定滴定终点。②亚磷酸(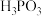 )是二元弱酸,其电离常数分别是
)是二元弱酸,其电离常数分别是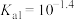 ,
,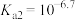 ]
]
 )溶液过程中的化学变化,得到电极电位U和溶液pH随盐酸滴加的体积变化曲线如图所示。下列说法正确的是
)溶液过程中的化学变化,得到电极电位U和溶液pH随盐酸滴加的体积变化曲线如图所示。下列说法正确的是[已知:①电位滴定法的原理:在化学计量点附近,被测离子浓度发生突跃,指示电极j电位也发生了突跃,进而确定滴定终点。②亚磷酸(
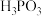 )是二元弱酸,其电离常数分别是
)是二元弱酸,其电离常数分别是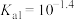 ,
,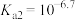 ]
]
A.a点对应溶液的溶质为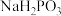 和NaCl,pH>7 和NaCl,pH>7 |
B.第二次电极电位突跃发生的离子反应为 |
C.水的电离程度: |
D.c点对应的溶液中一定存在: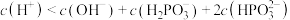 |
更新时间:2023-09-01 18:57:35
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关说法正确的是
| A.将Al2(SO4)3溶液蒸干得到Al2(SO4)3固体 |
| B.用广泛pH试纸测得某溶液pH为11.3 |
| C.向纯水通入少量HCl气体,水的电离程度减小,Kw减小 |
| D.向0.1 mol·L-1 CH3COOH溶液中加少量水,溶液中所有离子的浓度都减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】关于a:0.1 mol·L-1 CH3COONa溶液和b:0.1 mol·L-1 CH3COOH溶液,下列说法不正确的是
| A.两溶液中存在的微粒种类:a>b |
| B.若两者等体积混合,则混合液中微粒有6种 |
| C.若两者按体积比2∶1混合,则混合液中微粒有7种 |
| D.水电离出的c(H+):a>b |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,通过下列实验探究 、
、 溶液的性质
溶液的性质
实验1:向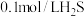 溶液中通入一定体积
溶液中通入一定体积 ,测得溶液pH为7
,测得溶液pH为7
实验2:向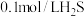 溶液中滴加等体积0.1mol/LNaOH溶液,充分反应后再滴入2滴酚酞,溶液呈红色
溶液中滴加等体积0.1mol/LNaOH溶液,充分反应后再滴入2滴酚酞,溶液呈红色
实验3:向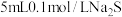 溶液中滴入
溶液中滴入 溶液,产生白色沉淀;再滴入几滴
溶液,产生白色沉淀;再滴入几滴 溶液,立即出现黑色沉淀
溶液,立即出现黑色沉淀
实验4:向 液中逐滴滴加等体积同浓度的盐酸,无明显现象
液中逐滴滴加等体积同浓度的盐酸,无明显现象
下列说法正确的是
 、
、 溶液的性质
溶液的性质实验1:向
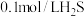 溶液中通入一定体积
溶液中通入一定体积 ,测得溶液pH为7
,测得溶液pH为7实验2:向
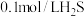 溶液中滴加等体积0.1mol/LNaOH溶液,充分反应后再滴入2滴酚酞,溶液呈红色
溶液中滴加等体积0.1mol/LNaOH溶液,充分反应后再滴入2滴酚酞,溶液呈红色实验3:向
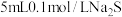 溶液中滴入
溶液中滴入 溶液,产生白色沉淀;再滴入几滴
溶液,产生白色沉淀;再滴入几滴 溶液,立即出现黑色沉淀
溶液,立即出现黑色沉淀实验4:向
 液中逐滴滴加等体积同浓度的盐酸,无明显现象
液中逐滴滴加等体积同浓度的盐酸,无明显现象下列说法正确的是
A.实验1得到的溶液中存在 |
B.由实验2可得出: |
C.由实验3可得出: |
D.实验4得到的溶液中存在: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关粒子间关系的说法不正确的是
A. 溶液与 溶液与 溶液等体积混合 溶液等体积混合 |
B.室温下,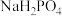 溶液中 溶液中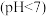 : :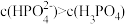 |
C.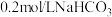 溶液与 溶液与 溶液等体积混合: 溶液等体积混合: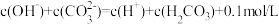 |
D. 水解能力弱于 水解能力弱于 ,则 ,则 的 的 溶液中, 溶液中, 和 和 的总数小于 的总数小于 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】T℃时,水的离子积为Kw,该温度下将x mol·L-1的一元酸HCl与y mol·L-1的一元碱BOH等体积混合,要使混合液呈中性,必须满足的条件是
| A.混合液中c(B+)=c(Cl-)+c(OH-) |
| B.混合液的pH=7 |
C.混合液中c(OH-)=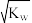 |
| D.x=y |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列溶液有关微粒的物质的量浓度关系正确的是( )
| A.NaHCO3的溶液中有c (Na+)=c (HCO3-) + c (CO32-) + 2c(H2CO3) |
| B.25℃时,pH=2的CH3COOH与pH=12的NaOH等体积混合:c(Na+)>c(CH3COO-) |
| C.pH=3的盐酸与pH=3的醋酸溶液中,水电离的c(H+)前者小 |
| D.常温下,物质的量浓度相等的①NH4HCO3 ②(NH4)2CO3 ③NH4HSO4三种溶液中c(NH4+):②>③>① |
您最近一年使用:0次





 ,实验测得溶液中
,实验测得溶液中 、
、 的分布系数
的分布系数 与
与 ,下列说法错误的是
,下列说法错误的是