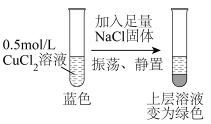
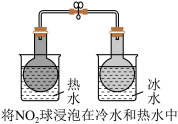
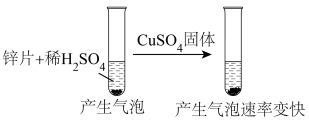
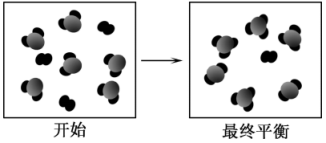
在3个体积均为2.0L的恒容密闭容器中,反应CO2(g)+C(s)  2CO(g) △H>0,分别在一定温度下达到化学平衡状态。下列说法正确的是
2CO(g) △H>0,分别在一定温度下达到化学平衡状态。下列说法正确的是
 2CO(g) △H>0,分别在一定温度下达到化学平衡状态。下列说法正确的是
2CO(g) △H>0,分别在一定温度下达到化学平衡状态。下列说法正确的是 | 容器 | 温度/K | 起始时物质的量/mol | 平衡时物质的量/mol | ||
| n(CO2) | n(C) | n(CO) | n(CO) | ||
| I | 977 | 0.28 | 0.56 | 01 | 0.4 |
| Ⅱ | 977 | 0.56 | 0.56 | 0 | x |
| Ⅲ | 1250 | 0 | 0 | 0.56 | y |
| A.977K,该反应的化学平衡常数值为 1 |
| B.达到平衡时,向容器I中增加C的量 平衡向右移动 |
| C.达到平衡时,容器Ⅱ中CO2的转化率比容器I中的大 |
| D.达到平衡时,容器Ⅲ中的CO 的转化率大于28.6% |
更新时间:2023-10-21 21:23:01
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在恒压、NO和O2的起始浓度均为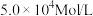 的条件下,催化反应相同时间,测得五种不同浓度下NO转化为NO2的转化率如下表:
的条件下,催化反应相同时间,测得五种不同浓度下NO转化为NO2的转化率如下表:
下列说法错误的是
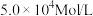 的条件下,催化反应相同时间,测得五种不同浓度下NO转化为NO2的转化率如下表:
的条件下,催化反应相同时间,测得五种不同浓度下NO转化为NO2的转化率如下表:| 温度/℃ | 100 | 200 | 300 | 400 | 500 |
| NO转化率/% | 28.8 | 78.5 | 80.0 | 50.0 | 18.2 |
A.反应 的 的 |
| B.200℃时,延长反应时间能提高NO转化率 |
| C.五种条件下,增加O2的起始浓度不一定都能提高NO的转化率 |
| D.300℃时,该反应一定处于平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】拥有中国自主知识产权的全球首套煤制乙醇工业化项目投产成功。某煤制乙醇过程表示如下:
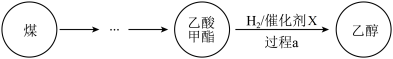
过程a包括以下3个主要反应:
I.

Ⅱ.

Ⅲ.

相同时间内,测得乙酸甲酯转化率随温度的变化如图1所示,乙醇和乙酸乙酯的选择性[乙醇选择性 ]随温度的变化如图2所示。
]随温度的变化如图2所示。

下列说法不正确的是

过程a包括以下3个主要反应:
I.


Ⅱ.


Ⅲ.


相同时间内,测得乙酸甲酯转化率随温度的变化如图1所示,乙醇和乙酸乙酯的选择性[乙醇选择性
 ]随温度的变化如图2所示。
]随温度的变化如图2所示。
下列说法不正确的是
| A.205℃后反应Ⅲ开始发生反应 |
| B.225~235℃,反应I处于平衡状态 |
| C.温度可影响催化剂的选择性,从而影响目标产物乙醇的选择性 |
| D.205℃时,CH3COOCH3起始物质的量为5mol,转化率为30%,则最终生成乙醇0.6mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】科学家曾尝试用焦炭消除烟气中的SO2,其反应原理为2C(s)+2SO2(g) S2(g)+2CO2(g) ΔH<0。一定温度下,向2L的恒容密闭容器中充入2molSO2,并加入合适的催化剂以及足量的焦炭(固体物质的体积可以忽略),反应过程中用压力计测得容器内压强的变化如表所示。
S2(g)+2CO2(g) ΔH<0。一定温度下,向2L的恒容密闭容器中充入2molSO2,并加入合适的催化剂以及足量的焦炭(固体物质的体积可以忽略),反应过程中用压力计测得容器内压强的变化如表所示。
下列说法正确的是
 S2(g)+2CO2(g) ΔH<0。一定温度下,向2L的恒容密闭容器中充入2molSO2,并加入合适的催化剂以及足量的焦炭(固体物质的体积可以忽略),反应过程中用压力计测得容器内压强的变化如表所示。
S2(g)+2CO2(g) ΔH<0。一定温度下,向2L的恒容密闭容器中充入2molSO2,并加入合适的催化剂以及足量的焦炭(固体物质的体积可以忽略),反应过程中用压力计测得容器内压强的变化如表所示。| t/min | 0 | 5 | 10 | 15 | 20 | 25 |
| p/MPa | 8.4 | 9.3 | 9.9. | 10.3 | 10.5 | 10.5 |
| A.其他条件不变,升高温度,正反应速率增大,SO2的平衡转化率也增大 |
| B.其他条件不变,往体系中再加入一定量的焦炭,再次平衡时SO2的体积分数减小 |
| C.若用单位时间内气体分压的变化来表示反应速率,则在0~10min内平均反应速率v(SO2)=0.075MPa•min-1 |
| D.该温度下平衡常数Kp=2.1MPa |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某温度下,可逆反应: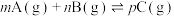 的平衡常数为K,下列对K的说法正确的是
的平衡常数为K,下列对K的说法正确的是
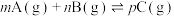 的平衡常数为K,下列对K的说法正确的是
的平衡常数为K,下列对K的说法正确的是A.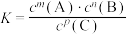 |
B.如果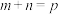 ,则 ,则 |
| C.K值越大,表明该反应越有利于C的生成,平衡时反应物的转化率越大 |
D.增大压强缩小反应器的容积到原来的一半,达到新的平衡时C的浓度为原平衡的1.5倍则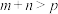 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知:H2(g)+I2(g)  2HI(g)+Q(Q>0)。现将三份物质的量相同的H2(g)和I2(g) 分别投入三个恒容密闭容器中,平衡前后容器的温度无变化。相关数据见下表。
2HI(g)+Q(Q>0)。现将三份物质的量相同的H2(g)和I2(g) 分别投入三个恒容密闭容器中,平衡前后容器的温度无变化。相关数据见下表。
下列说法错误的是
 2HI(g)+Q(Q>0)。现将三份物质的量相同的H2(g)和I2(g) 分别投入三个恒容密闭容器中,平衡前后容器的温度无变化。相关数据见下表。
2HI(g)+Q(Q>0)。现将三份物质的量相同的H2(g)和I2(g) 分别投入三个恒容密闭容器中,平衡前后容器的温度无变化。相关数据见下表。| 容器1 | 容器2 | 容器3 | |
| 容器体积(mL) | 200 | 100 | 200 |
| 反应温度(°C) | 400 | 400 | 500 |
| 平衡常数 | K 1 | K 2 | K 3 |
| HI的平衡浓度(mol⋅L-1) | c 1 | c 2 | c 3 |
| 达平衡的时间(s) | t 1 | t 2 | t 3 |
| H2的平衡转化率 | α1 | α2 | α3 |
| A.c 3<c 1< c 2 | B.t 1 > t 3 | C.K 1= K 2<K 3 | D.α1=α2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知:3CH4(g)+2N2(g) 3C(s)+4NH3(g) ΔH>0,在700 ℃,CH4与N2在不同物质的量之比
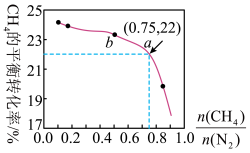
3C(s)+4NH3(g) ΔH>0,在700 ℃,CH4与N2在不同物质的量之比 时CH4的平衡转化率如图所示。下列说法正确的是( )
时CH4的平衡转化率如图所示。下列说法正确的是( )

 3C(s)+4NH3(g) ΔH>0,在700 ℃,CH4与N2在不同物质的量之比
3C(s)+4NH3(g) ΔH>0,在700 ℃,CH4与N2在不同物质的量之比 时CH4的平衡转化率如图所示。下列说法正确的是( )
时CH4的平衡转化率如图所示。下列说法正确的是( )

A. 越大,CH4的平衡转化率越高 越大,CH4的平衡转化率越高 |
B. 不变时,若升温,NH3的体积分数会增大 不变时,若升温,NH3的体积分数会增大 |
| C.b点对应的平衡常数比a点的大 |
| D.a点对应的NH3的体积分数约为26% |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知2HI(g)⇌H2(g) +I2(g), 443℃时IL密闭容器中充入1 mol HI,体系中c(HI)与反应时间t的关系如图所示。下列说法正确的是
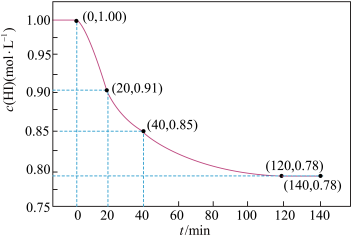

| A.0~20 min内,v(H2) = 0.0045mol·L-1·min-1 | B.升高温度,HI会完全分解 |
| C.40 min时,c(H2) = 0.075mol·L-1 | D.120 min反应达到最大限度,此时HI的转化率为78% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】 。相同温度下,按初始物质不同进行两组实验,浓度随时间的变化如表。下列分析
。相同温度下,按初始物质不同进行两组实验,浓度随时间的变化如表。下列分析不正确 的是
 。相同温度下,按初始物质不同进行两组实验,浓度随时间的变化如表。下列分析
。相同温度下,按初始物质不同进行两组实验,浓度随时间的变化如表。下列分析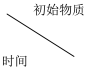 | 0 | 20 | 40 | 60 | 80 |
实验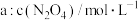 | 0.10 | 0.07 | 0.045 | 0.04 | 0.04 |
实验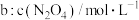  | 0.10 0.20 | …… | |||
A. ,实验a中 ,实验a中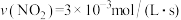 |
B.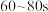 ,实验a中反应处于平衡状态, ,实验a中反应处于平衡状态, 的转化率为60% 的转化率为60% |
C.实验b中,反应向生成 的方向移动,直至达到平衡 的方向移动,直至达到平衡 |
| D.实验a、b达到化学平衡后,提高温度,反应体系颜色均加深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】恒温恒容下,向2L密闭容器中加入MgSO4(s)和CO(g),发生反应:MgSO4(s)+CO(g)  MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:
MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:
下列说法正确的是( )
 MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:
MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:| 反应时间/min | n(MgSO4)/mol | n(CO)/mol | n(SO2)/mol |
| 0 | 2.0 | 2.0 | 0 |
| 2 | 0.8 | ||
| 4 | 1.2 | ||
| 6 | 1.2 | 2.8 |
下列说法正确的是( )
| A.0~2min内的平均速率为v(CO)=0.6mol/(L·min) |
| B.4min后,平衡移动的原因可能是向容器中加入了2.2mol的SO2 |
| C.若升高温度,反应的平衡常数变为1.0,则正反应为放热反应 |
| D.其他条件不变,若起始时容器中MgSO4、CO均为1.0mol,则平衡时n(SO2)>0.6mol |
您最近一年使用:0次